Die Informationen Auf Dieser Website Stellen Keine Medizinische Beratung Dar. Wir Verkaufen Nichts. Die Richtigkeit Der Übersetzung Wird Nicht Garantiert. Haftungsausschluss
Antibiotika, LincosamidCleocin IV
Drogenzusammenfassung
Was ist Cleocin?
Cleocin (Clindamycin) ist ein Antibiotikum, das zur Behandlung schwerer Infektionen verwendet wird, die durch anfällige anaeroben Bakterien verursacht werden. Cleocin ist in generischer Form erhältlich.
Was sind Nebenwirkungen von Cleocin?
Cleocin IV
- Nesselsucht
- Schwierigkeiten beim Atmen
- Schwellung Ihrer Gesichtslippen Zunge oder Hals
- anhaltender Durchfall
- Bauchschmerzen
- Krämpfen
- Blut oder Schleim in Ihrem Stuhl
- Schmerzen oder Schwellungen an der Injektionsstelle
- dunkler Urin
- Gelben der Haut oder Augen (Gelbsucht)
- anhaltende Übelkeit oder Erbrechen
- Änderung der Urinmenge
- einfache Blutergüsse oder Blutergüsse
- Gelenkschmerzen
- Fieber
- anhaltend Halsschmerzen
- Schneller langsamer oder unregelmäßiger Herzschlag
- Ohnmacht und
- schwerer Schwindel
Holen Sie sich sofort medizinische Hilfe, wenn Sie eines der oben aufgeführten Symptome haben.
Nebenwirkungen von Cleocin umfassen:
Was ist D-Amphetaminsalz
- Bauchschmerzen
- Pseudomembran Colitis
- Speiseröhre
- Brechreiz
- Erbrechen
- Durchfall
- unangenehmer oder metallischer Geschmack im Mund (wenn Cleocin in eine Vene injiziert wird)
- Schmerzen und Schwellungen an der Injektionsstelle (wenn Cleocin in einen Muskel injiziert wird)
- Überempfindlichkeitsreaktionen (Hautausschlag und Nesselsucht)
- Juckreiz
- Vaginalinfektion und
- Gelben von Haut und Augen (Gelbsucht).
Sagen Sie Ihrem Arzt, wenn Sie ernsthafte Nebenwirkungen von Cleocin haben, einschließlich:
- Schmerzen oder Schwellungen am Injektionsort (wenn dieses Medikament in eine Vene injiziert wird)
- dunkler Urin
- vergilbende Augen oder Haut
- anhaltende Übelkeit oder Erbrechen
- Eine Änderung der Urinmenge
- einfache Blutergüsse oder Blutungen
- Schmerzen in mehreren Gelenken
- Neue Anzeichen einer Infektion (z. B. Fieber anhaltend Halsschmerzen)
- Schneller/langsamer/unregelmäßiger Herzschlag oder
- Ohnmacht.
Suchen Sie medizinische Versorgung oder rufen Sie auf einmal 911 an, wenn Sie die folgenden schwerwiegenden Nebenwirkungen haben:
- Schwerwiegende Augensymptome wie plötzlicher Sehverlust verschwommenes Sehen Tunnel Sehschmerzen oder Schwellungen oder Halos in der Umgebung des Lichts;
- Schwerwiegende Herzsymptome wie schnelle unregelmäßige oder pochende Herzschläge; Flattern in deiner Brust; Kurzatmigkeit; und plötzliche Schwindel -Benommenheit oder ohnmächtig;
- Starke Kopfschmerzen Verwirrung verwirrt Spracharm oder Bein Schwäche Schwierigkeiten beim Verlust der Koordination unstabil sehr steifes Muskeln hoher Fieber problemlos Schwitzen oder Zittern.
Dieses Dokument enthält nicht alle möglichen Nebenwirkungen und andere können auftreten. Wenden Sie sich an Ihren Arzt nach zusätzlichen Informationen zu Nebenwirkungen.
Dosierung für Cleocin
Die empfohlene Dosis von Cleocin für Erwachsene beträgt alle 6 Stunden 150-450 mg oral oder intravenöse Dosen von 600-2700 mg täglich in 2-4 geteilten Dosen.
Welche Medikamentenstoffe oder Nahrungsergänzungsmittel interagieren mit Cleocin?
Cleocin kann mit anderen neuromuskulären Blockierungsmitteln erythromycin und hormonelle Geburtenkontrolle interagieren. Sagen Sie Ihrem Arzt alle Medikamente und Nahrungsergänzungsmittel, die Sie verwenden.
Cleocin während der Schwangerschaft und Stillen
Cleocin wurde bei schwangeren Frauen nicht angemessen bewertet. Cleocin sollte während der Schwangerschaft nur dann verwendet werden, wenn es eindeutig benötigt wird. Cleocin geht in die Muttermilch ein und könnte unerwünschte Auswirkungen auf ein Pflegekind haben. Wenden Sie sich vor dem Stillen an Ihren Arzt.
Weitere Informationen
Unser Cleocin Side Effects Drug Center bietet einen umfassenden Überblick über die verfügbaren Arzneimittelinformationen über die potenziellen Nebenwirkungen bei der Einnahme dieses Medikaments.
FDA -Drogeninformationen
- Drogenbeschreibung
- Indikationen
- Dosierung
- Nebenwirkungen
- Wechselwirkungen mit Arzneimitteln
- Warnungen
- Vorsichtsmaßnahmen
- Überdosis
- Klinische Pharmakologie
- Medikamentenhandbuch
WARNUNG
C Lostridium hart -Anterendurchfall (CDAD) wurde unter Verwendung fast aller antibakteriellen Mittel, einschließlich Cleocin -Phosphat, berichtet und kann von leichten Durchfall bis zu tödlicher Kolitis reichen. Die Behandlung mit antibakteriellen Wirkstoffen verändert die normale Flora des Dickdarms C. schwierig .
Da die Cleocin -Phosphat -Therapie mit schwerer Kolitis in Verbindung gebracht wurde, die tödlich enden kann, sollte sie schwerwiegende Infektionen vorbehalten sein, bei denen weniger toxische antimikrobielle Wirkstoffe wie in den Indikationen und den Verwendungsabschnitt beschrieben sind. Es sollte nicht bei Patienten mit nicht bakteriellen Infektionen wie den meisten Infektionen der oberen Atemwege angewendet werden. C. schwierig Produziert Toxine A und B, die zur Entwicklung von CDAD beitragen. Hypertoxin produzieren Stämme von C. schwierig verursachen erhöhte Morbidität und Mortalität, da diese Infektionen gegenüber der antimikrobiellen Therapie refraktär sein können und möglicherweise eine Kolektomie erfordern. CDAD muss bei allen Patienten berücksichtigt werden, die nach Antibiotika -Anwendung mit Durchfall auftreten. Eine sorgfältige Anamnese ist erforderlich, da CDAD über zwei Monate nach der Verabreichung von Antibakterienmeistern berichtet wurde.
Wenn CDAD vermutet wird oder bestätigt wird C. schwierig Möglicherweise muss eingestellt werden. Geeignete Flüssigkeits- und Elektrolytmanagement -Protein -Supplementierung Antibiotika -Behandlung von C. schwierig und die chirurgische Bewertung sollte als klinisch angegeben eingeleitet werden.
Beschreibung für Cleocin I.V.
Die sterile Cleocin -Phosphat -Lösung in Fläschchen enthält Clindamycinphosphat, ein wasserlösliches Ester von Clindamycin und Phosphorsäure. Jedes ML enthält das Äquivalent von 150 mg Clindamycin 0,5 mg Dinatrium -Edetat und 9,45 mg Benzylalkohol, der in jeder ML als Konservierungsmittel zugesetzt wurde. Clindamycin ist ein semisynthetisches Antibiotikum, das durch eine 7 (s) -Schlor-Substitution der 7 (R) -Hydroxylgruppe der Elternverbindungs-Lincomycin produziert wird.
Der chemische Name von Clindamycin-Phosphat ist L- Richtung -Anzeige- Galacto -Octopyranosid methyl-7-chlor-678-trideoxy-6-[[(1-Methyl-4-Propyl-2-pyrrolidinyl) carbonyl] Amino -1-thio- 2- (Dihydrogenphosphat) (2S- trans )-.
Die molekulare Formel ist c 18 H 34 Essen 2 0 8 PS und das Molekulargewicht beträgt 504,96.
Die strukturelle Formel ist unten dargestellt:
 |
Cleocin-Phosphat in der Add-Valance-Fläschchen ist nur nach einer weiteren Verdünnung mit einem geeigneten Volumen der Add-Vantage-Verdünnungsbasislösung für den intravenösen Gebrauch bestimmt (sehen Gebrauchsanweisung ).
Die Cleocin -Phosphat -IV -Lösung im Galaxy -Kunststoffbehälter zur intravenösen Verwendung besteht aus Clindamycin -Phosphat, die 300 600 und 900 mg Clindamycin entsprechen, die mit 5% Dextrose als sterile Lösung vormischt wurde. Dinatrium -Edetat wurde bei einer Konzentration von 0,04 mg/ml zugegeben. Der pH -Wert wurde mit Natriumhydroxid und/oder Salzsäure eingestellt.
Der Kunststoffbehälter besteht aus einem speziell entwickelten mehrschichtigen Plastik -Plastik -PL 2501. Lösungen, die mit dem Kunststoffbehälter in Kontakt sind, können bestimmte chemische Komponenten in sehr geringen Mengen innerhalb der Ablaufzeit ausstreichen. Die Eignung des Kunststoffs wurde in Tests bei Tieren gemäß den USP -biologischen Tests für Kunststoffbehälter sowie durch Tissue -Kultur -Toxizitätsstudien bestätigt.
Verwendung für Cleocin I.V.
Cleocin -Phosphatprodukte sind bei der Behandlung schwerwiegender Infektionen angezeigt, die durch anfällige anaeroben Bakterien verursacht werden.
Cleocin -Phosphatprodukte sind auch bei der Behandlung schwerwiegender Infektionen aufgrund anfälliger Stämme von Streptokokken -Pneumokokken und Staphylococci angezeigt. Seine Verwendung sollte penicillin-allergischen Patienten oder anderen Patienten vorbehalten sein, für die im Urteil des Arztes ein Penicillin unangemessen ist. Aufgrund des Risikos einer antibiotika-assoziierten pseudomembranischen Kolitis, wie in der beschrieben WARNUNG BOXED Vor der Auswahl von Clindamycin sollte der Arzt die Art der Infektion und die Eignung weniger toxischer Alternativen (z. B. Erythromycin) berücksichtigen.
Bakteriologische Studien sollten durchgeführt werden, um die ursächlichen Organismen und ihre Anfälligkeit für Clindamycin zu bestimmen.
Die angegebenen chirurgischen Eingriffe sollten in Verbindung mit einer Antibiotikatherapie durchgeführt werden.
Cleocin -Phosphat ist bei der Behandlung schwerwiegender Infektionen angezeigt, die durch anfällige Stämme der festgelegten Organismen unter den unten aufgeführten Bedingungen verursacht werden:
Infektionen der unteren Atemwege, einschließlich Lungenentzündung, und Lungenabszess, die durch Anaerobes verursacht werden Streptococcus pneumoniae Andere Streptococci (außer E. faecalis ) Und Staphylococcus aureus.
Haut- und Hautstrukturinfektionen durch verursacht durch Streptococcus pyogenes Staphylococcus aureus und Anaerobes.
Gynäkologische Infektionen einschließlich Endometritis-Nongonokokken-Tube-Ovarian-Abszess-Beckenzellulitis und postoperativer Vaginalmanschetteninfektion, die durch anfällige Anaerobie verursacht werden.
Intraabdominale Infektionen, einschließlich Peritonitis und intraabdominaler Abszess, verursacht durch anfällige anaerobe Organismen.
Septikämie verursacht durch Staphylococcus aureus Streptococci (außer Enterococcus faecalis ) Und susceptible anaerobes.
Knochen- und Gelenkinfektionen einschließlich akuter hämatogener Osteomyelitis durch verursacht durch Staphylococcus aureus und als zusätzliche Therapie bei der chirurgischen Behandlung chronischer Knochen- und Gelenkinfektionen aufgrund anfälliger Organismen.
Um die Entwicklung von medikamentenresistenten Bakterien zu verringern und die Wirksamkeit von Cleocin-Phosphat und anderen antibakteriellen Arzneimitteln aufrechtzuerhalten, sollte Cleocin-Phosphat nur zur Behandlung oder Vorbeugung von Infektionen verwendet werden, die nachgewiesen oder stark durch anfällige Bakterien verursacht werden. Wenn Kultur- und Anfälligkeitsinformationen verfügbar sind, sollten sie bei der Auswahl oder Modifizierung der antibakteriellen Therapie in Betracht gezogen werden. In Ermangelung solcher Daten können lokale Epidemiologie- und Empfindlichkeitsmuster zur empirischen Auswahl der Therapie beitragen.
Dosierung für Cleocin I.V.
Wenn während der Therapie Durchfall auftritt, sollte dieses Antibiotikum abgesetzt werden (siehe Boxwarnung ).
Clindamycin -Phosphat -IM -Verabreichung sollte unverdünnt verwendet werden.
Bacopa Monnieri Vorteile und Nebenwirkungen
Die Verabreichung von Clindamycin -Phosphat IV sollte verdünnt werden (sehen Verdünnung für die IV -Verwendung und IV -Infusionsraten unten).
Erwachsene
Parenteral (IM- oder IV-Verabreichung): schwerwiegende Infektionen aufgrund aerobe grampositive Kokken und anfälligeren Anaerobiers (nicht allgemein einbezogen Bacteroides fragilis peptococcus Spezies und Clostridium andere Arten als Clostridium perfringens ):
600.1200 mg/Tag in 2 3 oder 4 gleiche Dosen.
Schwerwiegendere Infektionen, insbesondere solche, die nachgewiesen oder vermutet wurden Bacteroides fragilis peptococcus Spezies oder Clostridium species anders als Clostridium perfringens:
1200.2700 mg/Tag in 2 3 oder 4 gleiche Dosen.
Für schwerwiegendere Infektionen müssen diese Dosen möglicherweise erhöht werden. In lebensbedrohlichen Situationen aufgrund von Aerobes oder Anaerobes können diese Dosen erhöht werden. Dosen von bis zu 4800 mg täglich wurden intravenös für Erwachsene gegeben. Sehen Verdünnung für die IV -Verwendung und IV -Infusionsraten Abschnitt unten.
Einzelne intramuskuläre Injektionen von mehr als 600 mg werden nicht empfohlen.
Alternativ kann das Arzneimittel in Form einer einzelnen schnellen Infusion der ersten Dosis verabreicht werden, gefolgt von einer kontinuierlichen IV -Infusion wie folgt:
| Aufrechterhaltung des Serum Clindamycinspiegels | Schnelle Infusionsrate | Wartungsinfusionsrate |
| Über 4 mcg/ml | 10 mg/min für 30 min | 0,75 mg/min |
| Über 5 mcg/ml | 15 mg/min für 30 min | 1,00 mg/min |
| Über 6 mcg/ml | 20 mg/min für 30 min | 1,25 mg/min |
Neugeborene (weniger als 1 Monat)
15 bis 20 mg/kg/Tag in 3 bis 4 gleichen Dosen. Die niedrigere Dosierung kann für kleine Vorräte angemessen sein.
Kinderpatienten 1 Monat bis 16 Jahre alt
Parenteral (IM oder IV) Verabreichung: 20 bis 40 mg/kg/Tag in 3 oder 4 gleichen Dosen. Die höheren Dosen würden für schwerere Infektionen verwendet. Als Alternative zur Dosierung von Körpergewichtsbasis können pädiatrische Patienten auf der Grundlage der Quadratmeter -Körperoberfläche dosiert werden: 350 mg/m 2 /Tag für schwere Infektionen und 450 mg/m 2 /Tag für schwerere Infektionen.
Eine parenterale Therapie kann in orale Pädiatrikr -Cleocin -Pediatricr umgewandelt werden ® Aroma -Granulat (Clindamycin Palmitathydrochlorid) oder Cleocin HClR ® Kapseln (Clindamycinhydrochlorid), wenn der Zustand und nach Ermessen des Arztes garantiert werden.
Bei β-hemolytischen Streptokokkeninfektionen sollte die Behandlung mindestens 10 Tage lang fortgesetzt werden.
Verdünnung für die IV -Verwendung und IV -Infusionsraten: The concentration of clindamycin in diluent for infusion should not exceed 18 mg per mL. Infusion rates should not exceed 30 mg per minute. Die üblichen Infusionsverdünnungen und -raten sind wie folgt:
| Dosis | Verdünnung | Zeit |
| 300 mg | 50 ml | 10 min |
| 600 mg | 50 ml | 20 min |
| 900 mg | 50-100 ml | 30 min |
| 1200 mg | 100 ml | 40 min |
Die Verabreichung von mehr als 1200 mg in einer einzelnen 1-stündigen Infusion wird nicht empfohlen.
Parenterale Arzneimittel sollten vor der Verabreichung visuell auf Partikel und Verfärbungen untersucht werden, wenn Lösung und Behälter dies zulassen.
Verdünnung und Kompatibilität
Physikalische und biologische Kompatibilitätsstudien, die 24 Stunden bei Raumtemperatur überwacht wurden, haben keine Inaktivierung oder Inkompatibilität unter Verwendung von Cleocin -Phosphat -steriler Lösung (Clindamycin -Phosphat) in IV -Lösungen, die Natriumchlorid -Glukosecalcium oder Kalium und Lösungen in Konzentrationen enthalten, in Konzentrationen, die normalerweise klinisch verwendet werden, vorgewiesen. Mit dem Antibiotika Cephalothin Kanamycin Gentamicin Penicillin oder Carbenicillin wurde keine Inkompatibilität nachgewiesen.
Die folgenden Medikamente sind mit Clindamycin -Phosphat physisch inkompatibel: Ampicillin -Natrium -Phenytoin -Natrium -Barbiturate Aminophyllin Calciumgluconat und Magnesiumsulfat.
Die Kompatibilität und Dauer der Stabilität von Arzneimittelbeimgen variieren je nach Konzentration und anderen Erkrankungen. Für aktuelle Informationen zu Kompatibilitäten von Clindamycin -Phosphat unter bestimmten Bedingungen wenden Sie sich bitte an die Medical and Drug Information Unit Pharmacia
Physikalisch-chemische Stabilität verdünnte Lösungen von Cleocin-Phosphat-Raumtemperatur
6 9 und 12 mg/ml (äquivalent zur Clindamycin -Basis) in der Dextrose -Injektion 5% Natriumchloridinjektion 0,9% oder laktierte Ringer -Injektion in Glasflaschen oder Minibags zeigten mindestens 16 Tage bei 25 ° C physikalische und chemische Stabilität. Auch 18 mg/ml (entsprechend der Clindamycin -Base) in Dextrose -Injektion 5% in Minibags zeigte mindestens 16 Tage bei 25 ° C physikalische und chemische Stabilität.
Kühlung
6 9 und 12 mg/ml (äquivalent zur Clindamycin -Basis) in der Dextrose -Injektion 5% Natriumchloridinjektion 0,9% oder laktierte Ringer -Injektion in Glasflaschen oder Minibags zeigten mindestens 32 Tage bei 4 ° C physikalische und chemische Stabilität.
WICHTIG: Diese Informationen zur chemischen Stabilität zeigt in keiner Weise an, dass es eine akzeptable Praxis wäre, dieses Produkt nach der Vorbereitungszeit gut zu verwenden. Eine gute berufliche Praxis deutet darauf hin, dass zusammengesetzte Beimischungen so bald nach der Vorbereitung verwaltet werden sollten.
Gefroren
6 9 und 12 mg/ml (äquivalent zur Clindamycin -Basis) in der Dextrose -Injektion 5% Natriumchloridinjektion 0,9% oder laktierte Ringer -Injektion in Minibags zeigten mindestens acht Wochen bei -10 ° C physikalische und chemische Stabilität.
Gefroren solutions should be thawed at room temperature and not refrozen.
Anweisungen zum Abgeben
Apothekenpaket
Nicht für direkte Infusion
Das Pharmacy Bulk -Paket dient zur Verwendung in einem Apothekenmischungsservice nur unter einer laminaren Flusshaube. Der Eintritt in die Fläschchen sollte mit einem sterilen Übertragungssatz mit kleinem Durchmesser oder einem anderen sterilen Abspendungsgerät mit kleinem Durchmesser und in Aliquots unter Verwendung der aseptischen Technik ausgegebenen Inhalte durchgeführt werden. Mehrere Einträge mit Nadel und Spritze werden nicht empfohlen. Verwenden Sie nach dem Eintritt den gesamten Inhalt der Fläschchen umgehend. Jeder ungenutzte Teil muss innerhalb von 24 Stunden nach dem ersten Eintritt verworfen werden.
Gebrauchsanweisung
Cleocin -Phosphat -IV -Lösung in Galaxien -Kunststoffbehälter
Die vorgemischte Cleocin -Phosphat -IV -Lösung dient der intravenösen Verabreichung unter Verwendung steriler Geräte. Überprüfen Sie, ob Sie vor dem Gebrauch auf winzige Lecks durch festen Taschen eintreffen. Wenn Lecks als Verwirrungslösung festgestellt werden, kann die Sterilität beeinträchtigt werden. Zusätzliche Medikamente hinzufügen. Parenterale Arzneimittel sollten vor der Verabreichung visuell auf Partikel und Verfärbungen untersucht werden, wenn Lösung und Behälter dies zulassen. Verwenden Sie nicht, es sei denn, die Lösung ist klar und das Siegel ist intakt.
Vorsicht
Verwenden Sie keine Kunststoffbehälter in Reihe von Anschlüssen. Eine solche Verwendung könnte zu Luftembolien führen, da die verbleibende Luft aus dem Primärbehälter entnommen wird, bevor die Flüssigkeit aus dem sekundären Behälter abgeschlossen ist.
Vorbereitung für die Verwaltung
- Behälter aus Ösenunterstützung aussetzen.
- Entfernen Sie den Beschützer vom Auslassanschluss am Boden des Behälters.
- Anhängen Administrationssatz. Siehe vollständige Anweisungen, die einhergehören.
Herstellung von Cleocin-Phosphat im Add-Vorture-System- . Für IV nur verwenden. Cleocin -Phosphat 300 mg 600 mg und 900 mg können in 50 ml (für 300 mg und 600 mg) oder 100 ml (für 900 mg) Dextrose -Injektion 5% oder Natriumchloridinjektion 0,9% im ADD -DIS -DISTROSE -Behälter rekonstituiert werden. Siehe separate Anweisungen für das Add-Vantage-System.
Wie geliefert
Jede ml von Cleocin -Phosphat Die sterile Lösung enthält Clindamycin -Phosphat -äquivalent zu 150 mg Clindamycin 0,5 mg Dinatrium edetat 9,45 mg Benzylalkohol, das als Konservierungsmittel zugesetzt wurde. Bei Bedarf wird der pH -Wert mit Natriumhydroxid und/oder Salzsäure eingestellt. Cleocin -Phosphat ist in den folgenden Paketen erhältlich:
25-2 ml Fläschchen NDC 0009-0870-26
25-4 ml Fläschchen NDC 0009-0775-26
25-6 ml Fläschchen NDC 0009-0902-18
5-60 ml Apothekenpaket NDC 0009-0728-09
Cleocin -Phosphat wird wie folgt in add-vorteile-Fläschchen geliefert:
| NDC | Fläschchengröße | Total Clindamycin Phosphat/Fläschchen |
| 0009-6582-01 | 25-2 ml Fläschchen | 300 mg |
| 0009-3124-03 | 25-4 ml Fläschchen | 600 mg |
| 0009-3447-03 | 25-6 ml Fläschchen | 900 mg |
Lagern Sie bei kontrollierter Raumtemperatur von 20 ° bis 25 ° C (68 ° bis 77 ° F) [siehe USP].
Cleocin -Phosphat IV Solution In Galaxy -Kunststoffbehältern ist eine sterile Lösung von Clindamycin -Phosphat mit 5% Dextrose. Die einzelnen Dosis Galaxy -Kunststoffbehälter sind wie folgt erhältlich:
24-300 mg/50 ml Behälter NDC 0009-3381-02
24-600 mg/50 ml Behälter NDC 0009-3375-02
24-900 mg/50 ml Behälter NDC 0009-3382-02
Die Exposition von pharmazeutischen Produkten zur Wärme sollte minimiert werden. Es wird empfohlen, Galaxien -Kunststoffbehälter bei Raumtemperatur (25 ° C) aufzubewahren. Vermeiden Sie Temperaturen über 30 ° C.
Verteilt von: Pfizer Pharmacia
Nebenwirkungen for Cleocin I.V.
Die folgenden Reaktionen wurden unter Verwendung von Clindamycin gemeldet.
Infektionen und Befall: Clostridium difficile Kolitis
Magen -Darm: Antibiotika-assoziierte Kolitis (siehe WARNUNGS ) Pseudomembranische Kolitis Bauchschmerz Übelkeit und Erbrechen. Der Beginn der Symptome von Pseudomembran -Colitis kann während oder nach antibakterieller Behandlung auftreten (siehe WARNUNGS ). An unpleasant or metallic taste has been reported after intravenous administration of the higher doses of clindamycin phosphate.
Überempfindlichkeitsreaktionen: Während der medikamentösen Therapie wurden makulopapuläre Hautausschlag und Urtikaria beobachtet. Verallgemeinerte leichte bis mittelschwere morbilliforme Hautausschläge sind die am häufigsten gemeldeten Nebenwirkungen.
Schwere Hautreaktionen wie eine toxische epidermale Nekrolyse, einige mit tödlichem Ergebnis wurden berichtet (siehe WARNUNGS ). Cases of Acute Allgemeinized Exanthematous Pustulosis (AGEP) erythema multiforme some resembling Stevens-Johnson syndrome have been associated with clindamycin. Anaphylactic shock anaphylactic reaction and hypersensitivity have also been reported (sehen WARNUNGS ).
Haut und Schleimhäute: Pruritus -Vaginitis -Angioödeme und seltene Fälle von Peeling -Dermatitis wurden berichtet (siehe Überempfindlichkeitsreaktionen ).
Leber: Während der Clindamycin -Therapie wurden Gelbsucht und Anomalien bei Leberfunktionstests beobachtet.
Nieren: Obwohl keine direkte Beziehung von Clindamycin zu Nierenschäden festgestellt wurde, wurde eine Nierenfunktionsstörung festgestellt, wie durch Azotämie -Oligurie und/oder Proteinurie belegt wurde.
Hämatopoetisch: Übergangsneutropenie (Leukopenie) und Eosinophilie wurden berichtet. Es wurden Berichte über Agranulozytose und Thrombozytopenie erstellt. Bei einer der Vorstehenden konnte keine direkte ätiologische Beziehung zur gleichzeitigen Clindamycin -Therapie hergestellt werden.
Immunsystem: Es wurde Fälle von Arzneimitteln mit Eosinophilie und systemischen Symptomen (Kleider) berichtet.
Lokale Reaktionen: Die Injektionsstelle Irritation Schmerzverdauerung und steriler Abszess wurden nach intramuskulärer Injektion und Thrombophlebitis nach intravenöser Infusion berichtet. Reaktionen können minimiert oder vermieden werden, indem tiefe intramuskuläre Injektionen angezeigt und die längere Verwendung von intrennen intravenösen Kathetern vermieden werden.
Muskuloskelett: Es wurden Fälle von Polyarthritis berichtet.
Herz -Kreislauf: Kardiopulmonaler Verhaftung und Hypotonie wurden nach einer zu schnellen intravenösen Verabreichung berichtet (siehe Dosierung und Verwaltung ).
Wechselwirkungen mit Arzneimitteln for Cleocin I.V.
Es wurde gezeigt, dass Clindamycin neuromuskuläre Blockierungseigenschaften aufweist, die die Wirkung anderer neuromuskulärer Blocker verbessern können. Daher sollte es bei Patienten, die solche Wirkstoffe erhalten, mit Vorsicht verwendet werden.
Top-Reiseziele in den USA
Clindamycin wird vorwiegend durch CYP3A4 und in geringerem Maße von CYP3A5 zum Hauptmetaboliten Clindamycinsulfoxid und dem kleinen Metaboliten-N-Desmethylclindamycin metabolisiert. Daher können Inhibitoren von CYP3A4 und CYP3A5 die Plasmakonzentrationen von Clindamycin erhöhen, und Induktoren dieser Isoenzyme können die Plasmakonzentrationen von Clindamycin verringern. In Gegenwart starker CYP3A4 -Inhibitoren überwachen auf unerwünschte Reaktionen. In Gegenwart starker CYP3A4 -Induktoren wie Rifampicin -Monitor für den Wirksamkeitsverlust.
In vitro Studien zeigen, dass Clindamycin CYP1A2 CYP2C9 CYP2C19 CYP2E1 oder CYP2D6 nicht hemmt und nur mäßig CYP3A4 hemmt.
Antagonismus wurde zwischen Clindamycin und Erythromycin gezeigt in vitro . Aufgrund möglicher klinischer Bedeutung sollten die beiden Medikamente nicht gleichzeitig verabreicht werden.
Warnungen for Cleocin I.V.
Sehen Boxwarnung .
Clostridium Difficile Associated Diarrhea
Clostridium difficile Assoziiertes Durchfall (CDAD) wurde unter Verwendung von nahezu allen antibakteriellen Wirkstoffen, einschließlich Cleocin -Phosphat, berichtet und kann von leichten Durchfall bis zu tödlicher Kolitis reichen. Die Behandlung mit antibakteriellen Wirkstoffen verändert die normale Flora des Dickdarms C. schwierig .
C. schwierig Produziert Toxine A und B, die zur Entwicklung von CDAD beitragen. Hypertoxin produzieren Stämme von C. schwierig verursachen erhöhte Morbidität und Mortalität, da diese Infektionen gegenüber der antimikrobiellen Therapie refraktär sein können und möglicherweise eine Kolektomie erfordern. CDAD muss bei allen Patienten berücksichtigt werden, die nach Antibiotika -Anwendung mit Durchfall auftreten. Eine sorgfältige Anamnese ist erforderlich, da CDAD über zwei Monate nach der Verabreichung von Antibakterienmeistern berichtet wurde.
Wenn CDAD vermutet wird oder bestätigt wird C. schwierig Möglicherweise muss eingestellt werden. Geeignete Flüssigkeits- und Elektrolytmanagement -Protein -Supplementierung Antibiotika -Behandlung von C. schwierig und die chirurgische Bewertung sollte als klinisch angegeben eingeleitet werden.
Anaphylaktische und schwere Überempfindlichkeitsreaktionen
Es wurden anaphylaktische Schock- und anaphylaktische Reaktionen berichtet (siehe Nebenwirkungen ).
Schwere Überempfindlichkeitsreaktionen, einschließlich schwerer Hautreaktionen wie toxische epidermale Nekrolyse (zehn) Arzneimittelreaktion mit Eosinophilie und systemischen Symptomen (Kleid) und Stevens-Johnson-Syndrom (SJS), von denen einige mit tödlichem Ergebnis berichtet wurden (siehe Nebenwirkungen ).
Bei einer solchen anaphylaktischen oder schweren Überempfindlichkeitsreaktion werden die Behandlung dauerhaft eingestellt und eine angemessene Therapie einführen.
Eine sorgfältige Untersuchung sollte zu früheren Empfindlichkeiten gegenüber Drogen und anderen Allergenen durchgeführt werden.
Benzylalkoholtoxizität bei pädiatrischen Patienten (nach Luft schnappendes Syndrom)
Dieses Produkt enthält Benzylalkohol als Konservierungsmittel. Der konservative Benzylalkohol wurde mit schwerwiegenden unerwünschten Ereignissen in Verbindung gebracht, einschließlich des Ggasing -Syndroms und des Todes bei pädiatrischen Patienten. Obwohl normale therapeutische Dosen dieses Produkts normalerweise Mengen an Benzylalkohol liefern, die wesentlich niedriger sind als die, die in Verbindung mit dem Asping -Syndrom angegeben sind, ist die Mindestmenge an Benzylalkohol, bei der Toxizität auftreten kann, nicht bekannt.
Das Risiko einer Benzylalkoholtoxizität hängt von der verabreichten Menge und der Kapazität der Leber und der Nierenkapazität zur Entgiftung der Chemikalie ab. Frühgeborene und niedrige Geburtsgewichtsfants entwickeln möglicherweise eher Toxizität.
Verwendung bei Meningitis
Da Clindamycin nicht ausreichend in die Cerebrospinalflüssigkeit diffundiert, sollte das Medikament bei der Behandlung von Meningitis nicht eingesetzt werden.
Vorsichtsmaßnahmen for Cleocin I.V.
Allgemein
Die bisherige Überprüfung der Erfahrungen legt nahe, dass eine Untergruppe älterer Patienten mit schwerer schwerer Krankheit durch Durchfall weniger gut vertragen kann. Wenn Clindamycin bei diesen Patienten angezeigt wird, sollten sie sorgfältig auf die Änderung der Darmfrequenz überwacht werden.
Cleocin -Phosphat products should be prescribed with caution in individuals with a history of gastrointestinal disease particularly Kolitis.
Cleocin -Phosphat should be prescribed with caution in atopic individuals.
Bestimmte Infektionen können zusätzlich zur Antibiotikatherapie in Einschnitt und Entwässerung oder anderer angegebener chirurgischer Eingriff erforderlich sein.
Die Verwendung von Cleocin-Phosphat kann zu einem Überwachsen von nicht maßgeblichen Organismen, die partikulär Hefenwachsen sind. Sollten Superinfektionen auftreten, sollten geeignete Maßnahmen ergriffen werden, wie in der klinischen Situation angezeigt.
Cleocin -Phosphat should not be injected intravenously undiluted as a bolus but should be infused over at least 10-60 minutes as directed in the Dosierung und Verwaltung Abschnitt.
Bei Patienten mit Nierenerkrankungen ist möglicherweise nicht erforderlich. Bei Patienten mit mittelschwerer bis schwerer Lebererkrankung wurde eine Verlängerung der Clindamycin-Halbwertszeit gefunden. Aus Studien wurde jedoch postuliert, dass bei der Verabreichung alle acht Stunden Ansammlung selten auftreten sollte. Daher ist eine Dosierungsmodifikation bei Patienten mit Lebererkrankungen möglicherweise nicht erforderlich. Bei der Behandlung von Patienten mit schwerer Lebererkrankung sollten jedoch periodische Bestimmungen zur Leberenzym durchgeführt werden.
Die Verschreibung von Cleocin-Phosphat in Abwesenheit einer nachgewiesenen oder stark vermuteten bakteriellen Infektion oder einer prophylaktischen Indikation ist unwahrscheinlich, dass er dem Patienten einen Nutzen bringt und das Risiko für die Entwicklung von medikamentenresistenten Bakterien erhöht.
Informationen für Patienten
Die Patienten sollten beraten werden, dass antibakterielle Medikamente einschließlich Cleocin -Phosphat nur zur Behandlung von bakteriellen Infektionen eingesetzt werden sollten. Sie behandeln keine Virusinfektionen (z. B. die Erkältung). Wenn Cleocin -Phosphat zur Behandlung einer bakteriellen Infektion verschrieben wird, sollte Patienten gesagt werden, dass es zwar üblich ist, sich früh im Verlauf der Therapie besser zu fühlen, die Medikamente sollten genau wie angewiesen eingenommen werden. Das Überspringen von Dosen oder Nichtabschließung des gesamten Therapieverlaufs kann (1) die Wirksamkeit der sofortigen Behandlung verringern und (2) die Wahrscheinlichkeit erhöhen, dass Bakterien Resistenz entwickeln und in Zukunft nicht durch Cleocin -Phosphat oder andere antibakterielle Arzneimittel behandelt werden können.
Durchfall ist ein häufiges Problem, das durch Antibiotika verursacht wird, das normalerweise endet, wenn das Antibiotikum abgesetzt wird. Manchmal können Patienten nach Beginn der Behandlung mit Antibiotika wässrige und blutige Stühle (mit oder ohne Magenkrämpfe und Fieber) entwickeln, auch bis nach zwei oder mehr Monaten nach der letzten Dosis des Antibiotikums. Wenn dies auftritt, sollten Patienten so bald wie möglich ihren Arzt kontaktieren.
Labortests
Während längerer Therapie sollten periodische Leber- und Nierenfunktionstests und Blutzahlen durchgeführt werden.
Karzinogenese -Mutagenese -Beeinträchtigung der Fruchtbarkeit
Langzeitstudien an Tieren wurden nicht mit Clindamycin durchgeführt, um das krebsigene Potential zu bewerten. Die durchgeführten Genotoxizitätstests umfassten einen Ratten -Mikronukleus -Test und einen Ames -Salmonellen -Reversionstest. Beide Tests waren negativ.
Fertilitätsstudien an Ratten, die oral mit bis zu 300 mg/kg/Tag behandelt wurden (ungefähr das 1,1 -fache der am höchsten empfohlenen adulten menschlichen Dosis basierend auf Mg/M 2 ) zeigten keine Auswirkungen auf die Fruchtbarkeit oder die Paarungsfähigkeit.
Schwangerschaft
Teratogene Wirkungen
In klinischen Studien mit schwangeren Frauen wurde die systemische Verabreichung von Clindamycin während des zweiten und dritten Trimesters nicht mit einer erhöhten Häufigkeit angeborener Anomalien in Verbindung gebracht.
Clindamycin sollte im ersten Trimester der Schwangerschaft nur dann eindeutig eingesetzt werden. Während des ersten Trimesters der Schwangerschaft gibt es bei schwangeren Frauen keine angemessenen und gut kontrollierten Studien bei schwangeren Frauen. Da Studien zur Reproduktion von Tier nicht immer die menschliche Reaktion vorhersagen, sollte dieses Medikament nur dann während der Schwangerschaft angewendet werden, wenn sie eindeutig benötigt werden.
Fortpflanzungsstudien, die an Ratten und Mäusen unter Verwendung oraler Dosen von Clindamycin bis zu 600 mg/kg/Tag durchgeführt wurden (NULL,1 und 1,1 -mal die am höchsten empfohlene erwachsene menschliche Dosis basierend auf Mg/M. 2 bzw. subkutane Dosen von Clindamycin bis zu 250 mg/kg/Tag (NULL,9 und 0,5 -mal die am höchsten empfohlene erwachsene menschliche Dosis basierend auf Mg/M 2 jeweils) zeigten keine Hinweise auf Teratogenität.
Cleocin -Phosphat Sterile Solution contains benzyl alcohol. Benzyl alcohol can cross the placenta. see WARNUNGS .
Pflegemütter
Es wurde berichtet, dass Clindamycin in der Muttermilch im Bereich von 0,7 bis 3,8 mcg/ml bei Dosierungen von 150 mg oral bis 600 mg intravenös auftritt. Clindamycin hat das Potenzial, nachteilige Auswirkungen auf die Magen -Darm -Flora des gestillten Kindes zu haben. Wenn eine orale oder intravenöse Clindamycin von einer stillenden Mutter verlangt wird, ist dies kein Grund, das Stillen einzustellen, aber ein alternatives Medikament kann bevorzugt werden. Überwachen Sie das Kind auf mögliche nachteilige Auswirkungen auf die Magen-Darm-Flora wie Durchfall Candidiasis (Thrush-Windelausschlag) oder selten Blut im Stuhl, was auf mögliche Antibiotika-assoziierte Kolitis hinweist.
Die Entwicklungs- und gesundheitlichen Vorteile des Stillens sollten zusammen mit dem klinischen Bedarf der Mutter nach Clindamycin und potenziellen nachteiligen Auswirkungen des gestillten Kindes von Clindamycin oder aus dem zugrunde liegenden mütterlichen Zustand berücksichtigt werden.
Wien Reiseroute
Pädiatrische Verwendung
Wenn die sterile Cleocin -Phosphat -Lösung an die pädiatrische Bevölkerung (Geburt von 16 Jahren) verabreicht wird, ist eine geeignete Überwachung der Organsystemfunktionen wünschenswert.
Verwendung bei Neugeborenen und Säuglingen
Dieses Produkt enthält Benzylalkohol als Konservierungsmittel. Benzylalkohol wurde bei vorzeitigen Säuglingen mit einem tödlichen „nach Luft schnappenden Syndrom“ in Verbindung gebracht. sehen WARNUNGS .
Das Potenzial für die toxische Wirkung in der pädiatrischen Population aus Chemikalien, die aus der einzelnen Dosis vormischten IV -Präparation in Kunststoff ausstammt, wurde nicht bewertet. sehen WARNUNGS .
Geriatrische Verwendung
Klinische Studien von Clindamycin umfassten nicht eine ausreichende Anzahl von Patienten im Alter von 65 Jahren, um festzustellen, ob sie anders als jüngere Patienten reagieren. Andere berichtete klinische Erfahrung zeigen jedoch, dass Antibiotika-assoziierte Kolitis und Durchfall (aufgrund von Durchfall Clostridium difficile ) In Verbindung mit den meisten Antibiotika treten bei älteren Menschen (> 60 Jahre) häufiger auf und können schwerwiegender sein. Diese Patienten sollten sorgfältig auf die Entwicklung von Durchfall überwacht werden.
Pharmakokinetische Studien mit Clindamycin haben keine klinisch wichtigen Unterschiede zwischen jungen und älteren Probanden mit normaler Leberfunktion und normaler (altersbereinigter) Nierenfunktion nach oraler oder intravenöser Verabreichung gezeigt.
Überdosierungsinformationen für Cleocin I.V.
Bei Mäusen in einer intravenösen Dosis von 855 mg/kg und bei Ratten bei einer oralen oder subkutanen Dosis von ungefähr 2618 mg/kg wurde eine signifikante Mortalität beobachtet. In den Mäusen wurden Krämpfe und Depressionen beobachtet.
Hämodialyse und Peritonealdialyse sind nicht wirksam, um Clindamycin aus dem Serum zu entfernen.
Kontraindikationen für Cleocin I.V.
Dieses Medikament ist bei Personen mit Überempfindlichkeit gegenüber Präparaten, die Clindamycin oder Lincomycin enthalten, kontraindiziert.
Klinische Pharmakologie for Cleocin I.V.
Verteilung
Biologisch inaktives Clindamycin -Phosphat wird in aktives Clindamycin umgewandelt. Bis zum Ende der kurzfristigen intravenösen Infusionspeakserumspiegel von aktivem Clindamycin sind erreicht.
Nach der intramuskulären Injektion des Clindamycin -Phosphatspitzenspitzenspiegels von aktiven Clindamycin werden innerhalb von 3 Stunden bei Erwachsenen und 1 Stunde bei pädiatrischen Patienten erreicht. Serumspegelkurven können aus den IV-Spitzen-Serumspiegeln erstellt werden, wie in Tabelle 1 durch Anwendung der Eliminierungs-Halbwertszeiten angegeben (siehe Ausscheidung ).
Serumspiegel von Clindamycin können über dem erhalten werden in vitro Minimale Hemmkonzentrationen für die meisten angegebenen Organismen durch Verabreichung von Clindamycin -Phosphat alle 8 bis 12 Stunden bei Erwachsenen und alle 6 bis 8 Stunden bei pädiatrischen Patienten oder durch kontinuierliche intravenöse Infusion. Ein Gleichgewichtszustand wird durch die dritte Dosis erreicht.
Selbst in Gegenwart von entzündeten Meningen werden keine signifikanten Clindamycin -Spiegel in der Cerebrospinalflüssigkeit erreicht.
Stoffwechsel
In vitro Studien an menschlichen Leber- und Darmmikrosomen zeigten, dass Clindamycin vorwiegend durch Cytochrom P450 3A4 (CYP3A4) mit geringfügigem Beitrag von CYP3A5 zu Clindamycinsulfoxid und einem minormutschalen Metabolit N-Desmethylcclindamycin metabolisiert wird.
Ausscheidung
Biologisch inaktives Clindamycin -Phosphat verschwindet schnell aus dem Serum; Die durchschnittliche Halbwertszeit beträgt 6 Minuten; Die Halbwertszeit der Serumausscheidung von aktivem Clindamycin beträgt jedoch bei Erwachsenen etwa 3 Stunden und bei pädiatrische Patienten.
Besondere Populationen
Nieren-/Leberbeeinträchtigung
Die Eliminierungs-Halbwertszeit von Clindamycin ist bei Patienten mit einer deutlich reduzierten Nieren- oder Leberfunktion leicht erhöht. Hämodialyse und Peritonealdialyse sind nicht wirksam, um Clindamycin aus dem Serum zu entfernen. Dosierungspläne müssen in Gegenwart einer leichten oder mittelschweren Nieren- oder Lebererkrankung nicht modifiziert werden.
Verwendung bei älteren Menschen
Pharmakokinetische Studien an älteren Freiwilligen (61-79 Jahre) und jüngere Erwachsene (18-39 Jahre) weisen darauf hin, dass das Alter allein die Pharmakokinetik der Clindamycin nicht verändert (Clearance-Elimination-Halbwertsvolumen der Verteilung und Fläche unter der Serumkonzentrationszeitkurve) nach IV-Verabreichung von Clospamycin-Phosphat. Nach oraler Verabreichung der Clindamycin-Hydrochlorid-Eliminierungs-Halbwertszeit erhöht sich bei älteren Menschen auf ungefähr 4,0 Stunden (Bereich 3,4-5,1 h) im Vergleich zu 3,2 Stunden (Bereich 2,1 bis 4,2 h) bei jüngeren Erwachsenen. Das Ausmaß der Absorption unterscheidet sich jedoch nicht zwischen den Altersgruppen, und für ältere Menschen mit normaler Leberfunktion und normaler (altersbereinigter) Nierenfunktion ist keine Dosierungsveränderung erforderlich 1 .
Serum -Assays für aktives Clindamycin erfordern einen Inhibitor, um sie zu verhindern in vitro Hydrolyse von Clindamycin -Phosphat.
Tabelle 1. Durchschnittlicher Peak- und Trogserumkonzentrationen von aktivem Clindamycin nach der Dosierung mit Clindamycin -Phosphat
| Dosierung Regimen | Gipfel McG/ml | Trog McG/ml |
| Gesunde erwachsene Männer (Nachgleichgewicht) | ||
| 10.9 | 2.0 | |
| 10.8 | 1.1 | |
| 14.1 | 1.7 | |
| 9 | ||
| Pädiatrische Patienten (erste Dosis)* | ||
| 5-7 mg/kg IV in 1 hour | 10 | |
| 5-7 mg/kg IM | 8 | |
| 3-5 mg/kg IM | 4 | |
| *Daten in dieser Gruppe von Patienten, die zur Infektion behandelt werden. |
Mikrobiologie
Wirkungsmechanismus
Clindamycin hemmt die bakterielle Proteinsynthese durch Bindung an die 23S -RNA der 50S -Untereinheit des Ribosoms. Clindamycin ist bakteriostatisch.
Die Resistenzresistenz gegen Clindamycin wird am häufigsten durch Modifikation spezifischer Grundlagen der 23S -ribosomalen RNA verursacht. Die Kreuzresistenz zwischen Clindamycin und Lincomycin ist vollständig. Da die Bindungsstellen für diese antibakteriellen Arzneimittel die Kreuzresistenz überlappen, werden manchmal bei Lincosamiden-Macroliden beobachtet, und Streptogramin B.Macrolid-induzierbares Resistenz gegen Clindamycin tritt in einigen Isolaten von makrolidresistenten Bakterien auf. Makrolidresistente Isolate von Staphylococci und Beta-Hemolytic Streptococci sollten zur Induktion der Clindamycin-Resistenz unter Verwendung des D-Zone-Tests untersucht werden.
Antimikrobielle Aktivität
Es wurde gezeigt, dass Clindamycin gegen die meisten Isolate der folgenden Mikroorganismen aktiv ist in vitro und bei klinischen Infektionen wie in der beschrieben Indikationen und Nutzung Abschnitt.
Grampositive Bakterien
Staphylococcus aureus (Methicillin-empfindliche Stämme)
Streptococcus pneumoniae (Penicillin-empfindliche Stämme)
Streptococcus pyogenes
Anaerobe Bakterien
Clostridium perfringens
Fusobacterium necrophorum
Fusobacterium nucleatum
Peptostreptococcus anaerobius
Prevotella melaninogenica
Mindestens 90% der unten aufgeführten Mikroorganismen in vitro Minimale inhibitorische Konzentrationen (MICs) unter dem anfälligen MIC-Haltepunkt von Clindamycin von Clindamycin für Organismen eines ähnlichen Typs wie in Tabelle 2 gezeigt. Die Wirksamkeit von Clindamycin bei der Behandlung klinischer Infektionen wurde jedoch aufgrund dieser Mikroorganismen nicht festgestellt.
Grampositive Bakterien
Staphylococcus epidermidis (Methicillin-empfindliche Stämme)
Streptococcus agalactiae
Streptococcus tropft
Streptococcus Mild
Oraler Streptokokkus
Anaerobe Bakterien
Actinomyces israelii
Clostridium clostridioforme
Eggerthella lenta
Finegoldia (Peptostreptococcus) groß
Micromonas (peptostreptococcus) micros
Prevotella bivia
Prevetella intermedia
Propionibacterium acnes
Anfälligkeitstestmethoden
Wenn verfügbar ist, sollte das klinische Mikrobiologie -Labor kumulativ liefern in vitro Suszeptibilitätstestergebnisse für antimikrobielle Medikamente, die in örtlichen Krankenhäusern und Praxisgebieten für den Arzt als regelmäßige Berichte verwendet werden, die das Empfindlichkeitsprofil von nosokomialen und gemeinschafts erworbenen Krankheitserregern beschreiben. Diese Berichte sollten dem Arzt bei der Auswahl eines antibakteriellen Arzneimittels zur Behandlung helfen.
Verdünnungstechniken
Quantitative Methoden werden verwendet, um antimikrobielle minimale Hemmkonzentrationen (MICs) zu bestimmen. Diese Mikrofone liefern Schätzungen der Anfälligkeit von Bakterien gegenüber antimikrobiellen Verbindungen. Die MICs sollten unter Verwendung einer standardisierten Testmethode ermittelt werden 23 (Brühe und/oder Agar). Die MIC -Werte sollten gemäß den in Tabelle 2 angegebenen Kriterien interpretiert werden.
Technische Verbreitung
Quantitative Methoden, die die Messung von Zonendurchmessern erfordern, können auch reproduzierbare Schätzungen der Anfälligkeit von Bakterien gegenüber antimikrobiellen Verbindungen liefern. Die Zonengröße sollte unter Verwendung einer standardisierten Methode bestimmt werden 25 . In diesem Verfahren werden Papierscheiben verwendet, die mit 2 MCG Clindamycin imprägniert sind, um die Anfälligkeit von Bakterien gegenüber Clindamycin zu testen. Die Scheibendiffusionsbrandbezeichnungen sind in Tabelle 2 angegeben.
Anaerobe Techniken
Für anaerobe Bakterien kann die Anfälligkeit für Clindamycin durch eine standardisierte Testmethode bestimmt werden 24 . Die erhaltenen MIC -Werte sollten gemäß den in Tabelle 2 angegebenen Kriterien interpretiert werden.
Tabelle 2. Suszeptibilitätstest -Interpretationskriterien für Clindamycin
| Erreger | Anfälligkeitsinterpretationskriterien | |||||
| Minimale Hemmkonzentrationen (Mikrofon in MCG/ml) | Festplattendiffusion (Zonendurchmesser in mm) | |||||
| S | I | R | S | I | R | |
| Staphylococcus spp. | ≤ 0,5 | 1-2 | ≥4 | ≥21 | 15–20 | ≤ 14 |
| Streptococcus pneumoniae und andere Streptococcus spp. | ≤ 0,25 | 0.5 | ≥1 | ≥19 | 16–18 | ≤ 15 |
| Anaerobe Bakterien | ≤2 | 4 | ≥8 | N / A | N / A | N / A |
| N / A=not applicable |
Ein Bericht von Anfällige (en) zeigt an, dass das antimikrobielle Arzneimittel wahrscheinlich das Wachstum des Erregers hemmt, wenn das antimikrobielle Arzneimittel die Konzentration erreicht, die normalerweise am Ort der Infektion erreichbar ist. Ein Bericht von Zwischenprodukt (i) Zeigt an, dass das Ergebnis als zweifellos angesehen werden sollte und wenn der Mikroorganismus nicht vollständig für alternative klinisch realisierbare Medikamente anfällig ist, sollte der Test wiederholt werden. Diese Kategorie impliziert eine mögliche klinische Anwendbarkeit an Körperstellen, an denen das Arzneimittel physiologisch konzentriert ist oder in Situationen, in denen eine hohe Dosierung des Arzneimittels angewendet werden kann. Diese Kategorie bietet auch eine Pufferzone, die verhindert, dass kleine, unkontrollierte technische Faktoren wichtige Diskrepanzen in der Interpretation verursachen. Ein Bericht von Resistent (r) zeigt an, dass das antimikrobielle Arzneimittel wahrscheinlich nicht das Wachstum des Erregers hemmt, wenn das antimikrobielle Arzneimittel die Konzentration erreicht, die normalerweise an der Infektionsstelle erreichbar ist. Eine andere Therapie sollte ausgewählt werden.
Qualitätskontrolle
Standardisierte Anfälligkeitstestverfahren erfordern die Verwendung von Laborkontrollen, um die Genauigkeit und Präzision der im Assay verwendeten Vorräte und Reagenzien zu überwachen und sicherzustellen 2345 . Standard -Clindamycin -Pulver sollte die MIC -Bereiche in Tabelle 3 liefern. Für die Festplattendiffusionstechnik unter Verwendung der 2 MCG Clindamycin -Scheibe sollten die in Tabelle 2 angegebenen Kriterien erreicht werden.
Tabelle 3. Akzeptable Qualitätskontrollbereiche für Clindamycin
| QC -Stamm | Akzeptable Qualitätskontrollbereiche | |
| Minimaler Hemmkonzentrationsbereich (MCG/ml) | Festplattendiffusion Range (Zonendurchmesser in mm) | |
| Enterococcus faecalis 1 ATCC 29212 | 4-16 | N / A |
| Staphylococcus aureus ATCC 29213 | 06-0.25 | N / A |
| Staphylococcus aureus ATCC 25923 | N / A | 24-30 |
| Streptococcus pneumoniae ATCC 49619 | 0,03-0.12 | 19-25 |
| Bacteroides fragilis ATCC 25285 | 0,5-2 | N / A |
| Bacteroides Thetaiotaomicron ATCC 29741 | 2-8 | N / A |
| Clostridium difficile 2 ATCC 700057 | 2-8 | N / A |
| Eggerthella lenta ATCC 43055 | 06-0.25 | N / A |
| 1. Enterococcus faecalis wurde in dieser Tabelle nur für Qualitätskontrollzwecke aufgenommen. 2. Qualitätskontrolle für C. schwierig wird unter Verwendung der Agarverdünnungsmethode durchgeführt. Nur alle anderen obligierten Anaerobes können entweder durch Brülhikrodilution oder Agarverdünnungsmethoden getestet werden. N / A=Not applicable ATCC ® ist ein eingetragenes Markenzeichen der amerikanischen Typkultursammlung |
Referenzen
1. Smith RB Phillips JP: Bewertung von Cleocin HCL und Cleocin -Phosphat in einer gealterten Bevölkerung. Upjohn TR 8147-82-9122-021 Dezember 1982.
2. Clsi. Leistungsstandards für antimikrobielle Suszeptibilitätstests: 26 th ed. CLSI -Ergänzung M100S. Wayne PA: Institut für klinisches und Laborstandards; 2016.
3. CLSI. Methoden zur Verdünnung antimikrobieller Suszeptibilitätstests für Bakterien, die aerob wachsen; Zugelassener Standard -Tenth Edition. CLSI-Dokument M07-A10. Wayne PA: Institut für klinisches und Laborstandards; 2015.
4. Clsi. Methoden für antimikrobielle Suszeptibilitätstests anaerobe Bakterien; Genehmigte Standard-Achtelausgabe. CLSI-Dokument M11-A8. Wayne PA: Institut für klinisches und Laborstandards; 2012.
5. Clsi. Leistungsstandards für antimikrobielle Festplattenanfälligkeitstests; Genehmigte Standard -Twelfth Edition. CLSI-Dokument M02-A12. Wayne PA: Institut für klinisches und Laborstandards; 2015.
Patienteninformationen für Cleocin I.V.
Die Patienten sollten beraten werden, dass antibakterielle Medikamente einschließlich Cleocin -Phosphat nur zur Behandlung von bakteriellen Infektionen eingesetzt werden sollten. Sie behandeln keine Virusinfektionen (z. B. die Erkältung). Wenn Cleocin -Phosphat zur Behandlung einer bakteriellen Infektion verschrieben wird, sollte Patienten gesagt werden, dass es zwar üblich ist, sich früh im Verlauf der Therapie besser zu fühlen, die Medikamente sollten genau wie angewiesen eingenommen werden. Das Überspringen von Dosen oder Nichtabschließung des gesamten Therapieverlaufs kann (1) die Wirksamkeit der sofortigen Behandlung verringern und (2) die Wahrscheinlichkeit erhöhen, dass Bakterien Resistenz entwickeln und in Zukunft nicht durch Cleocin -Phosphat oder andere antibakterielle Arzneimittel behandelt werden können.
Durchfall ist ein häufiges Problem, das durch Antibiotika verursacht wird, das normalerweise endet, wenn das Antibiotikum abgesetzt wird. Manchmal können Patienten nach Beginn der Behandlung mit Antibiotika wässrige und blutige Stühle (mit oder ohne Magenkrämpfe und Fieber) entwickeln, auch bis nach zwei oder mehr Monaten nach der letzten Dosis des Antibiotikums. Wenn dies auftritt, sollten Patienten so bald wie möglich ihren Arzt kontaktieren.
Anweisungen für die Verwendung für Add-Vantage-System. Für IV. Verwenden Sie nur die Verwendung
Cleocin -Phosphat ®
Clindamycin Sterile Lösung für die Injektion USP
in Add-Vorture ® Phiole
Verdünnungsbehälter öffnen:
Schälen Sie das Überziehen aus der Ecke und entfernen Sie den Behälter. Eine gewisse Opazität des Kunststoffs aufgrund der Feuchtigkeitsabsorption während des Sterilisationsprozesses kann beobachtet werden. Dies ist normal und wirkt sich nicht auf die Qualität oder Sicherheit der Lösungen aus. Die Deckkraft wird allmählich abnehmen.
Kannst du allergisch gegen Kalium sein?
So zusammenstellen Fläschchen und flexibler Verdünnungsbehälter:
(Verwenden Sie eine aseptische Technik)
- Entfernen Sie die Schutzabdeckungen von der Oberseite des Fläschchens und dem Fläschchenanschluss am Verdünnungsbehälter wie folgt:
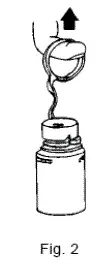
- Um die Ausreißerlauchleiterkappe zu entfernen, schwingen Sie den Pull -Ring über die Oberseite des Fläschchens und ziehen Sie weit nach unten, um die Öffnung zu starten (siehe Abbildung 1). Ziehen Sie dann gerade nach oben, um die Kappe zu entfernen. (Siehe Abbildung 2.) NOTIZ: Sobald die Breakaway -Kappe entfernt wurde Greifen Sie nicht mit Spritze auf Fläschchen zu.
- Um die Fläschchenanschlussabdeckung zu entfernen, fassen Sie die Lasche am Pull Ring nach oben, um die drei Krawattenketten zu brechen, und ziehen Sie sie zurück, um die Abdeckung zu entfernen. (Siehe Abbildung 3.)

- Schrauben Sie die Fläschchen in den Fläschchenanschluss, bis er nicht weiter geht. Die Fläschchen muss fest eingeschraubt werden, um eine Dichtung zu versichern. Dies tritt nach dem ersten hörbaren Klick ungefähr 1/2 Turn (180 °) auf. (Siehe Abbildung 4.) Der Klick -Sound versichert kein Siegel. Die Fläschchen muss so weit gedreht werden, wie es gehen wird. NOTIZ: Sobald die Fläschchen sitzen, versuchen Sie nicht, sie zu entfernen. (Siehe Abbildung 4.)
- Überprüfen Sie die Fläschchen erneut, um sicherzustellen, dass es eng ist, indem Sie versuchen, es weiter in Richtung der Montage zu drehen.
- Beschriftung angemessen.
 |
 |
Beim Vorbereiten von Beimischung:
- Drücken Sie den Boden des Verdünnungsbehälters vorsichtig zusammen, um den Teil des Behälters, der das Ende des Drogenfläschchens umgibt, aufzublasen.
- Drücken Sie die Medikamente mit der anderen Hand in den Behälter, um die Wände des Behälters zu teleskopieren. Fassen Sie die innere Kappe des Fläschchens durch die Wände des Behälters. (Siehe Abbildung 5.)
- Ziehen Sie die innere Kappe aus dem Drogenfläschchen. (Siehe Abbildung 6.) Vergewissern Sie sich, dass der Gummi -Stopper herausgezogen wurde, sodass das Medikament und das Verdünnungsmittel vermischen können.
- Behälterinhalt gründlich mischen und innerhalb der angegebenen Zeit verwenden.
 |
 |
Vorbereitung für die Verwaltung: (Verwenden Sie eine aseptische Technik)
- Bestätigen Sie die Aktivierung und Beimischung des Fläschcheninhalts.
- Überprüfen Sie auf Lecks, indem Sie den Container fest drücken. Wenn Lecks als Sterilität abgeworfen werden, kann die Sterilität beeinträchtigt werden.
- Schließung der Strömungsregelung des Verabreichungssatzes.
- Entfernen Sie die Abdeckung vom Auslassanschluss am Boden des Behälters.
- Setzen Sie den Piercing Pin der Verwaltungsstift mit einer Verdrehungsbewegung in den Port ein, bis der Stift fest sitzt. HINWEIS: Siehe vollständige Anweisungen auf dem Karton mit Administrationsset.
- Heben Sie das freie Ende der Kleiderliste auf dem Boden des Fläschchens an, das die beiden Krawattenketten brechen. Beugen Sie die Schleife nach außen, um ihn in die aufrechte Position zu sperren und den Behälter vom Kleiderbügel auszusetzen.
- Drücken Sie die Tropfkammer zusammen und lassen Sie sie frei, um den ordnungsgemäßen Flüssigkeitsspiegel in der Kammer festzulegen.
- Offene Flussregelklemme und löschen Sie die Luft vom Set. Schließklemme.
- Anbringen an das Venenpunktionsgerät. Wenn das Gerät nicht in der Primem in der Pause eingebaut ist, und die Venenpunktion herstellen.
- Regulieren Sie die Verabreichungsrate mit Durchflussregelungsklemme.
WARNUNG: Do not use flexible container in series connections.


