Die Informationen Auf Dieser Website Stellen Keine Medizinische Beratung Dar. Wir Verkaufen Nichts. Die Richtigkeit Der Übersetzung Wird Nicht Garantiert. Haftungsausschluss
Ergot -DerivateWahrheit
Drogenzusammenfassung
Was ist Trudhesa?
Trudhesa (Dihydroergotamin -Mesylat) Nasalspray ist ein Ergotamin -Derivat zur Behandlung von Migräne mit oder ohne Aura bei Erwachsenen.
Was sind Nebenwirkungen von Trudhesa?
Wahrheit
- Nesselsucht
- Schwierigkeiten beim Atmen
- Schwellung Ihrer Gesichtslippen Zunge oder Hals
- langsamer oder schneller Herzschlag
- Schwäche in den Beinen
- Muskelschmerzen in den Armen oder Beinen
- Kribbeln oder Taubheit
- Kälte in den Händen und Füßen
- blaue Finger und Zehen
- Starke Magenschmerzen
- Kiefer oder Schmerz des linken Arms
- Brustschmerzen oder Druck
- plötzliche Müdigkeit
- Schwäche auf einer Seite des Körpers
- Probleme beim Sprechen
- Sehveränderungen
- geistige oder Stimmungsänderungen
- Verwirrung
- Ausschlag
- Juckreiz und
- schwerer Schwindel
Holen Sie sich sofort medizinische Hilfe, wenn Sie eines der oben aufgeführten Symptome haben.
Nebenwirkungen von Trudhesa umfassen:
- laufende Nase
- Brechreiz
- geändert Sinn des Geschmacks
- Reaktionen für Anwendungsstellen
- Schwindel
- Erbrechen
- Schläfrigkeit
- Halsschmerzen Und
- Durchfall.
Suchen Sie medizinische Versorgung oder rufen Sie auf einmal 911 an, wenn Sie die folgenden schwerwiegenden Nebenwirkungen haben:
- Schwerwiegende Augensymptome wie plötzlicher Sehverlust verschwommenes Sehen Tunnel Sehschmerzen oder Schwellungen oder Halos in der Umgebung des Lichts;
- Schwerwiegende Herzsymptome wie schnelle unregelmäßige oder pochende Herzschläge; Flattern in deiner Brust; Kurzatmigkeit; und plötzlich Schwindel Benommenheit oder ohnmächtig;
- Starke Kopfschmerzen Verwirrung verwirrt Spracharm oder Bein Schwäche Schwierigkeiten beim Verlust der Koordination unstabil sehr steifes Muskeln hoher Fieber problemlos Schwitzen oder Zittern.
Dieses Dokument enthält nicht alle möglichen Nebenwirkungen und andere können auftreten. Wenden Sie sich an Ihren Arzt nach zusätzlichen Informationen zu Nebenwirkungen.
Dosierung für Trudhesa
Die empfohlene Dosis von Trudhesa -Nasenspray beträgt 1,45 mg (verabreicht als ein Messspray von 0,725 mg in jedes Nasenloch). Die Dosis kann bei Bedarf mindestens 1 Stunde nach der ersten Dosis wiederholt werden.
Trudhesa bei Kindern
Sicherheit und Wirksamkeit von Trudhesa -Nasenspray ist bei pädiatrischen Patienten nicht festgelegt.
Welche Drogensubstanzen oder Nahrungsergänzungsmittel interagieren mit Trudhesa?
Trudhesa Nasenspray kann mit anderen Medikamenten interagieren, wie z. B.:
- Beta-Blocker
- Nikotin
- Selektiver Serotonin -Wiederaufnahmehemmer ( Wenn ) Antidepressiva (z. B. Fluoxetin -Fluvoxamin -Paroxetin -Sertralin)
- Protease -Inhibitoren (z. B. Ritonavir Nelfinavir Indinavir)
- Makrolid Antibiotika (z. Erythromycin Clarithromycin)
- Antimykotika (z. B. Ketoconazol Itraconazol)
- Triptans und
- Vasokonstriktoren.
Sagen Sie Ihrem Arzt alle Medikamente und Nahrungsergänzungsmittel, die Sie verwenden.
Trudhesa während der Schwangerschaft und des Stillens
Sagen Sie Ihrem Arzt, wenn Sie schwanger sind oder planen, schwanger zu werden, bevor Sie Trudhesa Nasal Spray verwenden. Dies kann das Risiko einer Frühgeburt erhöhen und einen Fötus schädigen. Es ist nicht bekannt, ob Trudhesa -Nasenspray in die Muttermilch übergeht. Ergotamin ist jedoch in der Muttermilch ein verwandtes Medikament vorhanden. Aufgrund des Potenzials für verringerte Milchversorgung und schwerwiegende unerwünschte Ereignisse im gestillten Kind, einschließlich Durchfall, erbricht schwacher Impuls und ein instabiles Blutdruckstillung, wird während der Behandlung mit Trudhesa -Nasenspray und 3 Tage nach der letzten Dosis nicht empfohlen. Die Muttermilchversorgung in dieser Zeit sollte gepumpt und weggeworfen werden.
Weitere Informationen
Unsere Trudhesa (Dihydroergotamin -Mesylat) Nasenspray -Nebenwirkungen Arzneimittelzentrum bietet eine umfassende Übersicht über verfügbare Arzneimittelinformationen über die potenziellen Nebenwirkungen bei der Einnahme dieses Medikaments.
Dies ist keine vollständige Liste von Nebenwirkungen, und andere können auftreten. Rufen Sie Ihren Arzt an, um medizinische Beratung zu Nebenwirkungen zu erhalten. Sie können die FDA bei 1-800-FDA-1088 Nebenwirkungen melden.
FDA -Drogeninformationen
- Drogenbeschreibung
- Indikationen
- Nebenwirkungen
- Wechselwirkungen mit Arzneimitteln
- Warnungen
- Überdosis
- Kontraindikationen
- Klinische Pharmakologie
- Medikamentenhandbuch
WARNUNG
Periphere Ischämie nach gleichzeitiger Verabreichung mit starken CYP3A4 -Inhibitoren
Eine schwerwiegende und/oder lebensbedrohliche periphere Ischämie wurde mit der gleichzeitigen Verabreichung von Dihydroergotamin mit starken CYP3A4-Inhibitoren in Verbindung gebracht. Da die CYP3A4 -Hemmung die Serumspiegel von Dihydroergotamin erhöht, wird das Risiko für Vasospasmus, die zu einer Gehirnsämie führen, und/oder Ischämie der Extremitäten, die erhöht wird. Daher ist die gleichzeitige Verwendung von Trudhesa mit starken CYP3A4 -Inhibitoren kontraindiziert [siehe Kontraindikationen WARNUNGS AND PRECAUTIONS Und Wechselwirkungen mit Arzneimitteln ].
Beschreibung für Trudhesa
Trudhesa (Dihydroergotamin-Mesylat) Nasalspray ist ein Produkt mit einem eindosierten Arzneimittel-Gerätskombinationsprodukt, das ein Dihydroergotamin-Mesylat-Arzneimittelbestandteil und ein Bestandteil der Nasenspray-Gerät enthält.
Der chemische Name für Dihydroergotamin-Mesylat ist Ergotaman-3 '6' 18-Trione 910-Dihydro-12'-Hydroxy-2'-Methyl-5'- (Phenylmethyl)-(5'A)-Monomethanesulfonat. Sein Molekulargewicht beträgt 679,78 und seine molekulare Formel ist c 33 H 37 N 5 O 5 • Ch 4 O 3 S.
Die chemische Struktur ist:
 |
Das Arzneimittelbestandteil ist eine Dihydroergotamin -Mesylatlösung. Jeder Milliliter (Ml) der Lösung enthält Dihydroergotamin -Mesylat 4,0 mg (äquivalent zu 3,43 mg Dihydroergotamin) und die folgenden inaktiven Inhaltsstoffe: Koffein (NULL,0 mg) Kohlendioxid (q.s.) Dextrose (NULL,0 mg) und Wasser (Q. bis 1,0 ml).
Trudhesa -Nasenspray nach dem Zusammenbau und der Grundierung liefert 0,725 mg Dihydroergotamin -Mesylat pro Spray. Eine Gesamtdosis von 1,45 mg Dihydroergotamin -Mesylat wird in 2 Sprays geliefert. Das Nasenspray-Gerät enthält Hydrofluoralkane-134A (HFA) -Treibstoff.
Verwendung für Trudhesa
Trudhesa ist für die akute Behandlung von Migräne mit oder ohne Aura bei Erwachsenen angezeigt.
Einschränkungen der Nutzung
Trudhesa ist nicht für die vorbeugende Behandlung von Migräne angezeigt.
Trudhesa ist nicht für die Behandlung von hemiplegischer oder basilarischer Migräne angegeben.
Dosierung für Trudhesa
Dosierungsinformationen
Die empfohlene Dosis Trudhesa beträgt 1,45 mg als zwei Messsprays in die Nase (ein Spray von 0,725 mg in jedes Nasenloch).
Die Dosis kann bei Bedarf mindestens 1 Stunde nach der ersten Dosis wiederholt werden. Verwenden Sie nicht mehr als 2 Dosen Trudhesa innerhalb eines Zeitraums von 24 Stunden oder drei Dosen innerhalb eines Zeitraums von 7 Tagen.
Bewertung vor der ersten Dosis
Vor Beginn von Trudhesa wird eine kardiovaskuläre Bewertung empfohlen [siehe WARNUNGS AND PRECAUTIONS ]. For patients with risk factors predictive of coronary artery disease who are determined to have a satisfactory cardiovascular evaluation it is strongly recommended that administration of the first dose of TRUDHESA take place in the setting of an equipped healthcare facility.
Wichtige Verwaltungsanweisungen
Trudhesa ist nur für die Nasenverwaltung und darf nicht injiziert werden.
Trudhesa muss vor der Verwendung montiert werden (siehe Anweisungen zur Verwendung ). Nutzen oder verwerfen Sie Trudhesa innerhalb von 8 Stunden, sobald die Fläschchen geöffnet oder das Produkt zusammengestellt wurde.
Führen Sie die zusammengesetzte Trudhesa vor der ersten Verwendung durch die Veröffentlichung von 4 Sprays vor. Verwenden Sie Trudhesa unmittelbar nach dem Priming. Trockhesa unmittelbar nach dem Gebrauch verwerfen. Öffnen Sie und bereiten Sie eine neue Trudhesa vor, wenn eine zusätzliche Dosis erforderlich ist.
Wie geliefert
Dosierungsformen und Stärken
Trudhesa (Dihydroergotamin-Mesylat) Nasalspray ist ein Produkt mit einem eindosierten Arzneimittel-Gerät, das eine Fläschchen von Dihydroergotamin-Mesylat mit einer klaren und farblosen bis schwachen gelben Lösung und einer intranasalen Abgabegerät enthält. Jedes Spray liefert 0,725 mg Dihydroergotamin -Mesylat.
Trudhesa (Dihydroergotamin -Mesylat) Nasenspray (NULL,725 mg pro Spray) wird als Paket von 4 Einzeldosierungseinheiten geliefert ( NDC 77530-725-04). Jede eindosierte Einheit enthält:
- Ein bernsteinfarbenes Glasfläschchen ( NDC 77530-725-01) mit 4 mg Dihydroergotamin-Mesylat in einer 1 ml klaren und farblosen bis leicht gelben Lösung. Der Stopper wird nicht mit Naturkautschuk -Latex hergestellt.
- Ein Nasenspray -Gerät.
Lagerung und Handhabung
Lagern Sie Trudhesa bei kontrollierter Raumtemperatur von 20 ° C bis 25 ° C (68 ° F bis 77 ° F), wobei Exkursionen zwischen 15 ° C und 30 ° C (59 ° F bis 86 ° F) zulässig sind. Nicht kühlen oder einfrieren.
Hergestellt von: Mipharm S.P.A. Milano Italy. Überarbeitet: September 2021
Nebenwirkungen for Trudhesa
Die folgenden klinisch signifikanten Nebenwirkungen werden an anderer Stelle in der Markierung beschrieben:
- Periphere Ischämie nach gleichzeitiger Verabreichung mit starken CYP3A4 -Inhibitoren [siehe Boxwarnung Und WARNUNGS AND PRECAUTIONS ]
- Myokardischämie und/oder Infarkt anderer nachteiliger Herzereignisse und Todesfälle [siehe WARNUNGS AND PRECAUTIONS ]
- Zerebrovaskuläre Nebenwirkungen und Todesfälle [siehe WARNUNGS AND PRECAUTIONS ]
- Andere vasospasmus verwandte Nebenwirkungen [siehe WARNUNGS AND PRECAUTIONS ]
- Erhöhung des Blutdrucks [siehe WARNUNGS AND PRECAUTIONS ]
- Medikamente Überbeanspruchte Kopfschmerzen [siehe WARNUNGS AND PRECAUTIONS ]
- Frühgeborene [siehe WARNUNGS AND PRECAUTIONS ]
- Fibrotische Komplikationen [siehe WARNUNGS AND PRECAUTIONS ]
- Lokale Reizung [siehe WARNUNGS AND PRECAUTIONS ]
Klinische Studien Erfahrung
Da klinische Studien unter stark unterschiedlichen Bedingungen durchgeführt werden, die in den klinischen Studien eines Arzneimittels beobachtet werden, können in den klinischen Studien eines anderen Arzneimittels nicht direkt mit den Raten verglichen werden und spiegeln möglicherweise nicht die in der Praxis beobachteten Raten wider.
Nebenwirkungen in Placebo-kontrollierten Versuchen mit Dihydroergotamin (DHE) -Mesylat-Nasenspray [siehe Klinische Studien ]
Von den 1796 Patienten und Probanden, die mit Nasenspray -Dosen 2 mg oder weniger in US -amerikanischen und ausländischen klinischen Studien behandelt wurden, wurden 26 (NULL,4%) aufgrund unerwünschter Ereignisse abgebrochen. Die mit dem Absetzen verbundenen unerwünschten Ereignisse waren in einer abnehmenden Häufigkeitsreihenfolge: Rhinitis (13) Schwindel (2) Gesichtsödem (2) und jeweils ein Patient aufgrund eines kalten Schweißes versehentlicher Trauma -Depression elektiver Chirurgie Sämstrom -Allergie -Erbrechen Hypotonie und Paraästhesie.
Wie viel Trazodon ist zu viel
Tabelle 1 fasst die Inzidenzraten von unerwünschten Reaktionen zusammen, die von mindestens 1% der Patienten, die das Nasenspray für die Behandlung von Migräne erhalten haben, während placebokontrollierter doppelblindklinischer Studien und häufiger als bei Patienten, die Placebo erhielten. Die am häufigsten berichteten unerwünschten Reaktionen (mehr als 1% der Patienten, die das Nasenspray erhielten) waren Rhinitis -Übelkeit verändert veränderter Geschmackssinnsanwendungsstelle Reaktionen Schwindelerregung Erbrechen etwas Pharyngitis und Durchfall. In den meisten Fällen waren diese Ereignisse vorübergehend und selbstlimitiert und führten nicht zum Absetzen einer Patienten von einer Studie.
Tabelle 1 Nebenwirkungen von mindestens 1% der von DHE Nasenspray behandelten Patienten und traten häufiger auf als in der Placebogroup in den Migräne-Placebokontrollierten Studien
| Und Nasenspray N = 597 % | Placebo N = 631 % | |
| Atmungssystem | ||
| Rhinitis | 26 | 7 |
| Pharyngitis | 3 | 1 |
| Magen -Darm -System | ||
| Nausea | 10 | 4 |
| Vomiting | 4 | 1 |
| Diarrhea | 2 | <1 |
| Besondere Sinne andere | ||
| Altered Sense of Taste | 8 | 1 |
| Anwendungsseite | ||
| Anwendungsseite Reaction | 6 | 2 |
| Zentrales und peripheres Nervensystem | ||
| Dizziness | 4 | 2 |
| Somnolence | 3 | 2 |
| Körper als ganzer allgemeiner Körper | ||
| Hot Flashes | 1 | <1 |
| Asthenia | 1 | 0 |
| Muskuloskelettsystem | ||
| Stiffness | 1 | <1 |
Nebenwirkungen in Studien mit Trudhesa
Eine Open-Label-Studie an Erwachsenen (18 bis 66 Jahre) wurde durchgeführt, um die Sicherheit und Verträglichkeit von Trudhesa-wiederholten Verwendung von Trudhesa zu bewerten, wurde im Verlauf von 6 bis 12 Monaten zulässig. Insgesamt 354 Patienten mit Migräne erhielten mindestens eine Dosis Trudhesa. Einhundertfünfundachtzig Patienten behandelten 6 Monate lang durchschnittlich mindestens zwei Migräne pro Monat und 55 Patienten, die durchschnittlich mindestens zwei Migräne pro Monat für 12 Monate behandelt wurden. Von den Patienten, die mindestens eine Dosis Trudhesa 185 (NULL,3%) erhielten, hatten Patienten lokale irritative Symptome. Von diesen waren die häufigsten lokalen irritativen Symptome nasopharyngitis rhinitis nasales Beschwerdenprodukt Geschmack abnormal WARNUNGS AND PRECAUTIONS ].
Nachmarkterfahrung
Die folgenden nachteiligen Reaktionen wurden während der Verwendung von Dihydroergotamin -Mesylat nach der Annahme identifiziert. Da diese Reaktionen freiwillig aus einer Population unsicherer Größe berichtet werden, ist es nicht immer möglich, ihre Häufigkeit zuverlässig abzuschätzen oder ein kausales Verhältnis zur Arzneimittelexposition herzustellen:
Vasospasmus Parästhesie Hypertonie Schwindel Angst Dyspnoe Kopfschmerz spülen Durchfallausschlag Erhöhtes Schwitzen und Pleura- und Retroperitonealfibrose nach langfristiger Verwendung von Dihydroergotamin. Es wurden Fälle von Myokardinfarkt und Schlaganfall nach Verwendung von Dihydroergotamin -Mesylat berichtet [siehe WARNUNGS AND PRECAUTIONS ].
Wechselwirkungen mit Arzneimitteln for Trudhesa
CYP3A4 -Inhibitoren
Es gab seltene Berichte über schwerwiegende unerwünschte Ereignisse im Zusammenhang mit der gleichzeitigen Verabreichung der intravenösen Verabreichung von Dihydroergotamin und starken CYP3A4 -Inhibitoren wie Protease -Inhibitoren (z. Itraconazol), was zu Vasospasmus führte, die zu einer zerebralen Ischämie und/oder zu einer Ischämie der Extremitäten führten [siehe WARNUNGS AND PRECAUTIONS ]. The use of strong CYP3A4 Inhibitoren with dihydroergotamine is contraindicated [see Kontraindikationen ]. Administer moderate CYP3A4 Inhibitoren (e.g. saquinavir Nefazodon Fluconazol grapefruit juice fluoxetine fluvoxamine zileuton clotrimazole) with caution.
Triptanen
Triptanen (serotonin [5-HT] 1B/1D receptor agonists) have been reported to cause coronary artery vasospasm Und its effect could be additive with TRUDHESA. Therefore Triptans und TRUDHESA should not be taken within 24 Stunden of each other [see Kontraindikationen ].
Beta -Blocker
Es gab Berichte, dass Propranolol die vasokonstriktive Wirkung von Ergotamin durch Blockieren der vasodilatierenden Eigenschaft von Adrenalin potenzieren kann.
Vasokonstriktoren
Trudhesa ist für die Verwendung mit peripheren und zentralen Vasokonstriktoren kontraindiziert, da die Kombination eine synergistische Erhöhung des Blutdrucks verursachen kann [siehe WARNUNGS AND PRECAUTIONS ].
Nikotin
Nikotin may provoke vasoconstriction in some patients predisposing to a greater ischemic response to ergot therapy [see WARNUNGS AND PRECAUTIONS ].
Selektive Serotonin -Wiederaufnahmehemmer
Schwäche Hyperreflexie und Inkoordination wurden selten bei 5-HT berichtet 1 Agonisten wurden mit selektiven Serotonin -Wiederaufnahmehemmer (z. B. Fluoxetin -Fluvoxamin -Paroxetin -Sertralin) koadministeriert.
Drogenmissbrauch und Abhängigkeit
Kontrollierte Substanz
Trudhesa enthält Dihydroergotamin (als Mesylatsalz), das keine kontrollierte Substanz ist.
Missbrauch
Missbrauch is the intentional non-therapeutic use of a drug even once for its desirable psychological or physiological effects. Currently available data have not demonstrated drug abuse with dihydroergotamine. However cases of drug abuse in patients on other forms of ergot therapy have been reported.
Abhängigkeit
Die physische Abhängigkeit ist ein Zustand, der sich durch physiologische Anpassung als Reaktion auf wiederholten Drogenkonsum entwickelt, die sich nach abrupten Absetzen oder einer signifikanten Dosisreduktion eines Arzneimittels durch Entzugszeichen und Symptome manifestieren. Derzeit verfügbare Daten haben keine physische oder psychische Abhängigkeit von Dihydroergotamin gezeigt. Es wurden jedoch Fälle von psychologischer Abhängigkeit bei Patienten von anderen Formen der Ergot -Therapie berichtet.
Warnungen für Trudhesa
Eingeschlossen als Teil der 'VORSICHTSMASSNAHMEN' Abschnitt
Vorsichtsmaßnahmen für Trudhesa
Periphere Ischämie nach gleichzeitiger Verabreichung mit starken CYP3A4 -Inhibitoren
Eine schwerwiegende und/oder lebensbedrohliche periphere Ischämie wurde mit der gleichzeitigen Verabreichung von Dihydroergotamin mit starken CYP3A4-Inhibitoren in Verbindung mit Protease-Inhibitoren Makrolid-Antibiotika und Antimykotika in Verbindung gebracht. Da die CYP3A4 -Hemmung die Serumspiegel von Dihydroergotamin erhöht, wird das Risiko für Vasospasmus, die zu einer Gehirnsämie führen, und/oder Ischämie der Extremitäten, die erhöht wird. Daher ist die gleichzeitige Verwendung von Trudhesa mit starken CYP3A4 -Inhibitoren kontraindiziert [siehe Kontraindikationen Und Wechselwirkungen mit Arzneimitteln ].
Myokardischämie und/oder Infarkt anderer kardiischer Nebenwirkungen und Todesfälle
Das Potenzial für unerwünschte kardiale Nebenwirkungen besteht bei der Trudhesa -Behandlung. Nach Verwendung von Dihydroergotamin -Mesylat sind schwerwiegende unerwünschte Herzereignisse, einschließlich einiger tödlich, aufgetreten. Zu diesen Ereignissen gehörten akute Myokardinfarkte -lebenslange Störungen von Herzrhythmus (z. B. vasospasmus vasospasmus der ventrikulären Fibrillation ventrikulärer Fibrillation) und vorübergehende Myokardischämie.
Vor Beginn von Trudhesa wird eine kardiovaskuläre Bewertung empfohlen, um festzustellen, ob der Patient frei von Koronararterien und ischämischen Myokarderkrankungen oder einer anderen signifikanten zugrunde liegenden Herz -Kreislauf -Erkrankung ist. Wenn während der kardiovaskulären Beurteilung die Anamnese des Patienten (einschließlich Risikofaktoren) oder die Ergebnisse der elektrokardiographischen Untersuchung mit dem Vasospasmus der Koronararterie oder der Myokardischämie Trudhesa nicht übereinstimmen sollte [siehe Kontraindikationen ].
Bei Patienten mit Risikofaktoren, die eine Erkrankung der Koronararterien vorhersagen (z. Die Einstellung einer ausgestatteten Gesundheitseinrichtung, es sei denn, der Patient hat zuvor Dihydroergotamin -Mesylat erhalten. Während des Intervalls unmittelbar nach der ersten Verwendung von Trudhesa wird ein Elektrokardiogramm bei Patienten mit Risikofaktoren empfohlen, da Ischämie ohne klinische Symptome auftreten kann.
Zerebrovaskuläre Nebenwirkungen und Todesfälle
Das Potenzial für unerwünschte zerebrovaskuläre Nebenwirkungen besteht bei der Trudhesa -Behandlung. Bei Patienten, die mit Dihydroergotamin -Mesylat behandelt wurden, wurden zerebrale Blutungen und andere zerebrovaskuläre Ereignisse berichtet. und einige haben zu Todesfällen geführt. In mehreren Fällen scheint es möglich, dass die zerebrovaskulären Ereignisse primär waren. Das Dihydroergotamin -Mesylat wurde in der falschen Überzeugung verabreicht, dass die auftretenden Symptome eine Folge von Migräne waren, wenn dies nicht der Fall war. Es ist zu beachten, dass Patienten mit Migräne möglicherweise ein erhöhtes Risiko für bestimmte zerebrovaskuläre Ereignisse ausgesetzt sind (z. Trudhesa absetzen, wenn ein zerebrovaskuläres Ereignis vermutet wird.
Andere vasospasmus verwandte Nebenwirkungen
Trudhesa wie andere Ergot -Alkaloide können andere vasospastische Reaktionen als das Vasospasmus der Koronararterie verursachen. Mit Dihydroergotamin -Mesylat wurde mit Dihydroergotamin -Mesylat myokardiale periphere Gefäß- und Kolonischämie berichtet.
Dihydroergotamin -Mesylat -assoziierte vasospastische Phänomene können auch Muskelschmerzen verursachen Taubheitskältepallor und Zyanose der Ziffern. Bei Patienten mit beeinträchtigtem Kreislauf kann anhaltend Vasospasmus zu einem Gangrän oder Tod führen. Trudhesa sollte sofort abgesetzt werden, wenn Anzeichen oder Symptome der Vasokonstriktion auftreten.
Patienten, bei denen andere Symptome oder Anzeichen auf dem verminderten arteriellen Fluss wie dem ischämischen Darmsyndrom oder dem Raynaud-Syndrom nach Verwendung eines 5-HT-Agonisten einschließlich Trudhesa deuten, sollten von einem Gesundheitsdienstleister bewertet werden.
Blutdruckerhöhung
In seltenen Fällen wurde bei Patienten mit und ohne mit Dihydroergotamin -Mesylat behandelte Hypertonie eine signifikante Erhöhung des Blutdrucks berichtet. Trudhesa ist bei Patienten mit unkontrollierter Hypertonie kontraindiziert [siehe Kontraindikationen ].
Nach der Dosierung mit weiteren 5-ht wurde ein Anstieg des mittleren Lungenarteriendrucks um 18% beobachtet 1 Agonist in einer Studie zur Bewertung von Probanden, die sich einer Herzkatheterisierung unterziehen.
Medikamente Überbeanspruchung Kopfschmerzen
Überbeanspruchte von akuten Migränemedikamenten (z. B. Ergotaminer -Triptans -Opioide oder eine Kombination dieser Medikamente für 10 oder mehr Tage pro Monat) kann zu einer Verschärfung von Kopfschmerzen führen (d. H. Überbeanspruchte Kopfschmerzen mit Medikamenten übergebracht). Überbeanspruchte Kopfschmerzen in Medikamenten können als migräneähnliche tägliche Kopfschmerzen oder als deutliche Zunahme der Häufigkeit von Migräneangriffen vorhanden. Die Entgiftung von Patienten einschließlich des Entzugs der überbeanspruchten Arzneimittel und die Behandlung von Entzugssymptomen (zu denen häufig eine vorübergehende Verschlechterung von Kopfschmerzen gehört) kann erforderlich sein.
Frühgeborene
Basierend auf dem Wirkungsmechanismus von Dihydroergotamin und die Ergebnisse der veröffentlichten Literatur können trudhesa vorzeitige Arbeit verursachen. Vermeiden Sie die Verwendung von Trudhesa während der Schwangerschaft [siehe Verwendung in bestimmten Populationen ]
Fibrotische Komplikationen
Das Potenzial für fibrotische Komplikationen besteht bei der Trudhesa -Behandlung. Es gab Berichte über Pleura- und Retroperitonealfibrose bei Patienten nach längerem täglichem Einsatz von Dihydroergotamin -Mesylat. Selten verlängerte tägliche Verwendung anderer Ergot -Alkaloid -Medikamente wurde mit einer Herzklappenfibrose in Verbindung gebracht. Seltene Fälle wurden auch in Verbindung mit der Verwendung von Dihydroergotamin -Mesylat berichtet. In diesen Fällen erhielten Patienten jedoch auch Medikamente, von denen bekannt ist, dass sie mit einer Herzklappenfibrose assoziiert waren.
Die Verabreichung von Trudhesa sollte die Dosierungsrichtlinien nicht überschreiten und nicht für die chronische tägliche Verabreichung verwendet werden [siehe Dosierung und Verwaltung ].
Lokale Reizung
Bei 52% der mit mindestens einer Dosis Trudhesa behandelten Patienten wurden lokale irritative Symptome berichtet, die in einer offen markierten Studie behandelt wurden, die eine wiederholte Verwendung von Trudhesa über 6 bis 12 Monate ermöglichte. Die häufigsten lokalen irritativen Symptome (mindestens 1%der Patienten) waren Nasopharyngitis (21%) Rhinitis (19%) Nasenbeschwerden (7%) Produktgeschmack abnormaler/Dysgeusie (6%) Sinusitis (5%) Sinus -Unbehagen (4%) olfaktoriem, olfaktorischem Test, der auf einer Änderung der Preise bei einem Veränderung bei einem Veränderung bei einem Schaden wurde. Identifikationstest (Upsit)] (4%) Epistaxis (3%) Pharyngitis (3%) Nasenschleimhautstörung (2%) Veränderung des Geruchs (1%) Ohrenbeschwerden (1%) und Rhinorrhoe (1%). Wenn ein schwerwiegendes lokales Irritationsereignis aus keinen anderen zugerichteten Gründen erfolgt, sollte Trudhesa bis zum Auflösen des Ereignisses vorübergehend ausgesetzt werden. Wenn das Ereignis nicht auflöst oder es mit Wiederholungen trudhesa wiederholt, sollte dauerhaft eingestellt werden. Die Verabreichung von Trudhesa sollte die Dosierungsrichtlinien nicht überschreiten und nicht für die chronische tägliche Verabreichung verwendet werden [siehe Dosierung und Verwaltung ].
Nasengewebe bei Tieren, die täglich mit Dihydroergotamin -Mesylat behandelt wurden, zeigten eine leichte Schleimhautreizung, die durch Schleimzell- und Übergangszellhyperplasie und Plattenepithelkaplasie gekennzeichnet war. Die Veränderungen der Ratten -Nasenschleimhaut nach 64 Wochen waren weniger schwerwiegend als in 13 Wochen. Lokale Auswirkungen auf das Atemgewebe nach chronischer intranasaler Dosierung bei Tieren wurden nicht bewertet.
Patientenberatungsinformationen
Raten Sie dem Patienten, die von der FDA zugelassene Patientenkennzeichnung zu lesen ( Medikamentenhandbuch Und Anweisungen zur Verwendung ).
rosa Pille mit K56 darauf
Schwerwiegende und/oder lebensbedrohliche Reaktionen mit gleichzeitiger Verabreichung von CYP3A4-Inhibitoren
Die Patienten informieren, dass eine schwerwiegende und/oder lebensbedrohliche periphere Ischämie (zerebrale Ischämie und/oder Ischämie der Extremitäten) mit der gleichzeitigen Verabreichung von Dihydroergotam-Mesylat und starken CYP3A4-Inhibitoren wie Makrolidantibiotik und Protease-Inhibitoren in Verbindung gebracht wurde Kontraindikationen WARNUNGS AND PRECAUTIONS Und Wechselwirkungen mit Arzneimitteln ].
Myokardischämie und/oder Infarkt anderer Herzereignisse zerebrovaskuläre Ereignisse und Todesfälle
Informieren Sie die Patienten über das Risiko für schwerwiegende Herz cerebrovaskuläre und andere Vasospasmus -Ereignisse. Raten Sie den Patienten, ihren Gesundheitsdienstleister zu informieren, wenn sie Risikofaktoren oder Symptome entwickeln, während sie Trudhesa einnehmen. Informieren Sie die Patienten, dass Nikotin Vasokonstriktion provozieren kann, die zu einer größeren ischämischen Reaktion prädisponiert werden [siehe WARNUNGS AND PRECAUTIONS ].
Medikamente Überbeanspruchung Kopfschmerzen
Informieren Sie die Patienten, dass die Verwendung von Medikamenten zur Behandlung von Migräneanfällen für 10 oder mehr Tage pro Monat zu einer Verschlechterung von Kopfschmerzen führen kann und die Patienten dazu ermutigt, Kopfschmerzfrequenz und Drogenkonsum aufzuzeichnen (z. B. durch Kopfschmerz -Tagebuch) [siehe WARNUNGS AND PRECAUTIONS ].
Lokale Reizung
Raten Sie den Patienten, ihren Gesundheitsdienstleister zu benachrichtigen, wenn sie eine störende lokale Reizung haben [siehe WARNUNGS AND PRECAUTIONS ].
Wechselwirkungen mit Arzneimitteln
Raten Sie den Patienten, ihre Gesundheitsdienstleister zu informieren, wenn sie ein Verschreibung oder rezeptfreie Medikamente einnehmen oder planen Wechselwirkungen mit Arzneimitteln ].
Schwangerschaft
Beraten Sie Patienten über das Risiko für Frühgeborene. Raten Sie Frauen, ihren Gesundheitsdienstleister zu informieren, wenn sie schwanger sind oder schwanger werden [siehe WARNUNGS AND PRECAUTIONS Verwendung in bestimmten Populationen ]
Stillzeit
Raten Sie den Patienten, während der Behandlung mit Trudhesa nicht zu stillen [siehe Verwendung in bestimmten Populationen ].
Wichtige Verwaltungsanweisungen
Beraten Sie den Patienten, dass Trudhesa vor der Verwendung zusammengebaut werden muss und dass das Gerät vor der Verabreichung vorhanden sein muss (d. H. 4 -mal gepumpt). Weisen Sie die Patienten an, Trudhesa innerhalb von 8 Stunden zu verwenden oder zu verwerfen, sobald die Fläschchen geöffnet oder das Produkt zusammengestellt wurde.
Nichtklinische Toxikologie
Karzinogenese -Mutagenese -Beeinträchtigung der Fruchtbarkeit
Karzinogenese
Die Bewertung des krebserzeugenden Potentials von Dihydroergotamin -Mesylat bei Mäusen und Ratten wurde nicht bewertet.
Mutagenese
Dihydroergotamin -Mesylat war in einem negativ in vitro Mutagenität (AMES) -Test und positiv in in vitro Chromosomalaberration (V79 Chinese Hamster Cell Assay mit metabolischer Aktivierung und Lymphozyten -Assays des menschlichen peripheren Blutes). Dihydroergotamin war negativ in vergeblich Mikronukleus -Assays in Maus und Hamster.
Beeinträchtigung der Fruchtbarkeit
Es gab keine Hinweise auf eine Beeinträchtigung der Fertilität bei Ratten, die intranasale Dosen von Dihydroergotamin -Mesylat von bis zu 1,6 mg/Tag verzeichneten, die mit Plasmakapletten (AUC) ungefähr dreifache 3 -mal assoziiert waren, die beim Menschen bei der maximal empfohlenen menschlichen Dosis von 2,9 mg/Tag.
Verwendung in bestimmten Populationen
Schwangerschaft
Risikozusammenfassung
Die verfügbaren Daten aus der veröffentlichten Literatur zeigen ein erhöhtes Risiko für Frühgeborene mit Trudhesa -Verwendung während der Schwangerschaft. Vermeiden Sie die Verwendung von Trudhesa während der Schwangerschaft [siehe WARNUNGS AND PRECAUTIONS ]. Daten collected over decades have shown no increased risk of major birth defects or miscarriage with use of dihydroergotamine mesylate during pregnancy.
In animal studies adverse effects on embryofetal development were observed following administration of dihydroergotamine mesylate during pregnancy (decreased fetal body weight and/or skeletal ossification) in rats and rabbits or during pregnancy and lactation in rats (decreased body weight and impaired reproductive function in the offspring) in rats at doses less than those used clinically and which were not associated with maternal toxicity (see Daten ).
Die geschätzte Rate schwerer Geburtsfehler (NULL,2%bis 2,9%) und Fehlgeburt (17%) bei Lieferungen an Frauen mit Migräne ähneln den bei Frauen ohne Migräne gemeldeten Raten. Alle Schwangerschaften haben ein Hintergrundrisiko für einen Verlust von Geburtsfehlern oder andere nachteilige Ergebnisse. In der US -allgemeinen Bevölkerung beträgt das geschätzte Hintergrundrisiko für größere Geburtsfehler und Fehlgeburten in klinisch anerkannten Schwangerschaften 2% bis 4% bzw. 15% bis 20%.
Daten
Tierdaten
Die intranasale Verabreichung von Dihydroergotamin -Mesylat an schwangere Ratten während der gesamten Organogenese führte zu einem verringerten Körpergewicht des Fötus und/oder einer Skelett -Ossifikation bei Dosen von 0,16 mg/Tag (assoziiert mit Plasma -Expositionen [AUC], die bei Menschen beim menschlich empfohlenen menschlichen Dosis [mrHD] von 2,9 mg) oder zu einem maximal empfohlenen Menschen [mrHD] von 2,9 mg) oder mehr. Bei Ratten wurde kein Auswirkungsniveau für die Embryofetaltoxizität identifiziert. Die intranasale Verabreichung von Dihydroergotamin -Mesylat zu schwangeren Kaninchen während der gesamten Organogenese führte zu einer verminderten Skelett -Ossifikation bei 3,6 mg/Tag. Bei der Dosis ohne Effekt (NULL,2 mg/Tag) für nachteilige Auswirkungen auf die Embryofetalentwicklung bei Kaninchen-Plasmakonpositionen (AUC) waren beim Menschen bei der MRHD geringer.
Die intranasale Verabreichung von Dihydroergotamin -Mesylat an weibliche Ratten während der gesamten Schwangerschaft und der Laktation führte zu einem verringerten Körpergewicht und einer beeinträchtigten Fortpflanzungsfunktion (verringerte Paarungsindizes) wurden in den Nachkommen bei Dosen von 0,16 mg/Tag oder größer beobachtet. Eine Dosis ohne Effekt für unerwünschte Entwicklungseffekte bei Ratten wurde nicht festgestellt.
Auswirkungen auf die Entwicklung traten in Dosen unterhalb derjenigen auf, die in diesen Studien Hinweise auf eine signifikante mütterliche Toxizität lieferten.
Dihydroergotamin-induziertes intrauterines Wachstumsverzögerung wurde auf eine verringerte Uteroplazentalblutung zurückgeführt, die sich aus einer verlängerten Vasokonstriktion der Uterusgefäße und/oder einem erhöhten Myometriumonus ergibt.
Stillzeit
Risikozusammenfassung
Es gibt keine Daten zum Vorhandensein von Dihydroergotamin in der Muttermilch; Ergotamin ist jedoch in der Muttermilch ein verwandtes Medikament vorhanden. Es gibt Berichte über Durchfall, das sich schwacher Impuls und instabilen Blutdruck bei gestillten Säuglingen erbricht, die Ergotamin ausgesetzt sind. Trudhesa kann die Milchversorgung verringern, da sie den Prolaktinspiegel senken kann. Aufgrund des Potenzials für eine verringerte Milchversorgung und schwerwiegende unerwünschte Ereignisse im gestillten Kind, einschließlich Durchfall, erbricht schwacher Puls und instabiler Blutdruck den Patienten, während der Behandlung mit Trudhesa und 3 Tage nach der letzten Dosis nicht zu stillen. Die Muttermilchversorgung in dieser Zeit sollte gepumpt und weggeworfen werden.
Pädiatrische Verwendung
Sicherheit und Wirksamkeit bei pädiatrischen Patienten wurden nicht festgestellt.
Geriatrische Verwendung
Klinische Studien zu Trudhesa und anderen Dihydroergotamin -Mesylatprodukten umfassten keine ausreichende Anzahl von Probanden ab 65 Jahren, um festzustellen, ob sie unterschiedlich als jüngere Probanden reagieren. Im Allgemeinen sollte die Dosisauswahl für einen älteren Patienten vorsichtig sein, normalerweise am unteren Ende des Dosierungsbereichs, der die größere Häufigkeit einer verringerten Nieren- oder Herzfunktion von Lebern und einer gleichzeitigen Erkrankung oder einer anderen medikamentösen Therapie widerspiegelt.
Überdosis Information for Trudhesa
Symptome
Übermäßige Dosen von Dihydroergotamin können zu peripheren Anzeichen und Symptomen des Ergotismus führen. Im Allgemeinen ähneln die Symptome einer akuten Trudhesa -Überdosis denen einer Ergotamin -Überdosierung, obwohl es möglicherweise weniger ausgeprägte Übelkeit und Erbrechen mit Trudhesa geben kann. Die Symptome einer Überdosierung einer Ergotamin umfassen Folgendes: Taubheit Kribbeln und Zyanose der Extremitäten, die mit verminderten oder fehlenden peripheren Impulsen verbunden sind; Atemdepression; eine Erhöhung und/oder Abnahme des Blutdrucks normalerweise in dieser Reihenfolge; Verwirrungsdeliriumkrämpfe und Koma; und/oder ein gewisses Maß an Übelkeit Erbrechen und Bauchschmerzen.
Bei Labortieren war Dihydroergotamin tödlich, wenn in intravenösen Dosen von 44 mg/kg bei Mäusen 130 mg/kg bei Ratten und 37 mg/kg bei Kaninchen 130 mg/kg verabreicht wurden.
Behandlung
Behandlung includes discontinuance of the drug local application of warmth to the affected area the administration of vasodilators Und nursing care to prevent tissue damage. Up-to-date information about the treatment of overdosage can often be obtained from a certified Regional Poison Control Center.
Kontraindikationen for Trudhesa
Trudhesa ist bei Patienten kontraindiziert:
was man auf eine Reise einpacken sollte
- mit gleichzeitiger Verwendung starker CYP3A4 -Inhibitoren wie Protease -Inhibitoren (z. B. Ritonavir Nelfinavir oder Indinavir) Makrolidantibiotika (z. B. Erythromycin oder Clarithromycin) und Antimungal (Ketoconazol oder ITraconazol) [siehe [siehe [siehe) [ans WARNUNGS AND PRECAUTIONS Und Wechselwirkungen mit Arzneimitteln ]
- Mit ischämischen Herzerkrankungen (Angina Pectoris -Anamnese des Myokardinfarkts oder dokumentierten stillen Ischämie) oder Patienten mit klinischen Symptomen oder Befunden, die mit Vasospasmus der Koronararterie übereinstimmen, einschließlich Prinzmetals Variante Angina [siehe WARNUNGS AND PRECAUTIONS ]
- mit unkontrollierter Bluthochdruck [siehe WARNUNGS AND PRECAUTIONS ]
- mit peripherer arterieller Erkrankung
- mit Sepsis
- Nach Gefäßchirurgie
- mit schwerer Leberbeeinträchtigung
- mit schwerer Nierenbeeinträchtigung
- mit bekannter Überempfindlichkeit gegenüber Ergot -Alkaloiden
- mit jüngster Verwendung (d. H. innerhalb von 24 Stunden) anderer 5-HT 1 Agonisten (z. B. Sumatriptan) oder Ergotamin-haltige oder ergot-Medikamente [siehe Wechselwirkungen mit Arzneimitteln ]
- mit gleichzeitiger Verwendung peripherer und zentraler Vasokonstriktoren, da die Kombination zu einer additiven oder synergistischen Erhöhung des Blutdrucks führen kann [siehe WARNUNGS AND PRECAUTIONS ]
Klinische Pharmakologie for Trudhesa
Wirkungsmechanismus
Dihydroergotamin bindet mit hoher Affinität zu 5-HT 1da Und 5-HT 1 dB Rezeptoren. Die therapeutische Aktivität von Dihydroergotamin in Migräne wird im Allgemeinen auf die agonistischen Effekte bei 5-HT zurückgeführt 1d Rezeptoren.
Pharmakodynamik
Bei Patienten mit und ohne Bluthochdruck wurde eine signifikante Blutdruckerhöhung berichtet [siehe WARNUNGS AND PRECAUTIONS ].
Dihydroergotamin besitzt oxytocische Eigenschaften [siehe WARNUNGS AND PRECAUTIONS ].
Pharmakokinetik
Absorption
Die mittlere Zeit von der Dosierung bis zur maximalen Plasmakonzentration nach Trudhesa -Verabreichung betrug ungefähr 0,5 Stunden.
Verteilung
Dihydroergotamin -Mesylat ist zu 93% Plasmaprotein gebunden. Das scheinbare Verteilungsvolumen des stationären Zustands beträgt ungefähr 800 Liter.
Beseitigung
Stoffwechsel
In der oralen Verabreichung wurden vier Dihydroergotamin -Mesylatmetaboliten identifiziert. Der Hauptmetabolit 8'-ß-Hydroxy Dihydroergotamin zeigt Affinität vergeblich Und in vitro . Die anderen Metaboliten, d. H. Dihydrolyssäure -Dihydrolydrolydrie -Amid und ein Metaboliten, das durch oxidatives Öffnen des Prolinrings gebildet wird, sind von geringer Bedeutung. Nach der Verabreichung der Nasenverabreichung machen Gesamtmetaboliten nur 20% bis 30% des Plasma -AUC aus. Die systemische Clearance von Dihydroergotamin -Mesylat nach intravenöser und intramuskulärer Verabreichung beträgt 1,5 l/min. Die quantitative pharmakokinetische Charakterisierung der vier Metaboliten wurde nicht durchgeführt.
Ausscheidung
Der Hauptausscheidungsweg von Dihydroergotamin erfolgt über die Galle im Kot. Die Gesamtkörperfreiheit beträgt 1,5 l/min, was hauptsächlich hepatische Clearance widerspiegelt. Nur 6% bis 7% der unveränderten Dihydroergotamin werden nach intramuskulärer Injektion im Urin ausgeschieden. Die Nierenclearance (NULL,1 l/min) wird von der Verabreichung von Dihydroergotamin nicht beeinflusst.
Die mittlere scheinbare Halbwertszeit der Trudhesa-Nasenverabreichung bei gesunden Probanden beträgt ungefähr 12 Stunden.
Spezifische Populationen
Es wurden keine Studien zur Auswirkung der ethnischen Zugehörigkeit oder Schwangerschaft von Nieren- oder Leberunternehmen geschlechtsspezifische Pharmakokinetik durchgeführt [siehe Kontraindikationen Verwendung in bestimmten Populationen ].
Arzneimittelinteraktionsstudien
CYP3A4 -Inhibitoren
Seltene Berichte über Ergotismus wurden von Patienten erhalten, die mit Dihydroergotamin- und Makrolid -Antibiotika (z. B. Clarithromycin -Erythromycin) behandelt wurden, und von Patienten, die mit Dihydroerergotamin und Protease -Inhibitoren (z. B. Ritonavire) aufgrund der Hemmung von CYP3A -Metabitoren (z. B. ERGOTAM) behandelt wurden, wurden aufgrund der Hemmung von CYP3A -Metabitoren (z. Kontraindikationen ].
Andere Drogen
Die Pharmakokinetik von Dihydroergotamin schien durch die gleichzeitige Verwendung eines lokalen Vasokonstriktors nicht signifikant beeinflusst zu werden.
Mehrere orale Dosen des für die Migräneprophylaxe verwendeten β-Adrenozeptor-Antagonisten-Propranolols hatten keinen signifikanten Einfluss auf die Cmax Tmax oder AUC von Dihydroergotamin-Dosen bis zu 4 mg. Propranolol kann jedoch die vasokonstriktive Wirkung von Ergotamin potenzieren [siehe Wechselwirkungen mit Arzneimitteln ].
Die Wirkung von oralen Kontrazeptiva auf die Pharmakokinetik von Trudhesa wurde nicht untersucht.
Klinische Studien
Die Wirksamkeit von Trudhesa basiert auf der relativen Bioverfügbarkeit von Trudhesa -Nasenspray im Vergleich zu Dihydroergotamin -Mesylat -Nasenspray bei gesunden Probanden.
Die nachstehend beschriebenen klinischen Studien wurden unter Verwendung von Dihydroergotamin -Mesylat -Nasenspray durchgeführt.
Die Wirksamkeit von Dihydroergotamin-Mesylat-Nasenspray für die akute Behandlung von Migränekopfschmerzen wurde in vier randomisierten, doppelblind-placebo-kontrollierten Studien in den USA bewertet. Die Patientenpopulation war überwiegend überwiegend weiblich (87%) und Kaukasische (95%) mit einem mittleren Alter von 39 Jahren (Bereich 18 bis 65 Jahre). Die Patienten behandelten mit einer einzelnen Dosis von Studienmedikamenten mit einer einzigen mittelschweren bis schweren Migränekopfschmerzen und bewerteten die Schwere der Schmerzen über die 24 Stunden nach der Behandlung. Die Kopfschmerzreaktion wurde 0,5 1 2 3 und 4 Stunden nach der Dosierung bestimmt und als Verringerung des Schweregrads der Kopfschmerzen auf milde oder keine Schmerzen definiert. In den Studien 1 und 2 wurde eine Vier-Punkte-Schmerzintensitätsskala verwendet; In den Studien 3 und 4 wurde eine Fünf-Punkte-Skala verwendet, um die Schmerzreaktion aufzuzeichnen. Obwohl Rettungsmedikamente in allen vier Studien zugelassen wurden, wurden Patienten angewiesen, sie während der vierstündigen Beobachtungszeit nicht zu verwenden. In den Studien 3 und 4 wurde eine Gesamtdosis von 2 mg mit Placebo verglichen. In den Studien 1 und 2 Dosen von 2 und 3 mg wurden bewertet und zeigten keinen Vorteil der höheren Dosis für eine einzelne Behandlung. In allen Studien erhielten die Patienten ein Regime, das aus 0,5 mg in jedem Nasenloch bestand, das in 15 Minuten wiederholt wurde (und in den Studien 1 und 2 in weiteren 15 Minuten für die 3 mg -Dosis).
Der Prozentsatz der Patienten, die 4 Stunden nach der Behandlung eine Kopfschmerzantwort erzielen, war bei Patienten, die 2 mg Dosen Dihydroergotamin -Mesylat -Nasenspray erhielten, im Vergleich zu Patienten, die in 3 der 4 Studien Placebo erhielten (siehe Tabelle 2 und Abbildung 3 und Abbildung 2).
Tabelle 2 Studien 1 und 2: Prozentsatz der Patienten mit Kopfschmerzreaktion a 2 und 4 Stunden nach einer einzigen Behandlung von Studienmedikamenten (Dihydroergotamin -Mesylat -Nasenspray oder Placebo)
| N | 2 Stunden | 4 Stunden | ||
| Studie 1 | Dihydroergotamin -Mesylat -Nasenspray | 105 | 61%** | 70%** |
| Placebo | 98 | 23% | 28% | |
| Unterschied von Placebo | 37% | 42% | ||
| Studie 2 | Dihydroergotamin -Mesylat -Nasenspray | 103 | 47% | 56%* |
| Placebo | 102 | 33% | 35% | |
| Unterschied von Placebo | 14% | 21% | ||
| a Die Kopfschmerzreaktion wurde als Verringerung des Schweregrads der Kopfschmerzen auf milde oder keine Schmerzen definiert. Die Kopfschmerzreaktion basierte auf der Schmerzintensität, die vom Patienten unter Verwendung einer Vier-Punkte-Schmerzintensitätsskala interpretiert wurde. *P -Wert <0.01 ** p Wert <0.001 |
Tabelle 3 Studien 3 und 4: Prozentsatz der Patienten mit Kopfschmerzreaktion a 2 und 4 Stunden nach einer einzigen Behandlung von Studienmedikamenten (Dihydroergotamin -Mesylat -Nasenspray oder Placebo)
| N | 2 Stunden | 4 Stunden | ||
| Studie 3 | Dihydroergotamin -Mesylat -Nasenspray | 50 | 32 | 48%* |
| Placebo | 50 | 20% | 22% | |
| Unterschied von Placebo | 12% | 26% | ||
| Studie 4 | Dihydroergotamin -Mesylat -Nasenspray | 47 | 30% | 47% |
| Placebo | 50 | 20% | 30% | |
| Unterschied von Placebo | 10% | 17% | ||
| a Die Kopfschmerzreaktion wurde als Verringerung des Schweregrads der Kopfschmerzen auf milde oder keine Schmerzen definiert. Die Kopfschmerzreaktion wurde auf einer Fünf-Punkte-Skala bewertet, die die Schmerzreaktion beinhaltete. *P -Wert <0.01 |
Die nachstehenden Kaplan-Meier-Diagramme (Abbildung 1 und Abbildung 2) liefern eine Schätzung der Wahrscheinlichkeit, dass ein Patient auf eine einzelne 2 mg-Dosis von Dihydroergotamin-Mesylat-Nasenspray als Funktion der Zeit in Ablauf der Behandlung reagiert hat.
Abbildung 1 Geschätzte Wahrscheinlichkeit eines Patienten, der in den vier Stunden nach einer einzelnen 2 mg -Dosis Dihydroergotamin -Mesylat -Nasenspray als Funktion der seit Beginn der Behandlung verstrichenen Zeit reagierte*
| *Die Abbildung zeigt die Wahrscheinlichkeit über die Zeit, nach der Behandlung mit Dihydroergotamin -Mesylat -Nasenspray eine Reaktion zu erhalten. Die Kopfschmerzreaktion basierte auf der Schmerzintensität, die vom Patienten unter Verwendung einer 4 -Punkte -Schmerzintensitätsskala interpretiert wurde. Patienten, die innerhalb von 4 Stunden keine Reaktion erreichen, wurden auf 4 Stunden zensiert. |
Abbildung 2 Geschätzte Wahrscheinlichkeit eines Patienten, der in den vier Stunden nach der Dosierung auf Dihydroergotamin -Mesylat -Nasenspray reagiert*
| *Die Abbildung zeigt die Wahrscheinlichkeit über die Zeit, nach der Behandlung mit Dihydroergotamin -Mesylat -Nasenspray eine Reaktion zu erhalten. Die Kopfschmerzreaktion wurde auf einer Fünf-Punkte-Skala bewertet, die die Schmerzreaktion beinhaltete. Patienten, die innerhalb von 4 Stunden keine Reaktion erreichen, wurden auf 4 Stunden zensiert. |
Bei Patienten mit Migräne-assoziierter Übelkeitsphotophobie und Phonophobie zu Studienbeginn gab es 2 und 4 Stunden nach Verabreichung von Dihydroergotamin-Mesylat-Nasenspray im Vergleich zu Placebo eine geringere Inzidenz dieser Symptome.
Die Patienten durften nicht 8 Stunden lang zusätzliche Behandlungen anwenden, bevor die Medikamentendosierung der Studie und während des 4-stündigen Beobachtungszeitraums nach der Behandlung der Studie. Nach dem 4-stündigen Beobachtungszeitraum durften Patienten zusätzliche Behandlungen anwenden. Für alle Studien ist die geschätzte Wahrscheinlichkeit von Patienten, die zusätzliche Behandlungen für ihre Migräne über die 24 Stunden nach der einzelnen 2 -mg -Dosis der Studienbehandlung verwenden, in Abbildung 3 unten zusammengefasst.
Abbildung 3 Geschätzte Wahrscheinlichkeit eines Patienten, der zusätzliche Behandlungen für Migräne über die 24 Stunden nach Dihydroergotamin -Mesylat -Nasenspray 2 mg (oder Placebo)* verwendet
| *Kaplan-Meier-Diagramm basierend auf Daten, die aus allen Studien mit Patienten erhalten wurden, die keine zusätzlichen Behandlungen anwenden, die auf 24 Stunden zensiert wurden. Alle Patienten erhielten eine einzige Behandlung von Studienmedikamenten für ihren Migräneanfall. Die Handlung umfasst auch Patienten, die keine Reaktion auf die anfängliche Dosis hatten. |
Weder Alter noch Geschlecht scheinen die Reaktion des Patienten auf Dihydroergotamin -Mesylat -Nasenspray zu beeinflussen. Die rassistische Verteilung der Patienten war nicht ausreichend, um die Auswirkung der Rasse auf die Wirksamkeit des Dihydroergotamin -Mesylat -Nasensprays zu bestimmen.
Patienteninformationen für Trudhesa
Trusta ™
(Trae - Deh - eins)
(Dihydroergotamin -Mesylat) Nasenspray
Was sind die wichtigsten Informationen, die ich über Trudhesa wissen sollte?
Trudhesa kann schwerwiegende Nebenwirkungen verursachen, einschließlich:
- Ernsthafte Probleme mit der Durchblutung an Beinen und Füßen (periphere Ischämie). Trudhesa kann eine periphere Ischämie verursachen, wenn Sie sie mit bestimmten Medikamenten einnehmen, die als CYP3A4 -Inhibitoren bekannt sind. Periphere Ischämie kann zu Schlaganfall und Tod führen. Hören Sie auf, Trudhesa zu nehmen, und erhalten Sie sofort medizinische Hilfsmittel, wenn Sie folgende Symptome haben:
- Krämpfen und Schmerzen in den Beinen oder Hüften
- Gefühl der Schwere oder Enge in deinen Beinmuskeln
- Brennen oder schmerzende Schmerzen in Ihren Füßen oder Zehen während der Ruhe
- Taubheit Kribbeln oder Schwäche in deinen Beinen
- Kaltes Gefühl oder Farbwechsel in 1 oder beiden Beinen oder Füßen
- verschwommene Rede
- plötzliche Schwäche
Nehmen Sie keine Medikamente, die als starke CYP3A4 -Inhibitoren bekannt sind, wie:
-
- Ritonavir
- Erythromycin
- Ketoconazol
- Netfinavir
- Clarithromycin
- Itraconazol
Dies sind nicht alle Medikamente, die sich auswirken könnten, wie Trudhesa funktioniert. Ihr Gesundheitsdienstleister kann Ihnen sagen, ob es sicher ist, Trudhesa mit anderen Medikamenten zu nehmen.
Was ist Trudhesa?
Trudhesa ist eine verschreibungspflichtige Medizin, die für die akute Behandlung von Migräne mit oder ohne Aura bei Erwachsenen verwendet wird.
- Trudhesa wird nicht verwendet, um Migräne zu verhindern.
- Trudhesa wird nicht verwendet, um andere Arten von Kopfschmerzen wie hemiplegisch (die Sie nicht in der Lage machen, sich auf einer Seite Ihres Körpers zu bewegen) oder Basilar (seltene Form der Migräne mit Aura) Migräne.
Es ist nicht bekannt, ob Trudhesa bei Kindern sicher und wirksam ist.
Nehmen Sie Trudhesa nicht, wenn Sie:
- nehmen Medikamente ein, die als starke CYP3A4 -Inhibitoren bekannt sind.
- haben Herzprobleme oder eine Vorgeschichte von Herzproblemen.
- einen unkontrollierten Bluthochdruck haben.
- Verengung der Blutgefäße in Ihren Beinen Armen Magen oder Nieren (periphere Gefäßerkrankungen).
- Sepsis haben.
- haben eine Gefäßoperation.
- schwere Leberprobleme haben.
- schwerwiegende Nierenprobleme haben.
- sind allergisch gegen Dihydroergotamin -Mesylat -Ergot -Alkaloide oder Inhaltsstoffe in Trudhesa. Eine vollständige Liste von Zutaten finden Sie im Ende dieses Medikamentenleitfadens.
- haben in den letzten 24 Stunden einen der folgenden Medikamente eingenommen:
- Sumatriptan
- Almotriptan
- Eletriptan
- frovatriptat
- Naratriptan
- Rizatriptan
- Ergotamin- oder Ergotamin-Arzneimittel
- Halten Sie alle Medikamente eingenommen, die Ihre Blutgefäße einschränken oder Ihren Blutdruck erhöhen.
Fragen Sie Ihren Gesundheitsdienstleister, ob Sie nicht sicher sind, ob Sie diese Medikamente einnehmen. Ihr Gesundheitsdienstleister kann Ihnen sagen, ob es sicher ist, Trudhesa mit anderen Medikamenten zu nehmen.
Bevor Sie Trudhesa nehmen, teilen Sie Ihrem Gesundheitsdienstleister alle Ihre medizinischen Erkrankungen mit, einschließlich, wenn Sie:
- hohen Blutdruck haben.
- Leberprobleme haben.
- Nierenprobleme haben.
- Rauch.
- sind schwanger oder planen, schwanger zu werden. Trudhesa kann vorzeitige Arbeit verursachen. Trudhesa sollte während der Schwangerschaft vermieden werden. Sprechen Sie sofort mit Ihrem Gesundheitsdienstleister, wenn Sie schwanger sind oder schwanger werden möchten.
- stillen oder planen zu stillen. Trudhesa kann die Muttermilchversorgung verringern und in Ihre Muttermilch gingen. Trudhesa kann für Ihr Baby schädlich sein. Stillen Sie Ihr Baby nicht, während Sie Trudhesa und 3 Tage nach der Verwendung von Trudhesa einnehmen. Sprechen Sie mit Ihrem Gesundheitsdienstleister darüber, wie Sie Ihr Baby am besten füttern können, wenn Sie Trudhesa einnehmen.
Teilen Sie Ihrem Gesundheitsdienstleister über alle Medikamente, die Sie einnehmen einschließlich verschreibungspflichtiger und rezeptfreier Medikamente Vitamine und Kräuterpräparate. Ihr Gesundheitsdienstleister entscheidet, ob Sie Trudhesa mit Ihren anderen Medikamenten einnehmen können.
Sagen Sie Ihrem Gesundheitsdienstleister vor allem, wenn Sie einnehmen:
-
- Sumatriptan
- Fluconazol
- Propranolol oder andere Medikamente, die Ihre Herzfrequenz senken können
- Ergot-Medizin o Grapefruitsaft o alle Medikamente, die Ihren Blutdruck erhöhen können
- Saquinavir o Zileuton O Selektives Serotonin Wiederaufnahme Inhibitoren
- Nefazodon
- Nikotin
Dies sind nicht alle Medikamente, die sich auswirken könnten, wie Trudhesa funktioniert. Ihr Gesundheitsdienstleister kann Ihnen sagen, ob es sicher ist, Trudhesa mit anderen Medikamenten zu nehmen.
Wie soll ich Trudhesa nehmen?
- Bestimmte Menschen sollten ihre erste Dosis Trudhesa in der Arztpraxis oder in einer anderen medizinischen Umgebung einnehmen. Fragen Sie Ihren Arzt, ob Sie Ihre erste Dosis in einer medizinischen Umgebung nehmen sollten.
- Verwenden Sie Trudhesa genau so, wie Ihr Gesundheitsdienstleister Ihnen sagt, dass Sie es verwenden sollen. Lesen und befolgen Sie die Anweisungen in der Anweisungen zur Verwendung Dies ist das Trudhesa -Paket vor der Verwendung vorhanden.
- Sie sollten Trudhesa verwenden, sobald die Symptome Ihrer Kopfschmerzen beginnen, aber dies kann jederzeit während einer Migräne angegeben werden.
- Nachdem Trudhesa zusammengefügt und das Gerät 1 Zeit in jedem Nasenloch (eine vollständige Dosis) besprühen wird.
- Wenn Ihre Kopfschmerzen nach der ersten vollständigen Dosis zurückkommen oder Sie nur eine Erleichterung von Ihren Kopfschmerzen erhalten, können Sie eine zweite Dosis 1 Stunde nach der ersten vollständigen Dosis verwenden. Verwenden Sie für die zweite Dosis ein neues Trudhesa -Nasenspray -Gerät.
- Verwenden Sie nicht mehr als 2 Dosen Trudhesa innerhalb eines Zeitraums von 24 Stunden oder drei Dosen innerhalb eines Zeitraums von 7 Tagen.
- Wenn Sie zu viel Trudhesa verwenden, rufen Sie Ihren Gesundheitsdienstleister an oder gehen Sie sofort in die nächste Notaufnahme des Krankenhauses.
- Die Einnahme von Trudhesa für 10 oder mehr Tage im Monat kann Ihre Kopfschmerzen verschlimmern. Sie sollten aufschreiben, wenn Sie Kopfschmerzen haben und wenn Sie Trudhesa einnehmen, damit Sie mit Ihrem Gesundheitsdienstleister darüber sprechen können, wie Trudhesa für Sie arbeitet.
Was sind die möglichen Nebenwirkungen von Trudhesa?
Trudhesa kann schwerwiegende Nebenwirkungen verursachen, einschließlich:
Sehen Was sind die wichtigsten Informationen, die ich über Trudhesa wissen sollte?
- Herzinfarkt und andere Herzprobleme. Herzprobleme können zum Tod führen. Hören Sie auf, Trudhesa zu nehmen, und erhalten Sie sofort medizinische Hilfsmittel, wenn Sie die folgenden Symptome von a haben Herzinfarkt :
- Beschwerden in der Mitte Ihrer Brust, die länger als ein paar Minuten dauert oder die weggeht und zurückkommt
- Starker Straffheitschmerzdruck oder Schwere in Ihrem Brusthalshals oder Kiefer
- Schmerz oder Beschwerden in den Armen Rückenhalskiefer oder Magen
- Atemnot mit oder ohne Brust des Brusts
- kaltes Schweiß ausbrechen
- Brechreiz or Erbrechen
- sich benommen fühlen
Trudhesa ist nicht für Menschen mit Risikofaktoren für Herzerkrankungen gedacht, es sei denn, eine Herzuntersuchung wird durchgeführt und zeigt kein Problem. Sie haben ein höheres Risiko für Herzerkrankungen, wenn Sie:
-
- einen hohen Blutdruck haben
- hohe Cholesterinspiegel haben
- Rauch
- sind übergewichtig
- Diabetes haben
- eine familiäre Vorgeschichte von Herzerkrankungen haben
- Schlaganfall. Hören Sie auf, Trudhesa zu nehmen, und erhalten Sie sofort medizinische Hilfsmittel, wenn Sie die folgenden Symptome eines Schlaganfalls haben:
- Gesicht schlängelend
- ungewöhnliche Schwäche oder Taubheit
- verschwommene Rede
- Änderungen in Farb- oder Empfindungen in Ihren Fingern und Zehen (Raynaud -Syndrom).
- Magen- und Darmprobleme (gastrointestinale und kolonische ischämische Ereignisse). Zu den Symptomen von gastrointestinalen und kolonischen ischämischen Ereignissen gehören:
- plötzliche oder schwere Magenschmerzen
- Verstopfung oder Durchfall
- Magenschmerzen nach den Mahlzeiten
- blutiger Durchfall
- Gewichtsverlust
- Fieber
- Brechreiz or Erbrechen
- Blutdruck erhöhen.
- Medizin Überbeanspruchung Kopfschmerzen. Einige Leute, die zu viel Trudhesa verwenden, können ihre Kopfschmerzen verschlimmern (medizinische Kopfschmerzen). Wenn sich Ihre Kopfschmerzen verschlimmern, kann Ihr Gesundheitsdienstleister entscheiden, Ihre Behandlung mit Trudhesa zu stoppen.
- Frühgeborene.
- Gewebeveränderungen (fibrotische Komplikationen). Nflammation und faserähnliche Gewebe, das nicht normal ist (Fibrose), kann um Lunge und Magen auftreten.
- Verbrennen von Gefühlen in Nasenmund und Hals und abnormalem Geschmack.
Die häufigsten Nebenwirkungen von Trudhesa sind:
- laufende Nase
- Reaktionen für Anwendungsstellen
- Schläfrigkeit
- Brechreiz
- Schwindel
- Halsschmerzen
- abnormaler Geschmack
- Erbrechen
- Durchfall
Dies sind nicht alle möglichen Nebenwirkungen Trudhesa.
Rufen Sie Ihren Arzt an, um medizinische Beratung zu Nebenwirkungen zu erhalten. Sie können die FDA bei 1-800-FDA-1088 Nebenwirkungen melden.
Wie soll ich Trudhesa aufbewahren?
Halten Sie Trudhesa von Hitze und Licht fern.
- Lagern Sie Trudhesa bei Raumtemperatur zwischen 68 ° F und 77 ° F (20 ° C bis 25 ° C).
- Nicht kühlen oder einfrieren.
- Nachdem ein Trudhesa -Fläschchen geöffnet wurde, muss sie nach 8 Stunden weggeworfen werden.
Halten Sie Trudhesa und alle Medikamente außerhalb der Reichweite der Kinder.
Werfen Sie Trudhesa nicht in Feuer oder Verbrennungsanlagen, da der Kanister innerhalb des Geräts explodieren kann.
Allgemeine Informationen über den sicheren und effektiven Einsatz von Trudhesa.
Medikamente werden manchmal für andere Zwecke als die in einem Medikamentenhandbuch aufgeführten Zwecke verschrieben. Verwenden Sie Trudhesa nicht für eine Erkrankung, für die sie nicht verschrieben wurde. Geben Sie Trudhesa nicht an andere Menschen, auch wenn sie die gleichen Symptome haben, die Sie haben. Es kann ihnen schaden. Sie können Ihren Apotheker oder Gesundheitsdienstleister um Informationen über Trudhesa bitten, die für Angehörige der Gesundheitsberufe geschrieben wurden.
Was sind die Zutaten in Trudhesa?
Wirkstoff: Dihydroergotamin -Mesylat
Inaktive Zutaten: Koffeinkohlendioxid -Dextrose und Wasser. Der Nasenspray-Gerätskanister enthält Hydrofluoralkane-134A (HFA) -Treibstoff. Der Fläschchenstopper wird nicht mit Naturkautschuk -Latex hergestellt. Trudhesa ist eine Marke von Impel Neuropharma Inc.
Dieser Medikamentenführer wurde von der US -amerikanischen Food and Drug Administration zugelassen.
Anweisungen zur Verwendung
Trusta ™
(Roe-sa)
(Dihydroergotamin -Mesylat)
Nasenspray
Nur für den Nasengebrauch
Einführung
Lesen Sie diese Anweisungen zur Verwendung, bevor Sie Trudhesa verwenden, und jedes Mal, wenn Sie eine Rezept -Nachfüllung erhalten. Es kann neue Informationen geben.
Diese Informationen treten nicht mit Ihrem Gesundheitsdienstleister über Ihre Krankheit oder Behandlung ein. Sie und Ihr Gesundheitsdienstleister sollten über Trudhesa sprechen, wenn Sie mit der Einnahme und bei regelmäßigen Untersuchungen beginnen.
Es ist wichtig, diese Anweisungen genau zu befolgen, um die richtige Dosis zu erhalten. Kontaktieren Sie Ihren Gesundheitsdienstleister, wenn Sie Fragen zur Verwendung dieses Produkts haben.
 |
Nasenspray -Geräte -Teile
 |
Glasfläschchen
 |
Wichtige Informationen, die Sie kennen müssen, bevor Sie mit Trudhesa dosieren
- Nur für den Nasengebrauch.
- Führen Sie das Nasenspray -Gerät immer vor, bevor Sie die Fingergriffe und Glasfläschchen zusammen pumpen genau 4 mal
- Der Zweck des Priming besteht darin, das Medikament an die Sprühdüse zu bringen. Sie können während jeder Priming -Aktion Flüssigkeit oder Spray aus der Düse kommen oder nicht.
- Während des Primingmake richten Sie sicher die Sprühdüse von Ihrem Gesicht und alles, was Sie nicht mit dem Spray of Medicine in Kontakt kommen möchten.
- Eine vollständige Dosis beträgt 2 Sprays; 1 Spray in jedem Nasenloch.
- Nicht Nehmen Sie innerhalb eines Zeitraums von 24 Stunden mehr als 2 Dosen. Nicht Nehmen Sie in einem Zeitraum von 7 Tagen mehr als 3 Dosen ein.
- Halten Sie das Nasenspray -Gerät immer aufrecht im Priming und bei der Dosierung aufrecht.
- Das Schnüffeln während der Dosierung ist nicht notwendig. Wie man das Medikament weder verletzt noch weniger effektiv macht.
- Dieses Nasenspray-Gerätsprodukt ist eine einzelne Dosis (nur für eine vollständige Dosis) und sollte nach der Verwendung weggeworfen (weggeworfen) werden. Sie benötigen für jede Dosis ein neues Kit.
- Halten Sie das Produkt im Gehäuse bis zur Verwendung.
- Nachdem ein Trudhesa -Fläschchen eröffnet wurden, muss nach 8 Stunden weggeworfen werden.
- Nicht Öffnen Sie die Glasfläschchen und setzen Sie es der Luft aus, bis sie verwendet werden können.
- In Raumtemperatur in einem sauberen trockenen Bereich aufbewahren.
- Nicht Verwendung, wenn das Produkt beschädigt ist.
- Nicht Verwendung, wenn das Produkt abgelaufen ist.
- Jedes Glasfläschchen- und Nasenspray -Gerät kann nur 1 Zeit verwendet werden. Werfen Sie das gesamte Nasenspray -Gerät weg, nachdem Sie die Glasfläschchen nicht entfernen.
- Sie können eine weitere vollständige Dosis mindestens 1 Stunde nach Ihrer ersten Dosis einnehmen, wenn Ihre Symptome bestehen bleiben.
Trudhesa aufbewahren
- Lagern Sie Trudhesa bei Raumtemperatur zwischen 68 ° F und 77 ° F (20 ° C bis 25 ° C).
- Lagern Sie Trudhesa in der Originalverpackung in einem Reinigungsbereich von Hitze und Licht (Licht Abbildung a ).
- Halten Sie Trudhesa in der Originalverpackung, bis Sie zur Verwendung bereit sind.
- Nicht Trudhesa im Kühlschrankerat oder einfrieren.
- Halten Sie Trudhesa und alle Medikamente außerhalb der Reichweite der Kinder.
 |
Vorbereitung zur Dosis mit Trudhesa
Schritt 1: Versammeln und überprüfen Sie die Lieferungen
 |
 |
- Überprüfen Sie, ob Sie das richtige Medikament für Ihre Migräne verwenden (siehe Abbildung b ).
- Überprüfen Sie, ob Trudhesa nicht abgelaufen ist (EXP) (siehe Abbildung c ).
- Wenn abgelaufen ist, werfen Sie weg und holen Sie sich eine neue Glasfläschchen.
- Überprüfen Sie, ob die Abdeckung der Glasfläschchen und der blauen Plastik nicht beschädigt aussieht.
Schritt 2: Entfernen Sie die blaue Kunststoffabdeckung und graue Gummi -Stopper aus Glasfläschchen
 |
 |
 |
- Die blaue Kunststoffabdeckung aus der Glasfläschchen entfernen (siehe Abbildung d ).
- Verwenden Sie die blaue Kunststoffabdeckung, um die Metallfolie von dem grauen Gummi -Stopper in einer kreisförmigen Bewegung langsam ab (siehe Abbildung e ).

- Ziehen Sie den grauen Gummi -Stopfen nach oben und aus der Glasfläschchen ( Abbildung f Und Abbildung g ).
- Abdeckungsfolie und grauen Gummi -Stopper in den Müll wegwerfen (wegwerfen).
Schritt 3: Entfernen Sie die klare Kunststoffabdeckung vom Nasenspray -Gerät
- Halten Sie das Nasenspray -Gerät aufrecht.
- Ziehen Sie die klare Plastikabdeckung herunter und entfernen Sie sie aus der Nasenspray -Gerät ( Abbildung h ).
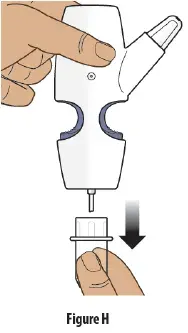
- Wirf die liebe Plastikabdeckung weg.
Schritt 4: Schrauben Sie die Glasfläschchen in das Nasenspray -Gerät ein
 |
 |
- Halten Sie das Nasenspray -Gerät aufrecht.
- Schieben Sie Glasfläschchen vorsichtig in den Boden des Nasensparay -Geräts (siehe Abbildung i ) und schrauben Sie es an, bis es wie in gezeigt befestigt ist Abbildung j .
Schritt 5: Führen Sie das Nasenspray -Gerät vor, indem Sie viermal mit Fingern und Daumen pumpen
 |
- Halten Sie das Nasenspray -Gerät halten aufrecht .
- Zeigen Sie die Sprühdüse von Ihrem Gesicht weg.
- Legen Sie Ihren Daumen auf den Boden des Glasfläschchens und legen Sie Ihren Zeiger (Index) und den Mittelfinger auf die Fingergriffe (siehe Abbildung k ).
- Pumpen Sie das Nasenspray -Gerät genau 4 mal.
- Um das Nasenspray -Gerät zu pumpen, drücken Sie den Fingergriff Dowm und die Glasfläschchen gleichzeitig nach oben. Dann veröffentlichen (siehe Abbildung k )
- Möglicherweise sehen Sie während des Priming etwas medizinisches Spray. Das ist normal. Es ist in Ordnung, wenn Sie bei den ersten Pumpen keine Medizin aussprühen sehen.
Wichtiger Tipp: Der Zweck des Primings besteht darin, das Medikament an die Sprühdüse zu bringen. Wenn Sie nicht vorbereiten, erhalten die Nasenspray -Geräte Ihre korrekte Medizin nicht.
Führen Sie das Nasenspray -Gerät immer vor dem Gebrauch durch Pumpen vor genau 4 mal.
Achten Sie beim Priming darauf, die Düse von Ihrem Gesicht zu zielen und alles, was Sie nicht mit dem Spray of Medicine in Kontakt kommen möchten.
Mit Trudhesa
Schritt 6: Positionieren Sie das Nasenspray -Gerät
 |
- Drehen Sie das Nasensprey-Gerät, so dass die Sprühdüse Ihnen zugewandt ist.
- Stellen Sie sicher, dass Ihr Kopf gerade ist und das Nasenspray -Gerät aufrecht ist.
- Fügen Sie die Sparay -Düse in Ihr erstes Nasenloch ein Abbildung l ).
Schritt 7: Sprühen Sie das erste Spray in 1 Nasenloch
- Drücken Sie den Fingergriff fest nach unten und drücken Sie die Glasfläschchen gleichzeitig nach oben, um das erste Spray zu liefern (siehe Abbildung m ).Then release.
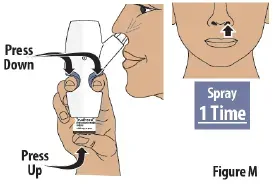
- Liefern Sie nur 1 Spray in dieses Nasenloch.
Schritt 8: Sprühen Sie das zweite Spray in ein anderes Nasenloch
- Bewegen Sie die Sprühdüse in Ihr anderes Nasenloch.
- Drücken Sie den Fingergriff fest nach unten und drücken Sie die Glasfläschchen gleichzeitig nach oben, um das zweite Spray zu liefern (siehe Abbildung n ).Then release.
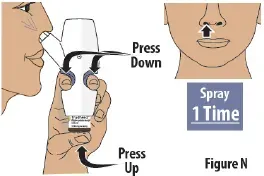
- Liefern Sie nur 1 Spray in dieses Nasenloch.
Wichtiger Tipp: Eine vollständige Dosis beträgt 2 Sprays; 1 Spray in jedem Nasenloch.
Wann sollte ich Garcinia Cambogia nehmen?
Nicht Nehmen Sie innerhalb eines Zeitraums von 24 Stunden mehr als 2 Dosen. Nicht Nehmen Sie in einem Zeitraum von 7 Tagen mehr als 3 Dosen ein.Please refer to the prescribing information for more information.
Das Schnüffeln während oder nach der Dosierung ist nicht notwendig. Wie man sich nicht verletzt oder das Medikament weniger wirksam macht.
Wichtige häufig gestellte Fragen (FAQs)
Frage: Kann ich Medikamente speichern, indem ich die 4 Pumpen in 'Schritt 5: das Nasenspray -Gerät' überspringen?
Antwort: Kein Überspringen der 4 Pumpen, um das Nasenspray -Gerät zu entfernen, kann dazu führen, dass Sie Ihre korrekte Dosis Medizin nicht erhalten.
Qestion: Als ich das Nasenspray -Gerät zum ersten Mal gepumpt habe, schien nichts zu bestimmen. Warum?
Antwort: Der Zweck des Primings besteht darin, das Medikament an die Spitze der Düse zu bringen. Auch wenn Sie auf Ihrer ersten oder zwei Pumpen möglicherweise nichts sehen oder hören, bewegt die Pumpaktion das Medikament vom Glasfläschchen durch das Innere des Nasenspray -Geräts und in die Düse. Sie sollten durch Ihren vierten Pumpenversuch ein Spray sehen.
Frage: Kann ich das Nasenspray -Gerät mit einer neuen Glasfläschchen wiederverwenden?
Antwort: Nicht das Nasenspray-Gerät dient nur zur einmaligen Verwendung und darf nach dem Schließen von 1 Spray in jedem Nasenloch weggeworfen werden. Dies liegt daran, dass das Gerät verstopfen kann. Den Dosierung des Glasfläschchens auf das Nasenspray-Gerät und das zusammengestellte Nasalspray-Gerät in den Müll wegwerfen. Recyceln Sie keinen Teil des Produkts.
Frage: Kann ich das Medikament verwenden, das für eine spätere Dosis in der Glasfläschchen bleibt?
Antwort: Noalth, obwohl es nrmal ist, dass einige Medikamente in der Glasfläschchen bleiben, die es nicht zur späteren Dosierung verwendet werden kann. Jede übrig gebliebene Medizin wird unwirksam.
Frage: Was passiert, wenn ich mehr als einmal im selben Nasenloch sparay?
Antwort: Eine vollständige und korrekte Dosis ist ein Spray in jedes Nasenloch. Nicht Dosis in Ihrem anderen Nasenloch, wenn Sie bereits zweimal in einem Nasenloch gesprüht haben.
Frage: Wie schnell kann ich eine weitere Dosis nehmen, wenn ich keine Erleichterung von meiner Migräne bekomme?
Antwort: Sie können eine weitere Dosis und mindestens 1 Stunde nach der ersten Dosis nehmen, wenn Ihre Symptome bestehen bleiben. Nicht Nehmen Sie innerhalb eines Zeitraums von 24 Stunden mehr als 2 Dosen. Nicht Nehmen Sie in einem Zeitraum von 7 Tagen mehr als 3 Dosen ein.Please refer to the prescribing information for more information.
Diese Verwendung wurden von der US -amerikanischen Food and Drug Administration genehmigt.




