Die Informationen Auf Dieser Website Stellen Keine Medizinische Beratung Dar. Wir Verkaufen Nichts. Die Richtigkeit Der Übersetzung Wird Nicht Garantiert. Haftungsausschluss
Kortikosteroide, topischKenalog Spray
Drogenzusammenfassung
Was ist Kenalog Spray?
Kenalog Spray (Triamcinolonacetonid) ist ein topisches Kortikosteroid, das für die Linderung des Juckreizes aufgrund von Hautreizungen angezeigt wird. Kenalog Spray ist als Generika .
Was sind Nebenwirkungen von Kenalog Spray?
Zu den häufigen Nebenwirkungen von Kenalogspray gehören das Verbrennen von Juckreiz und Trockenheit. Zu den schwerwiegenden Nebenwirkungen von Kenalog Spray gehören:
- Schwerer Hautausschlag
- Kurzatmigkeit
- Schwierigkeiten beim Schlucken und
- Hautinfektionen
Dosierung für Kenalog -Spray
Das Kenalog -Spray gibt es in zwei Größen, die eine Dose von 63 und 100 mg in Stärke von 0,147 mg pro Gramm haben. Anweisungen zur Verwendung der Sprühdose werden auf dem Etikett bereitgestellt. Kenalog -Spray kann auf einen beliebigen Bereich des Körpers aufgetragen werden, obwohl darauf geachtet werden sollte, dass die Augen bedeckt sind und dass das Einatmen des Sprays beim Sprühen über das Gesicht vermieden wird.
Welche Medikamentensubstanzen oder Nahrungsergänzungsmittel interagieren mit Kenalog Spray?
Kenalog Spray kann mit anderen Medikamenten interagieren. Sagen Sie Ihrem Arzt alle Medikamente und Nahrungsergänzungsmittel, die Sie verwenden.
Kenalog -Spray während der Schwangerschaft oder des Stillens
Es gibt keine angemessenen und gut kontrollierten Studien bei schwangeren Frauen zu teratogenen Wirkungen von topisch angewandten Kortikosteroiden wie Kenalog-Spray. Daher sollten topische Kortikosteroide während der Schwangerschaft nur dann verwendet werden, wenn der potenzielle Nutzen das potenzielle Risiko für den Fötus rechtfertigt. Topisch angewandte Kortikosteroide dürfen bei schwangeren Patienten in großen Mengen oder über längere Zeiträume nicht ausreichend angewendet werden. Es ist nicht bekannt, ob die Verwendung von Kenalog -Spray in Muttermilch nachweisbar ist. Es ist vorsichtig zu sein, wenn topische Kortikosteroide an eine stillende Frau verabreicht werden. Kenalog -Spray sollte bei Kindern vorsichtig angewendet werden, da ein größeres Verhältnis von Hautoberflächen zu Körpergewicht sie anfälliger für das Cushing -Syndrom der Nebennieren und die intrakranielle Hypertonie sind, die alle bei Kindern berichtet wurden, die topische Kortikosteroide erhalten.
Weitere Informationen
Unser Kenalog Spray Side Effects Drug Center bietet einen umfassenden Überblick über die verfügbaren Arzneimittelinformationen über die potenziellen Nebenwirkungen bei der Einnahme dieses Medikaments.
FDA -Drogeninformationen
- Drogenbeschreibung
- Indikationen
- Nebenwirkungen
- Warnungen
- Überdosis
- Klinische Pharmakologie
- Medikamentenhandbuch
Nur für Dermatologische Verwendung
Nicht für Augengebrauch
Beschreibung für Kenalog Spray
The topical corticosteroids constitute a class of primarily synthetic steroids used as anti-inflammatory and antipruritic agents. The steroids in this class include triamcinolone acetonide. Triamcinolone acetonide is designated chemically as 9-fluoro-11β 16α 17 21-tetrahydroxypregna-1 4-diene-3 20-dione cyclic 16 17-acetal with acetone. The structural formula is:
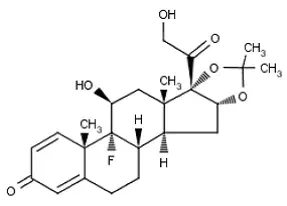 |
C 24 H 31 Fo 6
Eine Zwei-Sekunden-Anwendung, die einen Bereich ungefähr von der Größe der Hand abdeckt, liefert eine Menge Triamcinolonacetonid von nicht mehr als 0,2 mg. Nach dem Sprühen des nichtflüchtigen Fahrzeugs auf der Haut enthält ungefähr 0,2% Triamcinolonacetonid. Jedes Gramm Spray liefert 0,147 mg Triamcinolonacetonid in einem Fahrzeug von Isopropylpalmitatdehydrated Alkohol (NULL,3%) und Isobutan -Treibmittel.
Kommt Cholestyramin in Pillenform?
Verwendung für Kenalog Spray
Kenalog Spray (Triamcinolonacetonid Topical Aerosol USP) ist zur Linderung der entzündlichen und pruritischen Manifestationen von kortikosteroidresponsiven Dermatosen angezeigt.
Dosierung für Kenalog -Spray
Anweisungen zur Verwendung der Sprühdose werden auf dem Etikett bereitgestellt. Die Zubereitung kann auf einen beliebigen Bereich des Körpers aufgetragen werden, aber wenn sie über die Gesichtspflege gesprüht wird, sollte er feststellen, dass die Augen bedeckt sind und dass das Einatmen des Sprays vermieden wird.
Spray ist brennbar; Vermeiden Sie Wärmeflamme oder Rauchen, wenn Sie dieses Produkt verwenden.
Drei oder vier Anwendungen täglich von Kenalog Spray (Triamcinolon Acetonid Topical Aerosol) sind im Allgemeinen ausreichend.
Wie geliefert
Kenalog Spray (Triamcinolon Acetonid Topisches Aerosol USP)
63 g ( NDC 10631-093-62) Aerosol CAN.
100 g ( NDC 10631-093-07) Aerosol kann.
Lagerung und Handhabung
Bei Raumtemperatur aufbewahren; Vermeiden Sie übermäßige Hitze. Inhalt unter Druck; Nicht punktieren oder verbrennen. Außerhalb der Reichweite von Kindern.
Um vermutete unerwünschte Reaktionen zu melden, wenden Sie sich an die FDA unter 1-800-FDA-1088 oder www. FDA. Gehen Sie v/medwatch.
Ranbaxy Jacksonville FL 32257 USA. Überarbeitet Juli 2011
Nebenwirkungen für Kenalog Spray
The following local adverse reactions are reported infrequently with topical corticosteroids but may occur more frequently with the use of occlusive dressings (reactions are listed in an approximate decreasing order of occurrence): burning itching irritation dryness folliculitis hypertrichosis acneiform eruptions hypopigmentation perioral dermatitis allergic contact dermatitis maceration of the skin secondary infection skin atrophy Striae andmiliaria.
Wechselwirkungen mit Arzneimitteln für Kenalog -Spray
Keine Informationen zur Verfügung gestellt.
Nebenwirkungen von Phenazopyridin 200 mg
Warnungen für Kenalog Spray
Keine Informationen zur Verfügung gestellt.
Vorsichtsmaßnahmen für Kenalog Spray
Allgemein
Die systemische Absorption topischer Kortikosteroide hat bei einigen Patienten eine reversible hypothalamisch-hypophysen-Nebennieren-Achse-Unterdrückungsmanifestationen der Hyperglykämie und Glukosurie des Syndroms von Sprudeln hervorgebracht.
Zu den Bedingungen, die die systemische Absorption erweitern, gehören die Anwendung der stärkeren Steroide, die über große Oberflächen verwendet werden, und die Zugabe von Okklusivverbänden.
Daher sollten Patienten, die eine große Dosis eines wirksamen topischen Steroids erhalten, das auf eine große Oberfläche oder unter einem okklusiven Verband angewendet wird, regelmäßig bewertet werden, um eine HP -Achse -Unterdrückung unter Verwendung des freien Cortisol- und ACTH -Stimulationstests im Urin und zur Beeinträchtigung der thermischen Homöostase zu beeinträchtigen. Wenn eine HP -Achsenunterdrückung oder Erhöhung der Körpertemperatur auftritt, sollte ein Versuch unternommen werden, das Arzneimittel zurückzuziehen, um die Häufigkeit des Anwendungsfrequenz zu verringern, ein weniger starkes Steroid oder einen sequentiellen Ansatz zu verwenden.
Die Wiederherstellung von HP A -Achsenfunktion und thermische Homöostase sind im Allgemeinen schnell und abgeschlossen, wenn das Arzneimittel abgesetzt wird. Es können selten Anzeichen und Symptome des Steroidentzugs auftreten, die zusätzliche systemische Kortikosteroide erfordern.
Kinder können proportional größere Mengen topischer Kortikosteroide aufnehmen und somit anfälliger für systemische Toxizität sein (siehe Vorsichtsmaßnahmen pädiatrischer Gebrauch ).
Xanax -Pille Was macht es?
Wenn die Reizung topische Kortikosteroide entwickelt, sollte abgesetzt und eine angemessene Therapie eingeleitet werden.
In Gegenwart dermatologischer Infektionen sollte die Verwendung eines geeigneten antimykotischen oder antibakteriellen Mittel eingeleitet werden. Wenn eine günstige Reaktion nicht sofort auftritt, sollte das Kortikosteroid abgesetzt werden, bis die Infektion ausreichend kontrolliert wurde.
Labortests
Ein freier Cortisol -Test- und ACTH -Stimulationstest im Urin kann bei der Bewertung der HPA -Achsenunterdrückung hilfreich sein.
Karzinogenese -Mutagenese -Beeinträchtigung der Fruchtbarkeit
Langzeitstudien wurden nicht durchgeführt, um das krebserzeugende Potential oder die Auswirkung auf die Fruchtbarkeit topischer Kortikosteroide zu bewerten.
Studien zur Bestimmung der Mutagenität mit Prednisolon und Hydrocortison zeigten negative Ergebnisse.
Schwangerschaft: teratogene Wirkungen
Category C. Corticosteroids are generally teratogenic in laboratory animals when administered systemically at relatively low dosage levels. The more potent corticosteroids have been shown to be teratogenic after dermal application in laboratory animals. There are no adequate and well-controlled studies in pregnant women on teratogenic effects from topically applied corticosteroids. Therefore topical corticosteroids should be used during pregnancy only if the potential benefit justifies the potential risk to the fetus. Drugs of this class should not be used extensively on pregnant patients in large amounts or for prolonged periods of time.
Pflegemütter
Es ist nicht bekannt, ob die topische Verabreichung von Kortikosteroiden zu einer ausreichenden systemischen Absorption führen könnte, um nachweisbare Mengen in der Muttermilch zu erzeugen. Systemisch verabreichte Kortikosteroide werden in Mengen in der Muttermilch sekretiert, die wahrscheinlich keine schädliche Wirkung auf das Kind haben. Trotzdem ist Vorsicht geboten, wenn topische Kortikosteroide an eine stillende Frau verabreicht werden.
Pädiatrische Verwendung
Pädiatrische Patienten können eine stärkere Anfälligkeit für topische Kortikosteroid-induzierte HPA-Achseunterdrückung und das Cushing-Syndrom aufweisen als reife Patienten aufgrund eines größeren Verhältnisses von Hautoberflächen zu Körpergewicht zu Körpergewicht.
Die Unterdrückung von HPA -Achsen -Cushing -Syndrom und intrakranielle Hypertonie wurden bei Kindern berichtet, die topische Kortikosteroide erhalten. Manifestationen der Nebennierenunterdrückung bei Kindern umfassen eine lineare Verzögerung der Verzögerung der Gewichtszunahme niedriger Plasma -Cortisolspiegel und das Fehlen einer Reaktion auf ACTH -Stimulation. Manifestationen der intrakraniellen Hypertonie umfassen prall gefüllte Kopfschmerzen in Fontanellen und bilaterales Papillen.
Die Verabreichung topischer Kortikosteroide an Kinder sollte auf die geringste Menge beschränkt sein, die mit einem wirksamen therapeutischen Regime kompatibel ist. Die chronische Kortikosteroid -Therapie kann das Wachstum und die Entwicklung von Kindern beeinträchtigen.
Überdosierungsinformationen für Kenalog Spray
Topisch angewandte Kortikosteroide können in ausreichenden Mengen absorbiert werden, um systemische Effekte zu erzeugen (siehe VORSICHTSMASSNAHMEN Allgemein ).
Kontraindikationen für Kenalog Spray
Topische Kortikosteroide sind bei Patienten mit Überempfindlichkeit gegenüber den Bestandteilen der Präparate kontraindiziert.
Klinische Pharmakologie for Kenalog Spray
Topische Kortikosteroide teilen entzündungshemmende antipruritische und vasokonstriktive Wirkungen.
Der Mechanismus der entzündungshemmenden Aktivität der topischen Kortikosteroide ist unklar. Verschiedene Labormethoden, einschließlich Vasokonstriktor -Assays, werden verwendet, um Potenzen und/oder klinische Wirksamkeit der topischen Kortikosteroide zu vergleichen und vorherzusagen. Es gibt einige Hinweise darauf, dass eine erkennbare Korrelation zwischen vasokonstriktorischer Wirksamkeit und therapeutischer Wirksamkeit beim Menschen besteht.
Nebenwirkungen von Vitamin C und Lysin
Pharmakokinetik
Das Ausmaß der perkutanen Absorption topischer Kortikosteroide wird durch viele Faktoren bestimmt, einschließlich des Fahrzeugs, die Integrität der epidermalen Barriere und die Verwendung von okklusiven Verbänden.
Topische Kortikosteroide können von einer normalen intakten Haut absorbiert werden. Entzündung und/oder andere Krankheitsprozesse in der Haut erhöhen die perkutane Absorption.
Einmal durch die Haut absorbiert werden topische Kortikosteroide durch pharmakokinetische Wege behandelt, ähnlich wie systemisch verabreichte Kortikosteroide. Kortikosteroide sind in unterschiedlichem Maße an Plasmaproteine gebunden. Kortikosteroide werden hauptsächlich in der Leber metabolisiert und dann von den Nieren ausgeschieden. Einige der topischen Kortikosteroide und ihre Metaboliten werden ebenfalls in die ausgeschieden sogar .
Patienteninformationen für Kenalog Spray
Patienten, die Kenalog Spray verwenden, sollten die folgenden Informationen und Anweisungen erhalten:
- Dieses Medikament soll wie vom Arzt angewiesen werden. Es ist nur für den externen Gebrauch; Vermeiden Sie den Kontakt mit den Augen und Einatmen des Sprays.
- Den Patienten sollte empfohlen werden, dieses Medikament nicht für eine andere Störung zu verwenden, die es verschrieben wurde.
- Der behandelte Hautbereich sollte nicht gebunden oder anderweitig bedeckt oder verpackt werden, um nicht vom Arzt zu geleitet.
- Patienten sollten Anzeichen lokaler Nebenwirkungen melden.
- Eltern von pädiatrischen Patienten sollten empfohlen werden, bei einem Kind, das im Windelbereich behandelt wird, keine strengen Windeln oder Plastikhosen zu verwenden, da diese Kleidungsstücke okklusive Verbände darstellen können.
- Verwenden Sie kein Kenalog -Spray auf den Unterarmen oder Leistenbereichen, es sei denn, Ihr Arzt.
- Wenn innerhalb von 2 Wochen keine Verbesserung erfolgt, wenden Sie sich an Ihren Arzt.
- Verwenden Sie keine anderen kortikosteroidhaltigen Produkte, während Sie Kenalog Spray verwenden, ohne dass Sie Ihren Arzt zuerst konsultieren.
- Kenalog Spray ist entflammbar. Vermeiden Sie Wärmeflammen oder Rauchen beim Auftragen von Kenalog -Spray.
