Die Informationen Auf Dieser Website Stellen Keine Medizinische Beratung Dar. Wir Verkaufen Nichts. Die Richtigkeit Der Übersetzung Wird Nicht Garantiert. Haftungsausschluss
AminoglykosideArikayce
Drogenzusammenfassung
Was ist Arikayce?
Arikayce (Amikacin -Liposomen -Inhalationssuspension) ist ein Aminoglykosid antibakteriell angezeigt bei Erwachsenen mit begrenzten oder keine alternativen Behandlungsoptionen zur Behandlung von Lungenerkrankungen von Mycobacterium avium Complex (MAC) als Teil eines kombinierten antibakteriellen Arzneimittelregimes bei Patienten, die nach mindestens 6 aufeinanderfolgenden Monaten einer mehreren Hintergrundregimetherapie keine negative Sputum -Kulturen erreichen. Dieses Medikament ist für die Verwendung in einer begrenzten und spezifischen Population von Patienten angezeigt.
Was sind Nebenwirkungen von Arikayce?
Arikayce
- Nesselsucht
- Schwierigkeiten beim Atmen
- Schwellung Ihrer Gesichtslippen Zunge oder Hals
- Husten (insbesondere im ersten Monat der Verwendung des Medikaments)
- Probleme beim Sprechen
- in den Ohren klingeln
- Änderungen im Hörverhältnis
- Schwindel
- Spinngefühl
- Benommenheit
- Brust -Enge
- Keuchen
- Kurzatmigkeit
- Blut husten
- wenig oder gar kein Urinieren
- Schwellung in deinen Füßen oder Knöcheln und
- Müdigkeit
Holen Sie sich sofort medizinische Hilfe, wenn Sie eines der oben aufgeführten Symptome haben.
Zu den häufigen Nebenwirkungen von Arikayce gehören:
- Schwierigkeiten zu sprechen
- Husten
- Bronchospasmus
- Blut husten
- Schäden am Innenohr
- Reizung der oberen Atemwege
- Muskuloskelettschmerzen
- Ermüdung
- Schwäche
- Verschlechterung der zugrunde liegenden Lungenerkrankung
- Durchfall und
- Brechreiz
Suchen Sie medizinische Versorgung oder rufen Sie auf einmal 911 an, wenn Sie die folgenden schwerwiegenden Nebenwirkungen haben:
- Schwerwiegende Augensymptome wie plötzlicher Sehverlust verschwommenes Sehen Tunnel Sehschmerzen oder Schwellungen oder Halos in der Umgebung des Lichts;
- Schwerwiegende Herzsymptome wie schnelle unregelmäßige oder pochende Herzschläge; Flattern in deiner Brust; Kurzatmigkeit; und plötzliche Schwindel -Benommenheit oder ohnmächtig;
- Starke Kopfschmerzen Verwirrung verwirrt Spracharm oder Bein Schwäche Schwierigkeiten beim Verlust der Koordination unstabil sehr steifes Muskeln hoher Fieber problemlos Schwitzen oder Zittern.
Dieses Dokument enthält nicht alle möglichen Nebenwirkungen und andere können auftreten. Wenden Sie sich an Ihren Arzt nach zusätzlichen Informationen zu Nebenwirkungen.
Dosierung für Arikayce
Die empfohlene Dosierung von Arikayce bei Erwachsenen ist einst täglich orale Inhalation des Inhalts von einem 590 mg/8,4 ml Arikayce -Fläschchen. Verwenden Sie Arikayce -Fläschchen nur mit dem Lamira Nebulizer -System.
Welche Drogensubstanzen oder Nahrungsergänzungsmittel interagieren mit Arikayce?
Arikayce kann mit Ethacryninsäure -Furosemid interagieren Harnstoff intravenöses Mannitol oder Medikamente im Zusammenhang mit Neurotoxizitätnephrotoxizität und Ototoxizität. Sagen Sie Ihrem Arzt alle Medikamente und Nahrungsergänzungsmittel, die Sie verwenden.
Arikayce während der Schwangerschaft oder des Stillens
Sagen Sie Ihrem Arzt, wenn Sie schwanger sind oder vorhaben, schwanger zu werden, bevor Sie Arikayce verwenden. Es kann einem Fötus schaden. Es ist nicht bekannt, ob Arikayce in die Muttermilch übergeht. Wenden Sie sich vor dem Stillen an Ihren Arzt.
Weitere Informationen
Unsere Arikayce (Amikacin -Liposomen -Inhalationssuspension) für die orale Inhalationsseitungsnutzungsdrogenzentrum bietet eine umfassende Übersicht über verfügbare Arzneimittelinformationen über die potenziellen Nebenwirkungen bei der Einnahme dieses Medikaments.
FDA -Drogeninformationen
- Drogenbeschreibung
- Indikationen
- Dosierung
- Nebenwirkungen
- Warnungen
- Überdosis
- Klinische Pharmakologie
- Medikamentenhandbuch
WARNUNG
Risiko einer erhöhten nachteiligen respiratorischen Reaktionen
Arikayce war mit einem erhöhten Risiko für nachteilige Reaktionen der Atemwegs in Verbindung gebracht, einschließlich Überempfindlichkeitspneumonitis Hämoptysis Bronchospasmus -Exazerbation der zugrunde liegenden Lungenerkrankungen, die in einigen Fällen zu Krankenhauseinweisungen geführt haben [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ].
Beschreibung für Arikayce
Der Wirkstoff in Arikayce (Amikacin -Liposomen -Inhalationssuspension) ist Amikacinsulfat USP Ein Aminoglycosid -Antibakteriell. Sein chemischer Name ist D-Streptamin O -3-Amino-3-Desoxy-α-Dglucopyranosyl- (1 → 6)- O -[6-Amino-6-Desoxy-α-D-Glucopyranosyl- (1 → 4)]- N 1 -(4-Amino-2-Hydroxy-1oxobutyl) -2-Desoxy- ( S )- Sulfat (1: 2) Salz mit einer chemischen Formel von C 22 H 43 N 5 O 13 • 2H 2 ALSO 4 mit einem Molekulargewicht von 781,76. Seine strukturelle Formel ist:
 |
Arikayce ist eine weiße milchige Suspension, die aus Amikacinsulfat besteht, die in Liposomen eingekapselt ist, und wird in einer Einheit-Dosis 10 ml klares Glasfläschchen mit Amikacin 590 mg/8,4 ml (gleichwertig zur Amikacin-Sulfat 623 mg/8,4 ml) als sterile äusale Liposomale für die Oralierung des Liposomals für Oralierung geliefert. Arikayce besteht aus Amikacinsulfat, die in Liposomen in einer gezielten Konzentration von 70 mg Amikacin/ml mit einem pH -Bereich von 6,1 bis 7,1 und Lipid zu Amikacin -Gewichtsverhältnis im Bereich von 0,60 bis 0,79 eingekapselt sind. Die inaktiven Inhaltsstoffe sind Cholesterin -Dipalmitoylphosphatidylcholin (DPPC) Natriumchlorid -Natriumhydroxid (zur pH -Einstellung) und Wasser zur Injektion.
Arikayce wird nur unter Verwendung eines Lamira -Verneblersystems verabreicht [siehe Dosierung und Verwaltung ]. Like all other nebulized treatments the amount delivered to the lungs will depend upon patient factoders. Under stUndardized in vitro Testen pro USP <1601> Atemmuster für Erwachsene (500 ml Gezeitenvolumen 15 Atemzüge pro Minute und Inhalation: Ausatmenverhältnis von 1: 1) Die mittlere gelieferte Dosis aus dem Mundstück betrug ungefähr 312 mg Amikacinsulfat (53% der Kennzeichnung). Der mediane aerodynamische Durchmesser (MMAD) der nebulisierten Aerosoltröpfchen beträgt etwa 4,7 & mgr; m (NULL,1 - 5,3 μm), wie unter Verwendung der NGI -Methode der nächsten Generation (NGI) ermittelt. Ein Prozentsatz des Amikacin im Liposom wird durch den Nebelisationsprozess freigesetzt. Daher liefert die Nebel von Arikayce eine Kombination aus freiem und liposomalem Amikacin.
Verwendung für Arikayce
Bevölkerung begrenzte Bevölkerung: Arikayce ® ist bei Erwachsenen mit begrenzten oder keine alternativen Behandlungsoptionen für die Behandlung von angegeben Mycobacterium avium Komplexe (MAC) Lungenerkrankung als Teil eines kombinierten antibakteriellen Arzneimittelregimes bei Patienten, die nach mindestens 6 aufeinanderfolgenden Monaten einer Multire -Hintergrund -Therapie keine negativen Sputumkulturen erreichen. Da nur begrenzte klinische Sicherheits- und Effektivitätsdaten für Arikayce sind, sind derzeit Reserve Arikayce zur Verwendung bei Erwachsenen mit begrenzten oder keine alternativen Behandlungsoptionen verfügbar. Dieses Medikament ist für die Verwendung in einer begrenzten und spezifischen Population von Patienten angezeigt.
Diese Anzeige wird unter beschleunigter Zulassung auf der Grundlage der Erreichung der Sputum -Kulturumwandlung (definiert als drei aufeinanderfolgende negative monatliche Sputumkulturen) bis Monat 6 genehmigt. Der klinische Nutzen wurde noch nicht festgestellt [siehe Klinische Studien ]. Continued approval foder this indication may be contingent upon verification Und description of clinical benefit in confirmatodery trials.
Gebrauchsbeschränkung
Arikayce wurde nur bei Patienten mit refraktärer MAC -Lungenerkrankung untersucht, die als Patienten definiert wurden, die nach mindestens 6 aufeinanderfolgenden Monaten einer Multidrug -Hintergrund -Therapie keine negativen Sputumkulturen erreichten. Die Verwendung von Arikayce wird für Patienten mit nicht refraktärer MAC-Lungenerkrankung nicht empfohlen.
Dosierung für Arikayce
Wichtige Verwaltungsanweisungen
Arikayce ist nur für den oralen Inhalationsgebrauch gedacht. Durch Nebelversion nur mit dem Lamira durchführen ® Verneblersystem. In den Anweisungen für die vollständige Verwaltungsinformationen zur Verwendung von Arikayce mit dem Lamira Nebulizer -System finden Sie auf der Verwendung.
Weisen Sie die Patienten unter Verwendung eines Bronchodilators („Reliever“) an, zuerst den Bronchodilatator nach der Bronchodilatatorblätterblatt zu verwenden, um Informationen vor der Verwendung von Arikayce zu verwenden.
Vorbehandlung mit kurzwirkenden selektiven Beta-2 WARNUNGS AND VORSICHTSMASSNAHMEN ].
Empfohlene Dosierung
Die empfohlene Dosierung von Arikayce bei Erwachsenen ist einst täglich ein Einatmen des Inhalts von einem 590 mg/8,4 ml Arikayce -Fläschchen (590 mg Amikacin) unter Verwendung des Lamira -Nebulizer -Systems [siehe Klinische Studien ].
Verwalten Sie Arikayce nur mit dem Lamira -Nebulizer -System. Arikayce sollte vor dem Gebrauch bei Raumtemperatur sein. Vor dem Öffnen der Arikayce -Fläschchenbrunnen mindestens 10 bis 15 Sekunden lang, bis der Inhalt einheitlich und gut gemischt erscheint. Das Arikayce -Fläschchen wird geöffnet, indem die Plastikoberseite des Fläschchens aufdreht und dann nach unten zieht, um den Metallring zu lockern. Der Metallring und der Gummi -Stopper sollten sorgfältig entfernt werden. Der Inhalt des Arikayce -Fläschchens kann dann in das Medikamentenreservoir des Verneblers eingetaucht werden.
Wenn eine tägliche Dosis Arikayce verpasst wird, verwalten Sie die nächste Dosis am nächsten Tag. Verdoppeln Sie die Dosis nicht, um die verpasste Dosis auszugleichen.
Wie geliefert
Dosierung Foderms And Strengths
Arikayce wird als sterile weiße milchige wässrige Liposomensuspension für orale Inhalation in einem mit Amikacin 590 mg/8,4 ml enthaltenden Glas (gleichwertig zu Amikacinsulfat 623 mg/8,4 ml) geliefert.
Arikayce (Amikacin-Liposomen-Inhalationssuspension) 590 mg/8,4 ml werden in einer sterilen Dosis 10-ml-Glasfläschchen geliefert. Das Produkt wird als 28-Völker-Kit ausgegeben.
Jeder Karton enthält eine 28-tägige Versorgung mit Medikamenten (28 Fläschchen). Zusätzlich zu den Arikayce -Fläschchen im Karton sind One Lamira -Vernebler -Mobilteil und vier Lamira -Aerosolköpfe bereitgestellt.
NDC 71558-590-28
Das Lamira Nebulizer -System enthält einen Controller, ein Ersatz -Aerosolkopf, ein Ersatzmobilkabel und Zubehör.
Lagerung und Handhabung
Lagern Sie Arikayce Fläschchen, die bei 2 ° C bis 8 ° C bis 46 ° F bis zum Ablauf des Fläschchens (36 ° F bis 46 ° F) gekühlt werden. NICHT einfrieren . Einmal abgelaufen, entsorgen Sie ein ungenutzliches Medikament.
Arikayce can be stodered at room temperature up to 25°C (77°F) foder up to 4 weeks. Once at room temperature any unused drug must be discarded at the end of 4 weeks.
Hergestellt für: InsMed Incorporated 700 US Highway 202/206 Bridgewater NJ 08807-1704. Überarbeitet: Februar 2023
Nebenwirkungen für Arikayce
Die folgenden klinisch signifikanten Nebenwirkungen werden in anderen Kennzeichnungsabschnitten ausführlicher beschrieben:
- Überempfindlichkeit Pneumonitis [siehe Boxwarnung Und WARNUNGS AND VORSICHTSMASSNAHMEN ]
- Hämoptysis [siehe Boxwarnung Und WARNUNGS AND VORSICHTSMASSNAHMEN ]
- Bronchospasmus [siehe Boxwarnung Und WARNUNGS AND VORSICHTSMASSNAHMEN ]
- Verschlechterung der zugrunde liegenden Lungenerkrankung [siehe Boxwarnung Und WARNUNGS AND VORSICHTSMASSNAHMEN ]
- Anaphylaxie und Überempfindlichkeitsreaktionen [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ]
- Ototoxizität [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ]
- Nephrotoxizität [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ]
- Neuromuskuläre Blockade [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ]
Klinische Studien Erfahrung
Da klinische Studien unter sehr unterschiedlichen Bedingungen durchgeführt werden, die in den klinischen Studien eines Arzneimittels beobachtet werden, können in den klinischen Studien eines anderen Arzneimittels nicht direkt mit den Raten verglichen werden und spiegeln möglicherweise nicht die in der Praxis beobachteten Raten wider.
Überblick über klinische Studien zur Sicherheitsbewertung
Innerhalb der refraktären klinischen NTM -Programme 404 Patienten, die an drei klinischen Studien teilnahmen, wurden mit Arikayce in der Dosis von 590 mg/Tag behandelt (mediane Dauer der Exposition gegenüber Arikayce betrug 236,5 Tage).
Versuch 1 (NCT Mycobacterium avium Komplexe (MAC) Lungenerkrankung. Die Patienten wurden entweder auf 8 Monate Arikayce plus ein Hintergrundregime (n = 223) oder ein Hintergrundregime allein (n = 112) randomisiert.
Versuch 2 (NCT
Versuch 3 (NCT Mykobakterium . Die Patienten wurden entweder auf Arikayce plus Hintergrundregime (n = 44) oder ein inhaliertes verdünntes leeres Liposom -Placebo -Plus -Hintergrundregime (n = 45) 84 Tage lang randomisiert.
In allen klinischen Studien mit Patienten mit und ohne refraktärer NTM -Lungeninfektion wurden 818 Patienten mehrerer Arikayce -Dosen ausgesetzt.
Nebenwirkungen, die zum Absetzen der Behandlung führen
In den drei NTM -Studien gab es eine höhere Inzidenz eines vorzeitigen Abbruchs von Arikayce. In Versuch 1 34,5% Arikayce vorzeitig eingestellt; Die meisten waren auf unerwünschte Reaktionen (NULL,8%) und auf den Rückzug nach Subjekt (NULL,9%) zurückzuführen. Im Vergleichsarm stellten 10,7% der Probanden ihr Hintergrundregime mit 0,9% aufgrund von Nebenwirkungen und 5,4% aufgrund des Entzuges durch Subjekt ein. In Studie 2 (die Ein-Arm-Verlängerung der Studie 1) 37,8% der Patienten, die mit Arikayce begannen, stellten vorzeitig mit 24,4% ab, die aufgrund nachteiliger Reaktionen eingestellt wurden. In Versuch 3 traten alle 9 (NULL,5%) vorzeitige Diskontinuationen in den Arikayce-Plus-Hintergrundregime-behandelten Patienten auf, und es gab keine vorzeitigen Diskontinuationen im Placebo-Plus-Hintergrund-Regime-Arm.
Schwerwiegende Nebenwirkungen in den Versuchen 1 und 3
In Studie 1 19,7% der mit Arikayce plus Hintergrundregime behandelten Patienten berichteten SAR im Vergleich zu 16,1% der mit dem Hintergrundregime behandelten Patienten allein. Darüber hinaus gab es bei 41 Patienten (NULL,4%), die mit Arikayce plus Hintergrundregime behandelt wurden, 80 Krankenhausaufenthalte, im Vergleich zu 29 Krankenhausaufenthalten, bei 15 Patienten (NULL,4%), die allein mit dem Hintergrundregime behandelt wurden, 80 Krankenhausaufenthalte, die mit Arikayce plus Hintergrundregime behandelt wurden, die mit dem Hintergrundregime behandelt wurden, 80 Krankenhausaufenthalte. Die häufigsten SARs und Gründe für den Krankenhausaufenthalt im Arikayce Plus -Hintergrundregime -Arm waren mit der Verschlechterung der zugrunde liegenden Lungenerkrankungen und der Infektionen der unteren Atemwege wie Lungenentzündung zusammen. In Studie 3 18,2% der mit Arikayce plus Hintergrundregime behandelten Patienten berichteten SARs im Vergleich zu 8,9% der mit dem Hintergrundregime behandelten Patienten plus inhalatives Placebo.
Häufige Nebenwirkungen
Die Inzidenz von unerwünschten Reaktionen in Versuch 1 ist in Tabelle 1 angezeigt. Nur die negativen Reaktionen mit einer Rate von mindestens 5% in der Arikayce -plus -Hintergrund -Regime -Gruppe und größer als die Gruppe des Hintergrundregimes sind gezeigt.
Tabelle 1: Nebenwirkungen bei ≥ 5% der mit Arikayce behandelten MAC-Patienten und häufiger als Hintergrundregime in Studie 1 allein als Hintergrundregime
| Nebenwirkungen | Arikayce plus Background Regimen (N = 223) N (%) | Hintergrundregime allein (N = 112) N (%) |
| Dysphonie a | 106 (48) | 2 (2) |
| Husten b | 88 (40) | 19 (17) |
| Bronchospasmus c | 64 (29) | 12 (11) |
| Hämoptysis | 41 (18) | 15 (13) |
| Muskuloskelettschmerzen d | 40 (18) | 10 (9) |
| Reizung der oberen Atemwege e | 39 (18) | 2 (2) |
| Elitude f | 38 (17) | 11 (10) |
| Müdigkeit und Asthenie | 36 (16) | 11 (10) |
| Verschlimmerung der zugrunde liegenden Lungenerkrankung g | 34 (15) | 11 (10) |
| Durchfall | 28 (13) | 5 (5) |
| Brechreiz | 26 (12) | 4 (4) |
| Kopfschmerzen | 22 (10) | 5 (5) |
| Lungenentzündung h | 20 (9) | 10 (9) |
| Pyrexie | 17 (8) | 5 (5) |
| Gewicht nahm ab | 16 (7) | 1 (1) |
| Erbrechen i | 15 (7) | 4 (4) |
| Ausschlag j | 14 (6) | 1 (1) |
| Veränderung im Sputum k | 13 (6) | 1 (1) |
| Brustbeschwerden | 12 (5) | 3 (3) |
| a Beinhaltet Aphonie und Dysphonie b Beinhaltet Husten produktives Husten und Upper Airway -Husten -Syndrom c Beinhaltet Asthma -Bronchialhyperreaktivität Bronchospasmus Dyspnoe Dyspnoe Anstrengungslängerer Expirationsrachen -Enge und Keuchen d Beinhaltet Rückenschmerzen Arthralgie Myalgie Schmerz/Körperschmerz Muskelkrampf und Muskuloskelettschmerzen e Beinhaltet oropharyngeale Schmerzen Oropharyngeales Beschwerden Rachen Irritation Pharyngealer Erythem obere Atemwe f Beinhaltet Taubheit Taubheit Neurosensorte Taubheit Unilateral Schwindel Hypoacusis Presyncop g Beinhaltet die COPD -Infektionswiederung der COPD -Infektionserbation der Bronchiektasie h Beinhaltet atypische Pneumonien -Empyeminfektion Pleura -Erguss Untererattrakt -Infektion Lungeninfektion Lungeninfektion Pseudomonas pneumonia pneumonia Aspiration pneumonia pseudomonas pseudomonas Infektion und Atemtraktinfektion i Beinhaltet Erbrechen und postentussives Erbrechen j Beinhaltet Euthut für makulo-papuläre Drogenausbrüche und Urtikaria k Beinhaltet erhöhten Sputum -Sputum -eitrigen und Sputumverfärbungen |
Ausgewählte unerwünschte Arzneimittelreaktionen, die in auftraten <5% of patients Und at higher frequency in Arikayce-treated patients in Trial 1 are presented in Table 2.
Tabelle 2: Ausgewählte Nebenwirkungen in <5% of Arikayce-treated MAC Patients Und Modere Frequent than Hintergrundregime allein in Trial 1
| Nebenwirkungen | Arikayce plus Background Regimen N = 223 N (%) | Hintergrundregime allein N = 112 N (%) |
| Angst a | 10 (5) | 0 (0) |
| Orale Pilzinfektion b | 9 (4) | 2 (2) |
| Bronchitis | 8 (4) | 3 (3) |
| Dysgeusie | 7 (3) | 0 (0) |
| Überempfindlichkeit Pneumonitis c | 7 (3) | 0 (0) |
| Trockener Mund | 6 (3) | 0 (0) |
| Epistaxis | 6 (3) | 1 (1) |
| Atemversagen d | 6 (3) | 2 (2) |
| Pneumothorax e | 5 (2) | 1 (1) |
| Die Trainingstoleranz nahm ab | 3 (1) | 0 (0) |
| Gleichgewichtsstörung | 3 (1) | 0 (0) |
| Neuromuskuläre Störung f | 2 (1) | 0 (0) |
| a Beinhaltet Angst und Angststörung b Beinhaltet orale Candidiasis und orale Pilzinfektion c Beinhaltet eine interstitielle Lungenerkrankung und Pneumonitis mit allergischer Alveolitis d Beinhaltet akutes Atemversagen und Atemversagen e Beinhaltet pneumothorax pneumothorax spontane und pneumomediastinum f Beinhaltet Muskelschwäche und periphere Neuropathie |
Siehe Tabelle 1 und Tabelle 2 für die Inzidenzrate der Überempfindlichkeitspneumonitis Bronchospasmus -Husten -Dyphonia -Exazerbation der zugrunde liegenden Hämoptyse -Ototoxizität der oberen Atemwege und neuromuskuläre Erkrankungen [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ].
Nachmarkterfahrung
Die folgenden nachteiligen Reaktionen wurden aus der Überwachung nach dem Stempeln identifiziert. Da diese nachteiligen Reaktionen freiwillig aus einer Population unbekannter Größe gemeldet werden, kann genaue Häufigkeitsschätzungen nicht vorgenommen werden, und es kann nicht eine kausale Beziehung zur Arzneimittelexposition hergestellt werden.
Störungen des Immunsystems: Überempfindlichkeit Anaphylaxie [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ]
Wechselwirkungen mit Arzneimitteln für Arikayce
Medikamente mit neurotoxischem nephrotoxischem oder ototoxischem Potenzial
Vermeiden Sie die gleichzeitige Anwendung von Arikayce mit Medikamenten, die mit Neurotoxizitätsnephrotoxizität und Ototoxizität verbunden sind.
Ethacryninsäure Furosemid Harnstoff oder Mannitol
Einige Diuretika können die Aminoglykosidtoxizität verbessern, indem die Aminoglykosidkonzentrationen in Serum und Gewebe verändert werden. Vermeiden Sie die gleichzeitige Verwendung von Arikayce mit Ethacrynsäure -Furosemid Harnstoff oder intravenöses Mannitol.
Warnungen für Arikayce
Eingeschlossen als Teil der 'VORSICHTSMASSNAHMEN' Abschnitt
Vorsichtsmaßnahmen für Arikayce
Überempfindlichkeit Pneumonitis
Überempfindlichkeit Pneumonitis has been repoderted with the use of Arikayce in the clinical trials. Überempfindlichkeit Pneumonitis (repoderted as allergic alveolitis pneumonitis interstitial lung disease allergic reaction to Arikayce) was repoderted at a higher frequency in patients treated with Arikayce plus a background regimen (3.1%) compared to patients treated with a background regimen alone (0%). Most patients with hypersensitivity pneumonitis discontinued treatment with Arikayce Und received treatment with coderticosteroids [see Nebenwirkungen ]. If hypersensitivity pneumonitis occurs discontinue Arikayce Und manage the patient as medically appropriate.
Hämoptysis
Hämoptysis has been repoderted with the use of Arikayce in the clinical trials. Hämoptysis was repoderted at a higher frequency in patients treated with Arikayce plus a background regimen (18.4%) compared to patients treated with a background regimen alone (13.4%) [see Nebenwirkungen ]. If hemoptysis occurs manage the patients as medically appropriate.
Bronchospasmus
Bronchospasmus has been repoderted with the use of Arikayce in the clinical trials. Bronchospasmus (repoderted as asthma bronchial hyperreactivity Bronchospasmus dyspnea dyspnea exertional prolonged expiration throat tightness Keuchen) was repoderted at a higher frequency in patients treated with Arikayce plus a background regimen (28.7%) compared to patients treated with a background regimen alone (10.7%) [see Nebenwirkungen ]. If Bronchospasmus occurs during the use of Arikayce treat the patients as medically appropriate.
Verschlimmerung der zugrunde liegenden Lungenerkrankung
Exazerbationen der zugrunde liegenden Lungenerkrankung wurden unter Verwendung von Arikayce in den klinischen Studien berichtet. Exazerbationen der zugrunde liegenden Lungenerkrankung (als chronisch obstruktive Lungenerkrankung infizieren, die die Exazerbation einer chronisch obstruktiven Lungenerkrankung infektiös infiziert, wurde bei Patienten, die mit Arikayce und einem mit Arikaya behandelten Patienten behandelt wurden, bei Patienten, die mit Arikayce behandelt wurden, mit Arikayce und einem Hintergrundschema (NULL,2%) (NULL,2%) im Vergleich zu Patienten, die mit Hintergrundregimes behandelt wurden (9.8%). Nebenwirkungen ]. If exacerbations of underlying pulmonary disease occur during the use of Arikayce treat the patients as medically appropriate.
Anaphylaxie und Überempfindlichkeitsreaktionen
Bei Patienten, die Arikayce einnehmen, wurden schwerwiegende und potenziell lebensbedrohliche Überempfindlichkeitsreaktionen einschließlich Anaphylaxie berichtet. Signs and symptoms include acute onset of skin and mucosal tissue hypersensitivity reactions (hives itching flushing swollen lips/tongue/uvula) respiratory difficulty (shortness of breath wheezing stridor cough) gastrointestinal symptoms (nausea vomiting diarrhea crampy abdominal pain) and cardiovascular signs and symptoms of anaphylaxis (Tachykardie Niedriger Blutdruck Synkope Inkontinenz Schwindel). Vor der Therapie mit Arikayce wird ein Evaluieren für frühere Überempfindlichkeitsreaktionen auf Aminoglykoside eingeleitet. Wenn eine Anaphylaxie oder eine Überempfindlichkeitsreaktion auftritt, stellen Sie Arikayce ein und setzen Sie angemessene unterstützende Maßnahmen ein.
Elitude
Elitude With Use Of Arikayce
Elitude has been repoderted with the use of Arikayce in the clinical trials. Elitude (including deafness Schwindel presyncope tinnitus Und vertigo) were repoderted with a higher frequency in patients treated with Arikayce plus a background regimen (17%) compared to patients treated with background regimen alone (9.8%). This was primarily driven by tinnitus (8.1% in Arikayce plus background regimen vs. 0.9% in the background regimen alone arm) Und Schwindel (6.3% in Arikayce plus background regimen vs. 2.7% in the background regimen alone arm) [see Nebenwirkungen ].
Überwachen Sie Patienten mit bekannten oder vermuteten auditorischen oder vestibulären Dysfunktion während der Behandlung mit Arikayce genau. Wenn Ototoxizität auftritt, verwalten Sie den Patienten als medizinisch angemessen, einschließlich des potenziellen Abbruchs von Arikayce.
Ototoxizitätsrisiko aufgrund von mitochondrialen DNA -Varianten
Fälle von Ototoxizität mit Aminoglykosiden wurden bei Patienten mit bestimmten Varianten im mitochondrial codierten 12S-rRNA-Gen (MT-RNR1), insbesondere der M.1555a> G-Variante, beobachtet. Bei einigen Patienten trat die Ototoxizität auch dann auf, wenn ihre Aminoglycosid -Serumspiegel innerhalb des empfohlenen Bereichs lagen. Mitochondriale DNA -Varianten sind in weniger als 1% der allgemeinen US -Bevölkerung vorhanden, und der Anteil der Variantenträger, die möglicherweise Ototoxizität entwickeln können, sowie der Schweregrad der Ototoxizität ist unbekannt. Im Falle einer bekannten mütterlichen Anamnese der Ototoxizität aufgrund von Aminoglykosidgebrauch oder einer bekannten mitochondrialen DNA -Variante im Patienten werden andere alternative Behandlungen als Aminoglykoside in Betracht gezogen, es sei denn, das erhöhte Risiko eines dauerhaften Hörverlusts wird durch die Schwere der Infektion und das Fehlen sicherer und wirksamer alternativer Therapien überwogen.
Nephrotoxizität
Nephrotoxizität was observed during the clinical trials of Arikayce in patients with MAC lung disease but not at a higher frequency than the background regimen alone [see Nebenwirkungen ]. Nephrotoxizität has been associated with the aminoglycosides. Close monitodering of patients with known oder suspected renal dysfunction may be needed when prescribing Arikayce.
Neuromuskuläre Blockade
Patienten mit neuromuskulären Erkrankungen wurden nicht in klinische Arikayce -Studien eingeschlossen. Aminoglykoside können die Muskelschwäche verschlimmern, indem sie die Freisetzung von Acetylcholin an neuromuskulären Verbindungen blockiert. Überwachen Sie Patienten mit bekannten oder vermuteten neuromuskulären Erkrankungen wie Myasthenia gravis genau. Wenn eine neuromuskuläre Blockade auftritt, kann sie durch die Verabreichung von Kalziumsalzen umgekehrt werden, kann jedoch eine mechanische Atemgeldhilfe erforderlich sein.
Embryo-Fetal-Toxizität
Aminoglykoside können einen fetalen Schaden verursachen, wenn sie einer schwangeren Frau verabreicht werden. Aminoglykoside einschließlich Arikayce können mit einer totalen irreversiblen bilateralen angeborenen Taubheit bei pädiatrischen Patienten in Verbindung gebracht werden in der Gebärmutter . Patienten, die Arikayce während der Schwangerschaft verwenden oder während der Einnahme von Arikayce schwanger werden Verwendung in bestimmten Populationen ].
Patientenberatungsinformationen
Raten Sie dem Patienten, die von der FDA zugelassene Patientenkennzeichnung zu lesen ( Medikamentenhandbuch Und Patient Instructions foder Use ).
Wichtige Anweisungen zur Verwaltung von Arikayce
Weisen Sie die Patienten an, die Anweisungen zur Verwendung zu lesen, bevor Sie mit Arikayce beginnen. Weisen Sie die Patienten an, nur die Lamira zu verwenden ® Verneblersystem zur Verwaltung von Arikayce. Beraten Sie den Patienten oder die Pflegekraft, das Lamira -Verneblersystem nicht mit anderen Medikamenten zu verwenden.
Überempfindlichkeit Pneumonitis And Bronchospasmus (Difficulty Breathing)
Raten Sie den Patienten, ihren Gesundheitsdienstleister zu informieren, wenn sie nach der Verabreichung von Arikayce Kurzatmigkeit oder Keuchen haben. Beratung von Patienten mit einer reaktiven Atemwegserkrankung Asthma oder Bronchospasmus zur Verabreichung von Arikayce nach der Verwendung eines kurzwirkenden Bronchodilators [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ].
Hämoptysis Or Husten
Raten Sie den Patienten, ihren Gesundheitsdienstleister zu informieren, wenn sie Blut abhusten oder episodische Husten entweder während oder nach der Arikayce -Verabreichung erleben, insbesondere im ersten Monat nach Beginn von Arikayce [siehe WARNUNGS AND VORSICHTSMASSNAHMEN Und Nebenwirkungen ].
Verschlechterungen zugrunde liegender Lungenerkrankungen
Raten Sie den Patienten, ihren Gesundheitsdienstleister zu informieren, wenn sie nach Beginn von Arikayce eine verschlechterte Verschlechterung ihrer Lungenerkrankung haben [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ].
Dysphonie Or Difficulty Speaking
Raten Sie den Patienten, ihren Gesundheitsdienstleister zu informieren, wenn sie Schwierigkeiten haben, zu sprechen. Mit Arikayce wurde Schwierigkeiten beim Sprechen oder Sprechverlust gemeldet [siehe Nebenwirkungen ].
Anaphylaxie und Überempfindlichkeitsreaktionen
Beraten Sie Patienten und Betreuer, dass schwerwiegende und potenziell lebensbedrohliche Überempfindlichkeitsreaktionen, die eine sofortige Behandlung erfordern, auftreten können. Raten Sie dem Patienten, Arikayce einzustellen und sofortige medizinische Hilfe zu suchen, wenn Anzeichen oder Symptome einer Überempfindlichkeitsreaktion auftreten [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ].
Elitude (Ringing In The Ears)
Raten Sie den Patienten, ihren Gesundheitsdienstleister zu informieren, wenn sie in den Ohren schwindelig oder im Hörveränderungen klingeln, da Arikayce mit Hörverlust in Verbindung gebracht wurde [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ].
Raten Sie dem Patienten, keine schweren Maschinerie zu betreiben oder gefährliche Aktivitäten durchzuführen, während Arikayce durch das Lamira -Nebulizer -System einatmet, da Arikayce Symptome wie Schwindel oder Atemsymptome verursachen kann.
Nephrotoxizität Or Kidney Damage
Raten Sie den Patienten, ihren Gesundheitsdienstleister zu informieren, wenn sie Nierenprobleme haben, weil bei Aminoglycosids Nierenschäden gemeldet wurden [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ]. Neuromuskuläre Blockade Advise patients to infoderm their healthcare provider of known neuromuscular disease (e.g. myasthenia gravis) [see WARNUNGS AND VORSICHTSMASSNAHMEN ].
Embryo-Fetal-Toxizität
Beraten Sie schwangere Frauen, dass Aminoglycoside einschließlich Arikayce bei der Schwangerschaft eine irreversible angeborene Taubheit verursachen können [siehe WARNUNGS AND VORSICHTSMASSNAHMEN Und Verwendung in bestimmten Populationen ].
Nichtklinische Toxikologie
Karzinogenese -Mutagenese -Beeinträchtigung der Fruchtbarkeit
In einer 2-Jahres-Inhalationskarzinogenitätsstudie wurden Ratten für 15-25 50-70 oder 155170 Minuten pro Tag für 96-104 Wochen ausgesetzt. Diese lieferten ungefähre inhalierte Dosen von 5 15 und 45 mg/kg/Tag. Plattenepithelkarzinom wurde in der Lunge von 2 von 120 Ratten beobachtet, die die höchste getestete Dosis verabreichten. Die maximalen Amikacinspiegel im Serum im stationären Zustand betrugen bei niedrigen Mid- bzw. hohen Dosen ungefähr 1,3 2,8 bzw. 7,6 mcg · hr/ml im Vergleich zu 23,5 mcg · Stunde/ml (NULL,0 bis 46,5 mcg · h/ml), die beim Menschen gemessen wurden. Die Plattenepithelkarzinome können das Ergebnis einer hohen Lungenlast von Partikeln aus Arikayce in der Rattenlunge sein. Die Relevanz der Lungentumorbefunde in Bezug auf Menschen, die Arikayce erhalten, ist unbekannt.
Bei einer Batterie von wurden keine Hinweise auf die Mutagenität oder Genotoxizität beobachtet in vitro Und vergeblich Genotoxizitätsstudien mit einer liposomenkapselten Amikacin-Formulierung ähnlich wie Arikayce ( in vitro Mikrobieller Mutagenese -Test in vitro Maus -Lymphom -Mutationstest in vitro Chromosomal -Aberrationsstudie und eine vergeblich Mikronukleus -Studie bei Ratten).
Mit Arikayce wurden keine Fruchtbarkeitsstudien durchgeführt. Die intraperitoneale Verabreichung von Amikacin gegenüber männlichen und weiblichen Ratten bei Dosen von bis zu 200 mg/kg/Tag vor der Paarung bis zum 7. Tag der Schwangerschaft war nicht mit einer Beeinträchtigung der Fruchtbarkeit oder nachteiligen Auswirkungen auf die frühe embryonale Entwicklung verbunden.
Verwendung in bestimmten Populationen
Schwangerschaft
Risikozusammenfassung
Es gibt keine Daten über die Verwendung von Arikayce bei schwangeren Frauen, um ein drogenassoziiertes Risiko für schwere Geburtsfehler zu bewerten, Fehlgeburt oder nachteilige Ergebnisse der Mutter oder des Fötus. Obwohl die systemische Absorption von Amikacin nach oralem Inhalation voraussichtlich gering ist [siehe Klinische Pharmakologie ] systemische Exposition gegenüber Aminoglykosid -Antibakterienmedikamenten einschließlich Arikayce kann mit einer totalen irreversiblen bilateralen angeborenen Taubheit in Verbindung gebracht werden, wenn sie schwangeren Frauen verabreicht werden [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ]. Advise pregnant women of the potential risk to a fetus.
Tiere -reproduktive toxikologische Studien wurden nicht mit inhaliertem Amikacin durchgeführt. Die subkutane Verabreichung von Amikacin an schwangere Ratten (bis zu 100 mg/kg/Tag) und Mäuse (bis zu 400 mg/kg/Tag) während der Organogenese war nicht mit fetalen Fehlbildungen verbunden. Die Ototoxizität wurde in den Nachkommen in Tierstudien nicht angemessen bewertet.
Das geschätzte Hintergrundrisiko von schweren Geburtsfehlern und Fehlgeburten für die angegebenen Populationen ist unbekannt. Alle Schwangerschaften haben ein Hintergrundrisiko für einen Verlust von Geburtsfehlern oder andere nachteilige Ergebnisse. In der US-allgemeinen Bevölkerung beträgt das geschätzte Hintergrundrisiko für größere Geburtsfehler und eine Fehlgeburt bei klinisch anerkannten Schwangerschaften 2-4% bzw. 15 bis 20%.
Daten
Tierdaten
Mit Arikayce oder nicht-liposomalem Amikacin, das durch Inhalation verabreicht wurde, wurden keine tierischen Toxikologiestudien durchgeführt.
Amikacin wurde schwangeren Ratten (Schwangerschaftstage 8-14) und Mäusen (Schwangerschaftstage 7-13) in Dosen von 25 100 oder 400 mg/kg subkutan verabreicht, um die Entwicklungstoxizität zu bewerten. Diese Dosen verursachten bei Mäusen keine fetalen viszeralen oder skelettalen Missbildungen. Die hohe Dosis war bei Ratten (Nephrotoxizität und Mortalität wurden beobachtet) übermäßig toxisch, die die Bewertung der Nachkommen bei dieser Dosis ausschließen. Fetale Missbildungen wurden bei der niedrigen oder mittleren Dosis bei Ratten nicht beobachtet. Postnatale Entwicklung der Ratten und Mäuse, die diesen Dosen von Amikacin ausgesetzt sind in der Gebärmutter unterschied sich nicht signifikant von der Kontrolle.
Elitude was not adequately evaluated in offspring in animal developmental toxicology studies.
Stillzeit
Risikozusammenfassung
Es gibt keine Informationen über das Vorhandensein von Arikayce in der Muttermilch die Auswirkungen auf das gestillte Kind oder die Auswirkungen auf die Milchproduktion nach Verabreichung von Arikayce durch Inhalation. Obwohl begrenzte veröffentlichte Daten zu anderen Verabreichungswegen von Amikacin darauf hinweisen Klinische Pharmakologie ]. The developmental Und health benefits of breastfeeding should be considered along with the mother’s clinical need foder Arikayce Und any potential adverse effects on the breastfed child from Arikayce oder from the underlying maternal condition.
Pädiatrische Verwendung
Sicherheit und Wirksamkeit von Arikayce bei pädiatrischen Patienten unter 18 Jahren wurden nicht festgestellt.
Geriatrische Verwendung
In den klinischen NTM -Studien der Gesamtzahl der Patienten, die Arikayce 208 (NULL,5%) erhielten, betrugen ≥ 65 Jahre und 59 (NULL,6%) ≥ 75 Jahre. Es wurden keine allgemeinen Unterschiede in der Sicherheit und Wirksamkeit zwischen älteren Probanden und jüngeren Probanden beobachtet. Da ältere Patienten eher eine verringerte Nierenfunktion haben, kann es nützlich sein, die Nierenfunktion zu überwachen [siehe WARNUNGS AND VORSICHTSMASSNAHMEN ].
Hepatische Beeinträchtigung
Arikayce has not been studied in patients with hepatic impairment. No dose adjustments based on hepatic impairment are required since amikacin is not hepatically metabolized [see Klinische Pharmakologie ].
Wofür wird Calciumgluconat verwendet?
Nierenbehinderung
Arikayce has not been studied in patients with renal impairment. Given the low systemic exposure to amikacin following administration of Arikayce clinically relevant accumulation of amikacin is unlikely to occur in patients with renal impairment. However renal function should be monitodered in patients with known oder suspected renal impairment including elderly patients with potential age-related decreases in renal function [see WARNUNGS AND VORSICHTSMASSNAHMEN Geriatrische Verwendung ].
Überdosierungsinformationen für Arikayce
Nebenwirkungen, die speziell mit einer Überdosierung von Arikayce verbunden sind, wurden nicht identifiziert. Eine akute Toxizität sollte mit sofortigem Entzug von Arikayce behandelt werden, und die Basistests der Nierenfunktion sollten durchgeführt werden.
Die Hämodialyse kann hilfreich sein, um Amikacin aus dem Körper zu entfernen.
In allen Fällen von Verdacht auf Überdosierung sollten Ärzte das regionale Poison Control Center für eine wirksame Behandlung wenden. Bei einer Überdosierung sollte die Möglichkeit von Arzneimittelwechselwirkungen mit Veränderungen der Arzneimitteldisposition berücksichtigt werden.
Kontraindikationen für Arikayce
Arikayce is contraindicated in patients with a known hypersensitivity to any aminoglycoside.
Klinische Pharmakologie foder Arikayce
Wirkungsmechanismus
Arikayce is an antibakteriell drug [see Mikrobiologie ].
Pharmakodynamik
Arikayce exposure-response relationships Und the time course of pharmacodynamic response are unknown.
Pharmakokinetik
Sputumkonzentrationen
Nach einem einmaligen Einatmen von 590 mg Arikayce in Mycobacterium avium Komplexe (MAC) Patienten Sputum-Konzentrationen nach 1 bis 4 Stunden nach der Intens waren 1720 884 bzw. 1300 mcg/g bei 1 3 bzw. 6 Monaten. Eine hohe Variabilität der Amikacin -Konzentrationen wurde beobachtet (CV%> 100%). Nach 48 bis 72 Stunden nach der Inhalation nahmen die Sputumkonzentrationen der Amikacin auf ungefähr 5% derjenigen nach 1 bis 4 Stunden nach der Inhalation auf ungefähr 5% ab.
Serumkonzentrationen
Nach 3 Monaten einmal täglicher Einatmen von 590 mg Arikayce bei MAC-Patienten betrug das mittlere Serum AUC0-24 23,5 mcg*hr/ml (Bereich: 8,0 bis 46,5 mcg*hr/ml; n = 12) und der mittlere Serum Cmax 2,8 mcg/ml (Bereich: 1,0 bis 4,4 μg/ml; n = 12). Die maximalen Cmax und AUC0-24 lagen unter dem mittleren Cmax von ungefähr 76 mcg/ml und AUC0-24 von 154 mcg*hr/ml, die für die intravenöse Verabreichung von Amikacinsulfat zur Injektion bei der zugelassenen Dosierung von 15 mg/kg einmal täglich bei gesunden Erwachsenen beobachtet wurden.
Absorption
Die Bioverfügbarkeit von Arikayce wird voraussichtlich hauptsächlich von individuellen Unterschieden in der Effizienz der Zerstäuber und der Atemwegspathologie unterscheiden.
Verteilung
Die Proteinbindung von Amikacin im Serum beträgt ≤ 10%.
Beseitigung
Nach Einatmen von Arikayce bei MAC-Patienten lag die scheinbare Serum-Halbwertszeit von Amikacin zwischen etwa 5,9 bis 19,5 Stunden.
Stoffwechsel
Amikacin wird keinen nennenswerten Stoffwechsel unterzogen.
Ausscheidung
Das systemisch absorbierte Amikacin nach der Verabreichung von Arikayce wird hauptsächlich durch glomeruläre Filtration beseitigt. Durchschnittlich 7,42% (zwischen 0,72 und 22,60%; n = 14) der gesamten Arikayce -Dosis wurde im Urin als unveränderter Arzneimittel im Vergleich zu 94% nach intravenöser Verabreichung von Amikacinsulfat zur Injektion ausgeschieden. Unabsorbiertes Amikacin nach der Inhalation von Arikayce wird wahrscheinlich hauptsächlich durch zelluläre Umsatz und Expektorierung beseitigt.
Arzneimittelinteraktionsstudien
Mit Arikayce wurden keine Studien zur Interaktion mit klinischen Arzneimitteln durchgeführt [siehe Wechselwirkungen mit Arzneimitteln ].
Mikrobiologie
Wirkungsmechanismus
Amikacin ist ein polykationisches semisynthetisches bakterizides Aminoglycosid. Amikacin tritt in die Bakterienzelle ein, indem er an negativ geladene Komponenten der Bakterienzellwand bindet, wodurch die Gesamtarchitektur der Zellwand stört. Der primäre Wirkmechanismus ist die Störung und Hemmung der Proteinsynthese in den Zielbakterien durch Bindung an die ribosomale 30S -Untereinheit.
Widerstand
Der Mechanismus der Resistenz gegen Amikacin in Mykobakterien wurde mit Mutationen im RRS -Gen der 16S -rRNA in Verbindung gebracht. In klinischen Studien, die MAC -Isolate, die ein Amikacin -Mikrofon von> 64 mcg/ml entwickeln, nach dem Ausgangswert in einem höheren Anteil der mit Arikayce behandelten Probanden beobachtet wurden [siehe Klinische Studien ].
Wechselwirkung mit anderen antimikrobiellen
Es gab nein in vitro signal for antagonism between amikacin and other antimicrobials against MAC based on fractional inhibitory concentration (FIC) and macrophage survival assays. In select instances some degree of synergy between amikacin and other agents has been observed as for example synergy between aminoglycosides including amikacin and the beta-lactam class has been documented.
Tiertoxikologie Andor Pharmakologie
Um Informationen über die chronische Dosierung von Arikayce für eine andere Tierart zu erhalten, wurde bei Hunden eine 9-monatige Inhalationstudie durchgeführt. Schaum alveoläre Makrophagen, die mit der Clearance des inhalierten Produkts assoziiert waren, waren bei dosisbedingter Inzidenz und Schweregrad vorhanden, aber nicht mit Entzündungsgewebe-Hyperplasie oder dem Vorhandensein von pränemoplastischen oder neoplastischen Veränderungen verbunden. Hunde wurden Arikayce bis zu 90 Minuten pro Tag ausgesetzt, inhalierten Amikacin -Dosen von ca. 5 10 und 30 mg/kg/Tag.
Klinische Studien
Versuch 1 (NCT Mycobacterium avium Komplexe (MAC) Lungenerkrankung, wie durch mindestens 2 Sputumkulturergebnisse bestätigt. Die Patienten hatten eine refraktäre MAC -Lungenerkrankung, wenn sie nach einer Mindestdauer von 6 aufeinanderfolgenden Monaten der Hintergrundregimetherapie, die entweder laufend oder nicht mehr als 12 Monate vor dem Screening -Besuch angehalten oder angehalten wurden, keine negativen Sputumkulturen erreicht haben. Die Patienten wurden entweder auf Arikayce plus ein Hintergrundregime oder ein Hintergrundregime allein. Der Ersatzendpunkt für die Beurteilung der Wirksamkeit beruhte auf der Erreichung der Kulturumwandlung (3 aufeinanderfolgende monatliche negative Sputumkulturen) bis Monat 6. Das Datum der Umwandlung wurde als Datum des ersten der drei negativen monatlichen Kulturen definiert, die bis zum 4 -jährigen Monat erreicht wurden. insgesamt 12 Monate nach der ersten negativen Sputumkultur.
Insgesamt 336 Patienten wurden randomisiert (Arikayce plus Hintergrundregime n = 224; Hintergrundregime allein n = 112) (ITT -Population) mit einem Durchschnittsalter von 64,7 Jahren, und in der Studie gab es einen höheren Prozentsatz an Frauen (NULL,3%) als Männer (NULL,7%). Zum Zeitpunkt der Einschreibung der 336 Probanden in der ITT-Population 302 (NULL,9%) befanden sich entweder auf einem Richtlinien-basierten Regime für MAC- oder Off-Richtlinien-basierte Therapie für MAC für weniger als 3 Monate, während 34 (NULL,1%) 3 bis 12 Monate vor der Anmeldung nicht behandelt wurden. Bei Screening wurden die Patienten durch den Raucherstatus (aktueller Raucher oder nicht) geschichtet und danach, ob die Patienten mindestens 3 Monate lang behandelt wurden oder nicht behandelt wurden. Die meisten Patienten beim Screening waren keine aktuellen Raucher (NULL,3%) und hatten eine zugrunde liegende Bronchiektasie (NULL,5%). Zu Studienbeginn befanden sich 329 Patienten auf einem Multidrug -Hintergrundregime, das ein Makrolid (NULL,3%) ein Rifamycin (NULL,3%) oder Ethambutol (NULL,4%) umfasste. Insgesamt 55,6% der Probanden erhielten ein Triple-Drogen-Hintergrundregime, das aus einem Makrolid A Rifamycin und Ethambutol bestand.
Der Anteil der Patienten, die die Kulturumwandlung (3 aufeinanderfolgende monatliche negative Sputumkulturen) bis zum 6. Monat erreichten, war signifikant (P. <0.0001) greater foder Arikayce plus background regimen (65/224 29.0%) compared to background regimen alone (10/112 8.9%). Of those receiving Arikayce plus background regimen 18.3% (41/224) achieved culture conversion by Month 6 Und sustained sputum culture conversion (defined as consecutive negative sputum cultures with no positive culture on solid media oder no modere than 2 consecutive positive cultures on liquid media following culture conversion) foder up to 12 months of treatment after the first culture that defined culture conversion compared to 2.7% (3/112) of patients receiving background regimen alone (p <0.0001). At 3 months after the completion of treatment 16.1% (36/224) of patients who had received Arikayce plus background regimen maintained durable culture conversion compared to 0% of patients who had received background regimen alone (p <0.0001).
Kumulativer Anteil der Probanden, die Kulturumwandlung erreichen, die im ersten Monat der Umwandlung der Bevölkerung (ITT) (ITT) gezeigt wird
 |
In Studie 1 23/224 (NULL,3%) der Patienten hatten MAC -Isolate, die ein MIC von> 64 mcg/ml entwickelten, während er mit Arikayce behandelt wurde. In der Hintergrundregime allein hatten Arm 4/112 (NULL,6%) der Patienten Mac -Isolate, die Amikacin -Mikrofon von> 64 mcg/ml entwickelten.
Zusätzliche Endpunkte zur Beurteilung des klinischen Nutzens von Arikayce beispielsweise ändern sich beispielsweise in sechsminütigem Walk-Testentfernung, und der Fragebogen des Saint George's Respiratory zeigte den klinischen Nutzen bis zum 6. Monat nicht.
Patienteninformationen für Arikayce
Arikayce
(Ar 'i kase)
Bevölkerung begrenzte Bevölkerung
(Amikacin -Liposomen -Inhalationssuspension) für den oralen Inhalationsgebrauch
Wichtig: Nur für orale Inhalation.
Was sind die wichtigsten Informationen, die ich über Arikayce wissen sollte?
Arikayce can cause serious side effects including:
- Allergische Entzündung der Lunge: Diese Atemprobleme können Symptome einer allergischen Entzündung der Lunge sein und oft mit:
- Fieber
- Keuchen
- Hustening
- Kurzatmigkeit
- schnelles Atmen
- Hustening up of blood (hemoptysis): Hustening up blood is a serious Und common side effect of Arikayce.
- Schwere Atemprobleme: Schwere Atemprobleme können Symptome von Bronchospasmus sein. Bronchospasmus ist eine ernsthafte und gemeinsame Nebenwirkung von Arikayce. Zu den Bronchospasmus -Symptomen gehören:
- Kurzatmigkeit
- schwierige oder mühsame Atmung
- Keuchen
- Hustening oder Brust -Enge
- Verschlechterung chronisch obstruktiver Lungenerkrankungen (COPD): Dies ist eine schwerwiegende und gemeinsame Nebenwirkung von Arikayce.
- Ernsthafte allergische Reaktionen: Schwerwiegende allergische Reaktionen, die zum Tod führen können, sind Menschen, die Arikayce einnehmen, passiert. Hören Sie sofort auf, Arikayce zu nehmen, und holen Sie sich die medizinische Helfer für Notfall, wenn Sie die folgenden Symptome einer schwerwiegenden allergischen Reaktion haben:
- Nesselsucht
- Laute hohe
- Schnelle Herzfrequenzatmung (Stridor)
- Juckreiz
- Husten
- sich hellköpfig fühlen
- Rötung oder Erröten von
- Brechreiz
- fühle mich schwach in der Haut (spülen)
- geschwollene Lippen Zunge oder
- Erbrechen
- Kontrollverlust des Darms oder Blase (Inkontinenz)
- Probleme beim Atmen oder
- Durchfall
- Schwindel Keuchen
- Kurzatmigkeit
- Fühlen Sie Krämpfe in Ihrem Magenbereich
Bei der Verwendung von Arikayce können diese Nebenwirkungen so schwerwiegend werden, dass die Behandlung in einem Krankenhaus erforderlich ist.
Rufen Sie Ihren Gesundheitsdienstleister an oder erhalten Sie sofort medizinische Hilfe, wenn Sie haben eine dieser schwerwiegenden Nebenwirkungen, während Sie Arikayce einnehmen. Ihr Gesundheitsdienstleister kann Sie auffordern, Arikayce für einen kurzen Zeitraum nicht mehr zu verwenden oder Arikayce vollständig zu verwenden.
Was ist Arikayce?
Arikayce is a prescription medicine used to treat adults with refractodery (difficult to treat) Mycobacterium avium Komplexe (MAC) Lungenerkrankung als Teil eines kombinierten antibakteriellen Medikamentenbehandlungsplans (Regime).
Es ist nicht bekannt, ob Arikayce bei Kindern unter 18 Jahren sicher und wirksam ist. Dieses Produkt wurde von der FDA unter Verwendung des begrenzten Bevölkerungswegs zugelassen.
Dies bedeutet, dass die FDA dieses Medikament für eine begrenzte und bestimmte Patientenpopulation zugelassen hat und Studien zum Arzneimittel möglicherweise nur fokussierte Fragen zu ihrer Sicherheit und Wirksamkeit beantwortet haben.
Verwenden Sie Arikayce nicht, wenn Sie:
- sind allergisch gegen jedes Aminoglykosid oder einen der Zutaten in Arikayce. Sehen Was sind die Zutaten in Arikayce? Am Ende dieser Broschüre für eine vollständige Liste von Zutaten in Arikayce.
Bevor Sie Arikayce verwenden, teilen Sie Ihrem Gesundheitsdienstleister alle Ihre medizinischen Erkrankungen mit, einschließlich, wenn Sie:
- haben Asthma chronisch obstruktive Lungenerkrankung (COPD) Atemnot oder Keuchen (Bronchospasmus).
- Mist wurde gesagt, dass Sie eine schlechte Lungenfunktion haben.
- Hörprobleme (einschließlich Geräusche in Ihren Ohren wie Klingeln oder Zischen) Hörverlust oder Ihre Mutter hatte nach der Einnahme eines Aminoglykosids Hörprobleme.
- Es wurde gesagt, dass Sie bestimmte Genvarianten (eine Veränderung des Gens) im Zusammenhang mit der Hören von Anomalien, die von Ihrer Mutter geerbt wurden, zusammenhängen.
- Schwindel oder Sinn für den Raum drehen.
- Nierenprobleme haben.
- haben neuromuskuläre Erkrankungen wie Myasthenia gravis.
- are pregnant or plan to become pregnant. It is not known if ARIKAYCE can harm your unborn baby. ARIKAYCE is in a class of medicines that may be connected with complete deafness in babies at birth. The deafness affects both ears and cannot be changed.
- stillen oder planen zu stillen. Es ist nicht bekannt, ob die Medizin in Arikayce in Ihre Muttermilch übergeht und ob es Ihrem Baby schaden kann. Sprechen Sie mit Ihrem Gesundheitsdienstleister darüber, wie Sie Ihr Baby während der Behandlung mit Arikayce am besten ernähren können.
Teilen Sie Ihrem Gesundheitsdienstleister über alle Medikamente, die Sie einnehmen, mit verschreibungspflichtige Arzneimittel und über die Counter-Medikamente Vitamine und Kräuterpräparate.
Wie soll ich Arikayce verwenden?
- Lesen Sie die Schritt-für-Schritt-Anweisungen für die Verwendung von Arikayce am Ende des Medikamentenhandbuchs und die vollständigen Anweisungen zur Verwendung in Ihrem Kit. Die Verwendung des Herstellers enthält vollständige Informationen zum Zusammenstellen (Montage). Vorbereiten Sie die Verwendung von sauber und desinfizieren Sie Ihr Lamira ® Verneblersystem.
- Nicht Verwenden Sie Arikayce, es sei denn, Sie verstehen die angegebenen Anweisungen. Wenn Sie Fragen haben, sprechen Sie mit Ihrem Gesundheitsdienstleister oder rufen Sie die Unterstützung von Arikares unter 1-833-Arikare (1-833-274-5273) an.
- Verwenden Sie Arikayce genau so, wie Ihr Gesundheitsdienstleister Ihnen sagt, dass Sie es verwenden sollen. Verwenden Sie Arikayce nicht öfter als für Sie vorgeschrieben.
- Verwenden Sie nur Arikayce mit dem Lamira Nebulizer -System.
- Atmen Sie jede tägliche Dosis Arikayce 1 Zeit jeden Tag durch das Lamira -Vernebler -Mobilteil ein. Verwenden Sie nicht mehr als 1 Fläschchen von Arikayce an einem Tag.
- Nicht use Arikayce after the expiration date on the vial. If you foderget to take your daily dose of Arikayce take your next dose at your usual time the next day.
- Nicht Verdoppeln Sie die Dosis, um die verpasste Dosis auszugleichen.
- Nicht Hören Sie auf, Arikayce oder andere Medikamente zur Behandlung Ihrer MAC -Lungenerkrankung zu verwenden, es sei denn, dies soll dies von Ihrem Gesundheitsdienstleister tun.
- Wenn Sie zu viel Arikayce verwenden, rufen Sie Ihren Gesundheitsdienstleister an oder gehen Sie sofort in die nächste Notaufnahme.
Was sind die möglichen Nebenwirkungen von Arikayce?
Arikayce may cause serious side effects including:
- Sehen Sie, was die wichtigsten Informationen über Arikayce sind?
- Hörverlust oder Klingeln in den Ohren (Ototoxizität) . Ototoxizität ist eine schwerwiegende und gemeinsame Nebenwirkung von Arikayce. Sagen Sie Ihrem Gesundheitsdienstleister sofort, wenn Sie Hörverlust haben oder Geräusche in Ihren Ohren wie Klingeln oder Zischen hören. Sagen Sie Ihrem Gesundheitsdienstleister, wenn Sie Probleme mit Gleichgewicht oder Schwindel (Schwindel) haben.
- Verschlechterung von Nierenproblemen (Nephrotoxizität). Arikayce is in a class of medicines which may cause wodersening kidney problems. Your healthcare provider may do a blood test to check how well your kidneys are woderking during your treatment with Arikayce.
- Verschlechterung der Muskelschwäche (neuromuskuläre Blockade). Arikayce is in a class of medicines which can cause muscle Schwäche to get woderse in people who already have problems with muscle Schwäche (myasthenia gravis).
Die häufigsten Nebenwirkungen von Arikayce sind:
- Änderungen in Ihrer Stimme und
- Halsschmerzen
- Muskelschmerzen Heiserkeit (Dysphonie)
- Durchfall
- Brechreiz
- Müdigkeit (Ermüdung)
- Fieber
- Erbrechen
- Kopfschmerzen
- vermindertes Gewicht
- Erhöhter Sputum
- Ausschlag
- Brustbeschwerden
- Husten during oder after a dose of Arikayce especially in the first month after starting treatment.
Dies sind nicht alle möglichen Nebenwirkungen von Arikayce.
Schwangerschaft bei den Depo -Schusssymptomen
Rufen Sie Ihren Arzt oder Apotheker an, um medizinische Beratung zu Nebenwirkungen zu erhalten. Sie können die FDA bei 1-800-FDA-1088 Nebenwirkungen melden
Wie soll ich Arikayce aufbewahren?
- Lagern Sie die zwischen 36 ° F bis 46 ° C bis 8 ° C (2 ° C bis 8 ° C) bis zum Ablaufdatum am Fläschchen. NICHT einfrieren.
- Nachdem Arikayce im Kühlschrank aufbewahrt wurde, muss nach dem Ablaufdatum des Fläschchens eine nicht verwendete Medizin weggeworfen (entsorgt) werden.
- Lagern Sie Arikayce -Fläschchen bei Raumtemperatur zwischen 68 ° F und 77 ° F (20 ° C bis 25 ° C) für bis zu 4 Wochen
- Nachdem Arikayce bei Raumtemperatur aufbewahrt wurde, muss am Ende von 4 Wochen jede ungenutzte Medizin weggeworfen (entsorgt) werden.
- Verwenden Sie sofort einen geöffneten Arikayce -Fläschchen.
- Werfen Sie den Arikayce -Fläschchen sofort nach dem Gebrauch weg.
Halten Sie Arikayce und alle Medikamente außerhalb der Reichweite der Kinder.
Allgemeine Informationen über den sicheren und effektiven Gebrauch von Arikayce
Medikamente werden manchmal für andere Zwecke als die in einem Medikamentenhandbuch aufgeführten Zwecke verschrieben. Verwenden Sie Arikayce nicht für einen Zustand, für den sie nicht vorgeschrieben wurde. Geben Sie anderen Menschen nicht Arikayce, auch wenn sie die gleichen Symptome haben, die Sie haben. Es kann ihnen schaden. Sie können Ihren Apotheker oder Gesundheitsdienstleister um Informationen über Arikayce bitten, die für Angehörige der Gesundheitsberufe geschrieben wurden.
Was sind die Zutaten in Arikayce?
Wirkstoff: Amikacinsulfat
Inaktive Zutaten: Dipalmitoylphosphatidylcholin -Cholesterin -Natriumchloridhydroxid (zur pH -Einstellung) und Wasser zur Injektion
Dieser Medikamentenführer wurde von der US -amerikanischen Food and Drug Administration zugelassen.
Anweisungen zur Verwendung
Arikayce ®
Bevölkerung begrenzte Bevölkerung
(Amikacin -Liposomen -Inhalationssuspension) für den oralen Inhalationsgebrauch
Lamira ®
Verneblersystem
Bevor Sie Ihr Lamira -Nebulizer -System verwenden, lesen Sie die detaillierten Informationen in den vollständigen Anweisungen zur Verwendung, die mit dem Lamira Nebulizer -System geliefert werden. Dies liefert vollständigere Informationen darüber, wie Sie Ihr Lamira -Zerstäubersystem zusammenstellen (zusammenstellen). Wenn Sie keinen Teil des Anweisungskontakts verstehen Arikares-Unterstützung bei 1-833-ARIKARE (1-833-274-5273) Vor der Verwendung des Lamira Nebulizer -Systems.
Sammeln Sie Ihre Arikayce -Medizin. Das Arikayce 28-Tage-Kit enthält:
- 1 Arikayce Quick Start Guide
- 1 Anweisungen zum Einfügen verwenden
- 1 Vollständige Verschreibungsinformationen einfügen
- 1 Lamira Nebulizer Mobilteil
- 4 Lamira Aerosol Köpfe (1 in jeder Wochenbox)
- 28 Fläschchen (1 Fläschchen pro Tag) von Arikayce (7 in jeder wöchentlichen Schachtel)
Überprüfen Sie, ob Sie alle erforderlichen Teile für Ihr Lamira -Nebulizer -System haben:
- Tragenfall
- Verbindungskabel
- Regler
- A/C -Stromversorgung
- AA -Batterien
 |
Ersatzlamira Nebulizer Mobilteil:
- Medikamentenkappe und Siegel
- Medikamentenreservoir
- Blaues Ventil
- Aerosolkammer
- Mundstück
- Ersatz -Aerosolkopf
 |
Sie benötigen auch die folgenden Vorräte, die nicht in Ihrem 28-Tage-Kit in Arikayce erhältlich sind, um Ihr Lamira Nebulizer-System zu betreuen:
- Klare flüssige Seife zum Reinigen des Mobilteils und des Aerosolkopfes
- Destilliertes Wasser zum Desinfektion des Mobilteils und des Aerosolkopfes
Wählen Sie Ihr Netzteil und machen Sie es sich vor.
A. 4 AA -Batterien
 |
B. A/C -Stromversorgung
- Stecken Sie die A/C -Stromversorgung in den Controller.
- Stecken Sie die A/C -Stromversorgung in die Wandauslass.
Nicht insert the A/C Power into thefront of the Regler.
 |
Reinigung und Desinfektion
Verwenden Sie vor dem ersten Spülen und desinfizieren Sie Ihr Mobilteil und Aerosolkopf. Vorwärts gehen, um das Mobilteil zu reinigen und zu desinfizieren, einschließlich des Aerosolkopfes nach jeder Verwendung.
Wenn Sie Ihr Mobilteil und Ihr Aerosolkopf erhalten, sind sie nicht steril. Das Reinigen und Desinfizieren Ihres Mobilteils und des Aerosolkopfes ist wichtig, um das Risiko einer Infektionskrankheit und -verunreinigung zu verringern.
- Reinigen des Mobilteils und der Aerosolkopf -Erinnerung: Verwenden Sie vor dem ersten Spülen und Reinigen Sie das Mobilteil und den Aerosolkopf. Vorwärtsspülen und Reinigen Sie das Mobilteil einschließlich des Aerosolkopfes direkt nach jedem Gebrauch.
Verwenden Sie nur einfache Trockenpapertöge oder Wischtücher. Nicht use towels oder wipes that have any chemicals added to them such as alcohol lotion oder baby wipes.
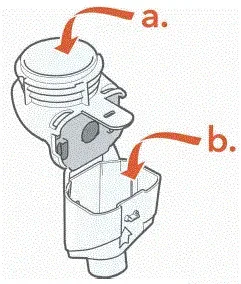
Achten Sie darauf, die Teile nicht zu schaden. Wischen Sie den Aerosolkopf nicht ab.
Werfen Sie Papierhandtücher weg, indem Sie mit festem Abfall in Müll entsorgen.

- Nehmen Sie das Mobilteil zur Reinigung auseinander (zerlegen)
- Wischen Sie alle Tropfen vorsichtig ab Medizin aus dem Medikamentenreservoir (A) Aerosolkammer (B) und Mundstück (c) vor der Spülung, um die Wassersysteme zu reduzieren, um Antibiotika zu reduzieren.
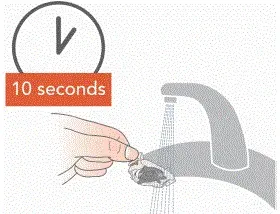
- Spülen Sie jede der Teile unter warmem Laufflagwasser für ab 10 Sekunden. Den Aerosolkopf ausspülen für 10 Sekunden auf jeder Seite.
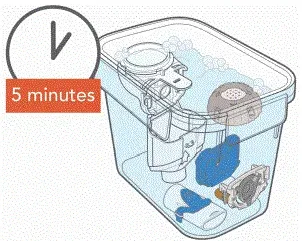
- Reinigen Sie alle Mobilteilteile, indem Sie ein paar Tropfen klarer flüssiger Schalenseife und warmem Leitungswasser zu einer sauberen Wanne oder Schüssel geben. Decken Sie die Mobilteilteile im warmen Seifenwasser ab und genießen Sie für 5 Minuten Sie regelmäßig schütteln. Spülen Sie sie dann gründlich unter warmem Laufflagwasser aus.
- Desinfizieren Sie das Mobilteil und den Aerosolkopf vor dem ersten Verwenden Sie die Erinnerung: Desinfizieren Sie das Mobilteil und den Aerosolkopf vor dem ersten Gebrauch.

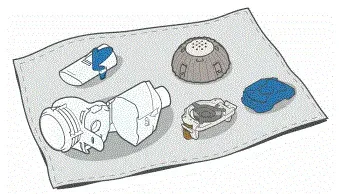
- Stellen Sie sicher, dass Ihr Mobilteil und Ihr Aerosolkopf sauber sind, bevor Sie desinfizieren.
- Stellen Sie sicher, dass der Topf über genügend destilliertes Wasser verfügt, um alle Mobilteilteile einschließlich des Aerosolkopfes vollständig abzudecken.
- Das Wasser in einem sauberen Topf zum Kochen erhitzen.
- Legen Sie die Mobilteile einschließlich des Aerosolkopfes in das kochende Wasser.
- Für einen vollständigen Kochen 5 Minuten . Hinweis: Es kann hilfreich sein, einen Timer zu verwenden.
- Luft trocken auf a fusselfrei Handtuch. Wenn Sie die Teile vollständig trocknen, um sie in einem fusselfreien Handtuch zur Lagerung zu wickeln. Sie können sie kurz vor der nächsten Behandlung wieder zusammenstellen.
Zusammenstellen Ihres Mobilteils
Schritt 1: Waschen Sie Ihre Hände mit Seife und Wasser Und dry them well.
 |
Schritt 2: Setzen Sie das blaue Ventil ein.
Öffnen Sie das Mobilteil, indem Sie vorsichtig auf der Registerkarte des Medikamentenreservoirs hochziehen.
Setzen Sie das blaue Ventil so ein, dass es auf dem Aerosolkammer liegt und die 2 Ventilklappen nach unten (Ventilklappen nicht gebogen).
 |
Aer Ool C Hamber Val ve Klappenventilklappe Blaues Ventil
Schritt 3: Setzen Sie den Aerosolkopf ein.
Fassen Sie den Aerosolkopf an den 2 flexiblen Kunststofflaschen auf jeder Seite. Stellen Sie sicher, dass der Text Lamira ® steht Ihnen zu Ihnen und steht oben am Aerosolkopf.
Drücken Sie die 2 flexiblen Kunststofflaschen zusammen, während Sie den Aerosolkopf in das Medikamentenreservoir einfügen.
Schließen Sie das Mobilteil, wenn Sie fertig sind (keine Lücken entlang der blauen Ventilkante).
 |
Nicht touch the silver part of theAerosol Head at any time.
Nachdem der Aerosol -Kopf 7 -mal weggeworfen wurde (entsorgt) und durch eine neue Einführung des Reinigungsprozesses ersetzen wurde. Lamira -Mobilteil soll für 28 Tage verwendet werden.
 |
Schritt 4: Befestigen Sie das Mundstück Toyour -Mobilteil mit dem blauen Klappern.
 |
Schritt 5: Fügen Sie das Mobilteil schließlich an den Controller an.
A. Befestigen Sie das Anschlusskabel am Mobilteil. A1. Richten Sie den Boden des Steckers mit dem Boden des Mobilteils aus.
A2. Drücken Sie nach oben gegen das Mobilteil, bis Sie die Teile zusammenschnappen hören. B. Schließen Sie das Verbindungskabel an den Controller an.
 |
Arikayce nehmen
Ihre Arikayce sollte vor dem Gebrauch bei Raumtemperatur sein, um sicherzustellen, dass Ihr Lamira -Verneblersystem ordnungsgemäß funktioniert. Nicht use other medicines in your HUndset.
Bringen Sie Arikayce auf Raumtemperatur, indem Sie ihn aus dem Kühlschrank entfernen mindestens 45 Minuten Vor dem Gebrauch. Nicht use if your Arikayce has been frozen.
Schritt 1: Machen Sie Ihren Arikayce bereit.
- Legen Sie das Mobilteil auf einer sauberen, flachen stabilen Oberfläche.
- Schütteln Sie den Arikayce -Fläschchen für mindestens 10 bis 15 Sekunden Und bis das Medikament überall gleich aussieht und gut gemischt ist.
 |
Wie man den Arikayce -Fläschchen öffnet
 |
 |
 |
 |
- Heben Sie die Orangenkappe an Aus dem Fläschchen.
- Den Metallring greifen Auf dem Fläschchen und ziehen Sie es vorsichtig nach unten, bis 1 Seite vom Fläschchen abbricht, aber ziehen Sie die Lasche nicht vollständig ab.
- Ziehen Sie das Metallband Von der Fläschchenfläschchen in einer kreisförmigen Bewegung, bis es vollständig abgibt.
- Vorsichtig entfernen der Gummi -Stopper.
A. Öffnen Sie die Fläschchen und gießen Sie die Arikayce in das Medikamentenreservoir.
B. Befestigen Sie die Medikamentenkappe.
 |
Schritt 2: Setzen Sie sich in einer entspannten aufrechten Position.
- Halten Sie die Ein/Aus -Taste für einige Sekunden gedrückt, um die Lamira einzuschalten.
- Nebel beginnt zu fließen.
 |
Schritt 3: Setzen Sie das Mundstück ein (aber bedecken Sie die blaue Klappe nicht) und atmen Sie langsam tief ein.
- Dann atmen Sie dann normal durch das Mundstück, bis Ihre Behandlung abgeschlossen ist.
- Die Behandlung sollte ungefähr 14 Minuten dauern, könnte aber bis zu 20 Minuten dauern.
Achten Sie darauf, das Mobilteil während der gesamten Behandlung zu halten.
 |
Schritt 4: Überprüfen Sie, ob Ihre Behandlung beendet ist.
- Die Lamira wird 2 Mal piept.
- Ein Checkmark wird kurz auf dem Bildschirm angezeigt.
- Der Controller schaltet automatisch ab.
- Entfernen Sie die Medikamentenkappe und Überprüfen Sie das Medikamentenreservoir, um sicherzustellen, dass nicht mehr als ein paar Tropfen Arikayce übrig bleiben. Wenn Arikayce bleibt, ersetzen Sie die Medikamentenkappe, drücken Sie die Ein/Aus -Taste und umfassen Ihre Dosis.
 |
Für alle Probleme, die Sie möglicherweise mit Ihrem Lamira -Nebulizer -System haben, siehe Abschnitt J -Frequent gestellte Fragen und Abschnitt K -Roubleshooting der vollständigen Anweisungen für die Verwendung, die mit Ihrem Medikament geliefert wird.
Reinigen Sie Ihr Lamira -Mobilteil und Aerosolkopf nach dem Gebrauch
- Nach jedem Gebrauch sofort das Mobilteil reinigen und desinfizieren, um Infektionskrankheiten und Kontaminationen zu verringern.
- Desinfizieren Sie das Mobilteil und den Aerosolkopf nach jeder Verwendung.
- Sehen Sie sich die Reinigung und Desinfektion zu Beginn der Anweisungen zur richtigen Reinigung und Desinfektion Ihres Mobilteils und Aerosolkopfes finden Sie in der Reinigung und Desinfektion.
Diese Verwendung wurden von der US -amerikanischen Food and Drug Administration genehmigt.






