Die Informationen Auf Dieser Website Stellen Keine Medizinische Beratung Dar. Wir Verkaufen Nichts. Die Richtigkeit Der Übersetzung Wird Nicht Garantiert. Haftungsausschluss
Antikonvulsiva, andereFINTEPLA
Drogenzusammenfassung
Was ist FINTEPLA?
FINTEPLA (Fenfluramin) ist ein Antikonvulsant Wird zur Behandlung von Anfällen im Zusammenhang mit dem Dravet -Syndrom bei Patienten 2 Jahre und älter verwendet.
Was sind Nebenwirkungen von FintePla?
FINTEPLA
- Nesselsucht
- Schwierigkeiten beim Atmen
- Schwellung Ihrer Gesichtslippen Zunge oder Hals
- Stimmung oder Verhalten ändert sich
- Angst
- Panikattacken
- Probleme beim Schlafen
- Impulsivität
- Agitation
- Feindseligkeit
- Aggressionen
- Unruhe
- Hyperaktivität (geistig oder körperlich)
- erhöhte Depression
- Gedanken an Selbstverletzung
- Brustschmerzen
- Herzschläge
- Flattern in Ihrer Brust
- Kurzatmigkeit
- Blau gefärbte Haut oder Lippen
- Schwellung in Ihren Unterbeinen
- ungewöhnliche Müdigkeit
- Schwäche
- Benommenheit
- Appetitverlust
- Gewichtsverlust
- Verschlechterung von Anfällen
- verschwommenes Sehen
- Tunnelsicht
- Augenschmerzen oder Rötung
- Halos um Licht herum sehen
- Brechreiz
- Erbrechen
- Starke Kopfschmerzen
- verschwommenes Sehen
- in deinen Hals oder Ohren klopfen
- Nasenbluten
- Fieber
- Schwitzen
- Halluzinationen
- Zittern
- Schnelle Herzfrequenz
- Muskelsteifigkeit
- zucken
- verlangsamtes Wachstum (bei Kindern)
- Koordinierungsverlust und
- Durchfall
Holen Sie sich sofort medizinische Hilfe, wenn Sie eines der oben aufgeführten Symptome haben.
Nebenwirkungen von FintePla umfassen:
- Verringerter Appetit
- Schläfrigkeit
- Beruhigung
- Lethargie
- Durchfall
- Verstopfung
- Abnormale Echokardiogramm
- Ermüdung
- sich unwohl fühlen (Unwohlsein)
- Schwäche
- Probleme mit der Muskelkoordination
- Gleichgewichtsstörung
- Gangstörung
- Erhöhter Blutdruck
- Sabbern/Überschuss
- Fieber
- Infektion der oberen Atemwege
- Erbrechen
- Gewichtsverlust
- fällt und
- Status epilepticus
Suchen Sie medizinische Versorgung oder rufen Sie auf einmal 911 an, wenn Sie die folgenden schwerwiegenden Nebenwirkungen haben:
- Schwerwiegende Augensymptome wie plötzlicher Sehverlust verschwommenes Sehen Tunnel Sehschmerzen oder Schwellungen oder Halos in der Umgebung des Lichts;
- Schwerwiegende Herzsymptome wie schnelle unregelmäßige oder pochende Herzschläge; Flattern in deiner Brust; Kurzatmigkeit; und plötzliche Schwindel -Benommenheit oder ohnmächtig;
- Starke Kopfschmerzen Verwirrung verwirrt Spracharm oder Bein Schwäche Schwierigkeiten beim Verlust der Koordination unstabil sehr steifes Muskeln hoher Fieber problemlos Schwitzen oder Zittern.
Dieses Dokument enthält nicht alle möglichen Nebenwirkungen und andere können auftreten. Wenden Sie sich an Ihren Arzt nach zusätzlichen Informationen zu Nebenwirkungen.
Dosierung für FintePla
Die anfängliche Start- und Wartungsdosis von FinstePla beträgt zweimal täglich 0,1 mg/kg, was wöchentlich erhöht werden kann, basierend auf Wirksamkeit und Verträglichkeit.
FintePla bei Kindern
Die Sicherheit und Wirksamkeit von FintePla zur Behandlung von mit dem Dravet -Syndrom verbundenen Anfällen wurde bei Patienten ab 2 Jahren und älter festgelegt. Sicherheit und Wirksamkeit von FintePla bei Patienten, die weniger als 2 Jahre alt sind, wurden nicht festgelegt.
Dystonien und andere extrapyramidale Symptome im Zusammenhang mit Metoclopramid sind bei pädiatrischen Patienten häufiger als bei Erwachsenen. Zusätzlich haben Neugeborene eine verringerte Nadh-Cytochrom-B5-Reduktase, was sie anfälliger für Methämoglobinämie ist, eine mögliche nachteilige Reaktion der Metoclopramidverwendung bei Neugeborenen.
Welche Drogensubstanzen oder Nahrungsergänzungsmittel interagieren mit FintePla?
FINTEPLA kann mit anderen Medikamenten interagieren, wie z. B.:
- Rifampin
- Strippentol plus Clobazam
- Cyproheptadin
- Potent 5-HT1A 5-HT1D 5-HT2A oder 5-HT2C Serotonin Rezeptorantagonisten und
- Medikamente rezeptfreie Medikamente oder pflanzliche Nahrungsergänzungsmittel, die Serotonin erhöhen, wie selektive Serotonin-Wiederaufnahmehemmer (SSRIS) Serotonin-Norpinephrin-Wiederaufnahmehemmer (SNRIS) (SNRIS) trizyklische Antidepressiva Monoaminoxidase -Inhibitoren
Sagen Sie Ihrem Arzt alle Medikamente und Nahrungsergänzungsmittel, die Sie verwenden.
BINTEPLA während der Schwangerschaft und des Stillens
Sagen Sie Ihrem Arzt, wenn Sie schwanger sind oder vorhaben, vor der Verwendung von FintePla schwanger zu werden. Es ist nicht bekannt, wie es einen Fötus beeinflussen würde. Es gibt ein Schwangerschafts -Expositionsregister, das die Schwangerschaftsergebnisse bei Frauen überwacht, die Antiepileptika (AEDs) wie FintePla während der Schwangerschaft ausgesetzt sind. Es ist nicht bekannt, ob FintePla in die Muttermilch übergeht. Wenden Sie sich vor dem Stillen an Ihren Arzt.
Weitere Informationen
Unsere FINTEPLA (Fenfluramin) orale Lösung Civ Side Effects Drug Center bietet einen umfassenden Überblick über die verfügbaren Arzneimittelinformationen über die potenziellen Nebenwirkungen bei der Einnahme dieses Medikaments.
Dies ist keine vollständige Liste von Nebenwirkungen, und andere können auftreten. Rufen Sie Ihren Arzt an, um medizinische Beratung zu Nebenwirkungen zu erhalten. Sie können die FDA bei 1-800-FDA-1088 Nebenwirkungen melden.
FDA -Drogeninformationen
- Drogenbeschreibung
- Indikationen
- Nebenwirkungen
- Wechselwirkungen mit Arzneimitteln
- Warnungen
- Überdosis
- Klinische Pharmakologie
- Medikamentenhandbuch
WARNUNG
Klappenherzerkrankung und pulmonale arterielle Hypertonie
Es besteht eine Assoziation zwischen serotonergen Arzneimitteln mit einer Agonistenaktivität von 5-HT2B-Rezeptor-Agonisten, einschließlich Fenfluramin (dem Wirkstoff in der Fintepla) und einer Herzkrankheit der Klappen und einer pulmonalen arteriellen Hypertonie [siehe WARNUNGS AND PRECAUTIONS ].
Echokardiogrammbewertungen sind vor und nach der Behandlung mit FintePla erforderlich. Die Vorteile im Vergleich zu den Risiken der Initiierung oder der fortgesetzten Fintepla müssen auf der Grundlage von Echokardiogram -Befunden berücksichtigt werden [siehe Dosierung und Verwaltung Und WARNUNGS AND PRECAUTIONS ].
Aufgrund der Risiken von Herzklappenerkrankungen und pulmonaler arterieller Hypertonie ist FINTEPLA nur durch ein eingeschränktes Programm im Rahmen einer Risikobewertung und Minderungsstrategie (REMS) als FINTEPLA REMS verfügbar [siehe WARNUNGS AND PRECAUTIONS ].
Beschreibung für FINTEPLA
Die mündliche FINTEPLA -Lösung enthält 2,2 mg/ml Fenfluramin, die 2,5 mg/ml des Hydrochloridsalzes entsprechen.
Der Wirkstoff-Fenfluraminhydrochlorid wird chemisch als N-Ethyl-α-Methyl-3- (Trifluormethyl) -Phenethylaminhydrochlorid bezeichnet.
Die strukturelle Formel lautet:
| |
Fenfluraminhydrochlorid ist ein weißer bis branchierter kristalliner Feststoff. Die PKA von Fenfluramin beträgt 10,2.
FINTEPLA ist eine klare farblose Lösung pH 5.
FINTEPLA enthält die folgenden inaktiven Inhaltsstoffe: Kirschgeschmack Zitronensäure -Ethylparabenhydroxyethylcellulose -Methylparaben -Kalium -Citrat -Sucralose und Wasser.
FINTEPLA enthält keine Zutat aus glutenhaltigem Getreide (Weizengerste oder Roggen).
Verwendung für FintePla
FINTEPLA ist für die Behandlung von Anfällen im Zusammenhang mit dem Dravet-Syndrom (DS) und dem Lennox-Gastaut-Syndrom (LGS) bei Patienten 2 Jahre und älter gekennzeichnet.
Dosierung für FintePla
Bewertungen vor der Einleitung von FintePla
Vor Beginn der Behandlung mit FintePla erhalten Sie eine Echokardiogramm -Bewertung, um die Herzkrankheit und die pulmonale arterielle Hypertonie zu bewerten [siehe Bewertungen während und nach der Verabreichung von FintePla Und WARNUNGS AND PRECAUTIONS ].
Dosierungsinformationen
FINTEPLA ist mündlich verabreicht und kann mit oder ohne Nahrung eingenommen werden.
Draved Syndrom
- Die anfängliche Start- und Erhaltungsdosis für Patienten mit Dravet -Syndrom beträgt zweimal täglich 0,1 mg/kg, was auf der Grundlage von Wirksamkeit und Verträglichkeit wöchentlich erhöht werden kann. Tabelle 1 enthält bei Bedarf den empfohlenen Titrationsplan.
- Patienten mit Dravet -Syndrom, die nicht mit einem gleichzeitigen Strippentol, der zweimal täglich bei 0,1 mg/kg toleriert, toleriert und eine weitere Verringerung der Anfälle erfordern, können von einer Dosierungserhöhung bis zu einer maximal empfohlenen Erhaltungsdosis von 0,35 mg/kg zweimal täglich profitieren (Maximum Daily Dosierung von 26 mg).
- Patienten mit Dravet -Syndrom, die gleichzeitig mit 0,1 mg/kg Bintenstuhl zweimal täglich die Farbbücher tolerieren und eine weitere Verringerung der Anfälle benötigen, kann von einer Dosierungssteigerung bis zu einer maximal empfohlenen Erhaltungsdosis von 0,2 mg/kg zweimal täglich profitieren (maximal täglicher Dosierung von 17 mg) [siehe [siehe [siehe) [siehe [siehe [siehe Wechselwirkungen mit Arzneimitteln ].
Lennox-Gastaut-Syndrom
- Die anfängliche Startdosis für Patienten mit Lennox-Gastaut-Syndrom beträgt zweimal täglich 0,1 mg/kg, was auf der Grundlage der Verträglichkeit wöchentlich erhöht werden sollte. Tabelle 1 enthält den empfohlenen Titrationsplan.
- Patienten mit Lennox-Gastaut-Syndrom, die nicht auf gleichzeitigen Strippentol tolerieren, die FinzePla tolerieren, sollten zweimal täglich auf die empfohlene Erhaltungsdosis von 0,35 mg/kg titriert werden (maximale tägliche Dosierung von 26 mg).
- Patienten mit Lennox-Gastaut-Syndrom, die gleichzeitig mit Strippentol plus Clobazam, die toleriert, sollten zweimal täglich auf die empfohlene Erhaltungsdosis von 0,2 mg/kg titriert werden (maximale tägliche Dosierung von 17 mg) [siehe Wechselwirkungen mit Arzneimitteln ].
Tabelle 1: FINTEPLA empfohlene Titrationsplan*
| Ohne gleichzeitige Strippentol* | Mit gleichzeitigem Strippentol plus Clobazam | |||
| Gewichtsbasierte Dosierung | Maximale Gesamtdosis der täglichen Dosierung ± | Gewichtsbasierte Dosierung | Maximale Dosierung ± Gesamttäglich | |
| Anfängliche Dosierung | 0,1 mg/kg zweimal täglich | 26 mg | 0,1 mg/kg zweimal täglich | 17 mg |
| Tag 7 | 0,2 mg/kg zweimal täglich | 26 mg | 0,15 mg/kg zweimal täglich | 17 mg |
| Tag 14 ** | 0,35 mg/kg zweimal täglich | 26 mg | 0,2 mg/kg zweimal täglich | 17 mg |
| * Bei Patienten, die nicht in gleichzeitiger Sturz auf Stripentol, bei dem eine schnelle Titration gerechtfertigt ist, kann die Dosis alle 4 Tage erhöht werden. Bei Patienten mit Dravet -Syndrom -Dosierung kann die Dosierung aufgrund des klinischen Ansprechens auf die maximal empfohlene Dosierung bei Bedarf erhöht werden. ** Bei Patienten mit Lennox-Gastaut-Syndromdosis sollte die empfohlene Erhaltungsdosis (d. H. Tag 14) erhöht werden. ± Für maximale Dosierung mit gleichzeitiger Verwendung starker CYP1A2- oder CYP2D6 -Inhibitoren bei Patienten mit schwerer Nierenbeeinträchtigung oder bei Patienten mit Leberfunktion Dosierungsmodifikationen für Patienten mit gleichzeitiger Anwendung starker CYP1A2- oder CYP2D6 -Inhibitoren (DS und LGs) Dosierungsmodifikationen für Patienten mit schwerer Nierenbeeinträchtigung (DS und LGS) Dosierungsmodifikationen für Patienten mit leichter mittelschwerer und schwerer Leberminderung (DS und LGs und LGs) (DS und LGs) (DS und LGs) (DS und LGs) (DS und LGs) |
Dosierungsmodifikationen für Patienten mit gleichzeitiger Verwendung starker CYP1A2- oder CYP2D6 -Inhibitoren (DS und LGs)
Bei Patienten mit gleichzeitiger Verwendung von FinstePla mit einem starken CYP1A2- oder CYP2D6 Wechselwirkungen mit Arzneimitteln ].
Dosierungsmodifikationen für Patienten mit schwerer Nierenbeeinträchtigung (DS und LGS)
Bei Patienten mit schwerer Nierenbeeinträchtigung (geschätzte glomeruläre Filtrationsrate (EGFR) 15 bis 29 ml/min/1,73 m 2 ) Eine maximale tägliche Dosierung von 20 mg ohne begleitende Strippentol und 17 mg mit gleichzeitigem Sturzauftrieb plus Clobazam [siehe Verwendung in bestimmten Populationen ].
Dosierungsmodifikationen für Patienten mit leichter mittelschwerer und schwerer Leberbeeinträchtigung (DS und LGS)
Siehe Tabelle 2 für Dosierungsanpassungen und Empfehlungen für Patienten mit Leberbeeinträchtigung [siehe Verwendung in bestimmten Populationen ].
Tabelle 2: Modifikationen und Empfehlungen für Patienten, die bei Patienten zurückgehalten werden
| Leberbeeinträchtigungsklassifizierung | Ohne gleichzeitige Strippentol* | Mit gleichzeitigem Strippentol plus Clobazam |
| Maximale Gesamtdosis der Gesamtdosis | Maximale Gesamtdosis der Gesamtdosis | |
| Leicht (Kinder-Pugh A) | 20 mg | 13 mg* |
| Mäßig (Kinder-Pugh B) | 20 mg | Verwenden Sie nicht empfohlen |
| Schwer (Kinder-Pugh C) | 17 mg | Verwenden Sie nicht empfohlen |
| * Titrieren Sie wie empfohlen [siehe Dosierungsinformationen |
Bewertungen während und nach der Verabreichung von FintePla
Um die Herzkrankheit und die pulmonale arterielle Hypertonie zu bewerten WARNUNGS AND PRECAUTIONS ].
Verwaltungsanweisungen
Eine kalibrierte Messvorrichtung (entweder 3 ml oder 6 ml orale Spritze) wird von der Apotheke bereitgestellt und wird empfohlen, die vorgeschriebene Dosis genau zu messen und zu verabreichen [siehe Wie geliefert ]. A household teaspoon or tablespoon is not an adequate measuring device Und should not be used.
Verwerfen Sie eine nicht verwendete mündliche FintePla -Lösung, die nach 3 Monaten zum ersten Mal die Flasche oder den Abwurf nach dem Datum auf der Flasche geöffnet wird, je nachdem, was früher ist.
FINTEPLA ist mit im Handel erhältlichen Magen- und Nasogastr -Fütterungsröhrchen kompatibel.
Einstellung von FintePla
Beim Absetzen der Fintepla sollte die Dosis allmählich verringert werden. Wie bei allen Antiepileptika sollte abruptes Absetzen nach Möglichkeit vermieden werden, um das Risiko einer erhöhten Anfallsfrequenz und des Status epilepticus zu minimieren [siehe WARNUNGS AND PRECAUTIONS ].
Wie geliefert
Dosierungsformen und Stärken
Orale Lösung : 2,2 mg/ml Fenfluramin als klare farblose Flüssigkeit mit Kirschgeschmack.
FINTEPLA Die orale Lösung ist eine klare farblose Flüssigkeit mit kirscharem Geschmack mit 2,2 mg/ml Fenfluramin und wird wie folgt in einer weißen Plastikflasche mit einem kinderbeständigen Verschluss geliefert:
- Karton mit einer 360 ml Flasche (Flasche ( NDC 43376-322-36)
- Karton mit einer 30 -ml -Flasche (Flasche ( NDC 43376-322-30)
Vor dem Abgeben fügt der Apotheker einen Press-in-Flaschenadapter in die Flasche ein. Die Apotheke liefert 3 ml oder 6 ml kalibrierte orale Dosierspritzen.
Lagerung und Handhabung
FINTEPLA bei Raumtemperatur zwischen 20 ° C und 25 ° C (68 ° F bis 77 ° F) aufbewahren; Die Exkursionen sind zwischen 15 ° C bis 30 ° C (59 ° F bis 86 ° F) zulässig [siehe USP -kontrollierte Raumtemperatur].
Nicht kühlen oder einfrieren. Lagern Sie die Flasche und spritzen Sie zusammen.
Verwerfen Sie einen ungenutzten Teil 3 Monate nach dem ersten Öffnen der Flasche oder dem Abwurf nach dem Datum auf der Flasche, je nachdem, was früher ist.
Prozentuale Reduzierung von Ausgangswert bei der Frequenz der Abfallannahme
Anteil der Patienten (%)
Hergestellt für: UCB Inc. Smyrna GA 30080. Überarbeitet: Apr 2025.
Nebenwirkungen for Fintepla
Die folgenden klinisch signifikanten Nebenwirkungen werden an anderer Stelle bei der Markierung beschrieben:
- Herzklappenherzerkrankung und pulmonale arterielle Hypertonie [siehe WARNUNGS AND PRECAUTIONS ]
- Verminderter Appetit und verringerte Gewicht [siehe WARNUNGS AND PRECAUTIONS ]
- Schläfrigkeits -Sedierung und Lethargie [siehe WARNUNGS AND PRECAUTIONS ]
- Selbstmordverhalten und Selbstmordverhalten [siehe WARNUNGS AND PRECAUTIONS ]
- Rückzug von Antiepileptika [siehe WARNUNGS AND PRECAUTIONS ]
- Serotons Syndrom [siehe WARNUNGS AND PRECAUTIONS ]
- Erhöhung des Blutdrucks [siehe WARNUNGS AND PRECAUTIONS ]
- Glaukom [siehe WARNUNGS AND PRECAUTIONS ]
Klinische Studien Erfahrung
Da klinische Studien unter stark unterschiedlichen Bedingungen durchgeführt werden, die in den klinischen Studien eines Arzneimittels beobachtet werden, können in den klinischen Studien eines anderen Arzneimittels nicht direkt mit den Raten verglichen werden und spiegeln möglicherweise nicht die in der Praxis beobachteten Raten wider.
Bei kontrollierten und unkontrollierten Studien bei Patienten mit Dravet -Syndrom (DS) wurden 341 Patienten mit FINTEPLA behandelt, einschließlich 312 Patienten, die mehr als 6 Monate behandelt wurden, 284 Patienten, die mehr als 1 Jahr behandelt wurden, und 138 Patienten, die mehr als 2 Jahre behandelt wurden.
Bei kontrollierten und unkontrollierten Studien bei Patienten mit Lennox-Gastaut-Syndrom (LGS) wurden 262 Patienten mit FinstePla behandelt, einschließlich 219 Patienten, die mehr als 6 Monate lang behandelt wurden, 172 Patienten, die mehr als 1 Jahr behandelt wurden, und 127 Patienten, die mehr als 2 Jahre behandelt wurden.
Draved Syndrom
In placebokontrollierten Studien mit Patienten mit DS, die gleichzeitig eingehen, wurden 122 Patienten mit BINTEPLA behandelt, und 84 Patienten erhielten Placebo [siehe Klinische Studien ]. The duration of treatment in these trials was 16 weeks (Studie 1) or 17 weeks (Studie 2).
In Studie 1 und Studie 2 betrug das Durchschnittsalter 9 Jahre (Bereich 2 bis 19 Jahre), und ungefähr 46% der Patienten waren weiblich und 74% waren weiß. Alle Patienten erhielten mindestens einen anderen AED.
In Studie 1 und Studie 2 betrug die Abbruchraten infolge einer Nebenwirkung 13% 0% und 7% bei Patienten, die mit 7 mg/kg/Tag 0,2 mg/kg/Tag und 0,4 mg/kg/Tag in Kombination mit Stripentol im Vergleich zu 6% für Patienten auf Placebo behandelt wurden. Die häufigste Nebenwirkung, die zu Absetzen bei den mit einer Finanzdosis behandelten Patienten führte, war die Schläfrigkeit (3%).
Die häufigsten Nebenwirkungen bei Patienten, die mit FinzePla (Inzidenz mindestens 10% und größer als Placebo als Placebo) auftraten, waren ein verringerter Appetit. Schläfrigkeit Sedierung Lethargie; Durchfall; Verstopfung; abnormales Echokardiogramm; Müdigkeits -Unwohlsein Asthenie; Ataxie -Gleichgewichtsstörung Störung; Der Blutdruck nahm zu; Sabberer Speichelhypersekretion; Pyrexie; Infektion der oberen Atemwege; Erbrechen; vermindertes Gewicht; fallen; Status epilepticus.
In Tabelle 4 sind die nachteiligen Reaktionen aufgeführt, die bei 5% oder mehr von Patienten, die während der Titrations- und Erhaltungsphasen von Studie 1 und Studie 2 größer sind, und mit einer Geschwindigkeit, die über Placebo behandelt wurden, berichtet wurden.
Tabelle 4: Nebenwirkungen bei 5% oder mehr von Patienten, die mit FinzePla und Greater behandelt werden als Placebo in Placebo-kontrollierten Studien zum Dravet-Syndrom (Studie 1 und 2)
| Nebenwirkungen | FINTEPLA Dose Group | Kombinierte Placebo -Gruppe (2) | ||
| Studie 1 | Studie 2 | |||
| 0,2 mg/kg/Tag | 0,7 mg/kg/Tag | 0,4 mg/kg/Tag (1) | ||
| N = 39 % | N = 40 % | N = 43 % | N = 84 % | |
| Verringerter Appetit | 23 | 38 | 49 | 8 |
| Somnolence Sedation Lethargie | 26 | 25 | 23 | 11 |
| Abnormale Echokardiogramm (3) | 18 | 23 | 9 | 6 |
| Durchfall | 31 | 15 | 23 | 6 |
| Verstopfung | 3 | 10 | 7 | 0 |
| Müdigkeit Unwohlsein Asthenie | 15 | 10 | 30 | 5 |
| Ataxie -Gleichgewichtsstörung Störung | 10 | 10 | 7 | 1 |
| Abnormales Verhalten | 0 | 8 | 9 | 0 |
| Der Blutdruck nahm zu | 13 | 8 | 0 | 5 |
| Sabberer Speichelhypersekretion | 13 | 8 | 2 | 0 |
| Hypotonie | 0 | 8 | 0 | 0 |
| Ausschlag | 8 | 8 | 5 | 4 |
| Blutprolaktin nahm zu | 0 | 5 | 0 | 0 |
| Schüttelfrost | 0 | 5 | 2 | 0 |
| Verringerte Aktivität | 0 | 5 | 0 | 1 |
| Dehydration | 0 | 5 | 0 | 0 |
| Schlaflosigkeit | 0 | 5 | 5 | 2 |
| Pyrexie | 15 | 5 | 21 | 14 |
| Stereotypen | 0 | 5 | 0 | 0 |
| Infektion der oberen Atemwege | 21 | 5 | 7 | 10 |
| Erbrechen | 10 | 5 | 5 | 8 |
| Gewicht nahm ab | 13 | 5 | 7 | 1 |
| Kruppe | 5 | 3 | 0 | 1 |
| Ohrenentzündung | 8 | 3 | 9 | 5 |
| Gastroenteritis | 8 | 3 | 2 | 0 |
| Erhöhte Herzfrequenz | 5 | 3 | 0 | 2 |
| Reizbarkeit | 0 | 3 | 9 | 2 |
| Rhinitis | 8 | 3 | 7 | 2 |
| Tremor | 3 | 3 | 9 | 0 |
| Harninkontinenz | 5 | 3 | 0 | 0 |
| Verminderter Blutzucker | 0 | 0 | 9 | 1 |
| Bronchitis | 3 | 0 | 9 | 1 |
| Prellung | 5 | 0 | 0 | 0 |
| Ekzem | 0 | 0 | 5 | 0 |
| Enuresis | 5 | 0 | 0 | 0 |
| Fallen | 10 | 0 | 0 | 4 |
| Kopfschmerzen | 8 | 0 | 0 | 2 |
| Laryngitis | 0 | 0 | 5 | 0 |
| Negativismus | 5 | 0 | 0 | 0 |
| Status epilepticus | 3 | 0 | 12 | 2 |
| Harnwegsinfektion | 5 | 0 | 5 | 0 |
| Virusinfektion | 0 | 0 | 5 | 1 |
| (1) 0,4 mg/kg/Tag was not an intermediate dose. Patients on the 0,4 mg/kg/Tag dose were also taking concomitant Strippentol plus Clobazam which increases exposure of FINTEPLA. (2) Patienten in Placebo -Gruppen aus den Studien 1 und 2 wurden gepoolt. (3) Bestand aus Spuren- und leichten Mitralinsuffizienz- und Spurenaorten -Regurgitation, die als physiologisch angesehen werden |
Lennox-Gastaut-Syndrom
In der placebokontrollierten Studie mit Patienten mit LGs, die gleichzeitig den Pflegestandard einnehmen Klinische Studien ]. The duration of treatment in this trial was 16 weeks. The mean age was 13.7 years (range 2 to 35 years) Und 29% of patients were at least 18 years of age 45% of patients were female Und 79% were White. All patients were receiving at least one other AED.
Die Abbruchraten infolge einer negativen Reaktion betrugen 6% und 5% bei Patienten, die mit 7 mg/kg/Tag und 0,2 mg/kg/Tag behandelt wurden, verglichen mit 1% bei Patienten auf Placebo. Die häufigsten Nebenwirkungen, die zum Absetzen bei den mit einer Finanzdosis behandelten Patienten führten, waren Anfälle (2%) und Somnolence (2%).
Die häufigen nachteiligen Reaktionen bei Patienten, die mit FinzePla (Inzidenz mindestens 10% und größer als Placebo) behandelt wurden, waren Durchfall; verminderter Appetit; Ermüdung; Schläfrigkeit; Erbrechen.
In Tabelle 5 sind die nachteiligen Reaktionen aufgeführt, die bei 5% oder mehr der mit der Finzepla behandelten Patienten und einer Geschwindigkeit, die über Placebo während der Titrations- und Erhaltungsphasen von Studie 3 behandelt wurden, gemeldet wurden.
Tabelle 5: Nebenwirkungen bei 5% oder mehr von Patienten, die in der placebokontrollierten Studie für das Lennox-Gastaut-Syndrom behandelt wurden, und mehr als Placebo mehr als Placebo (Studie 3)
| Nebenwirkungen | FINTEPLA Dose Group | ||
| Studie 3 | Placebo -Gruppe | ||
| 0,2 mg/kg/Tag | 0,7 mg/kg/Tag | ||
| N = 89 % | N = 87 % | N = 87 % | |
| Verringerter Appetit | 20 | 36 | 12 |
| Müdigkeit Unwohlsein Asthenie | 14 | 24 | 16 |
| Somnolence Sedation Lethargie | 12 | 22 | 16 |
| Durchfall | 11 | 13 | 5 |
| Verstopfung | 6 | 9 | 6 |
| Erbrechen | 14 | 8 | 6 |
| Gewicht nahm ab | 2 | 8 | 2 |
| Infektion der oberen Atemwege | 8 | 7 | 3 |
| Beschlagnahme | 9 | 5 | 7 |
| Reizbarkeit | 8 | 3 | 6 |
Echokardiographische Sicherheitsbewertungen der Herzkrankheiten mit Klappen und pulmonaler arterieller Hypertonie
Valvulare Herzerkrankungen und pulmonale arterielle Hypertonie wurden in den placebokontrollierten und Open-Label-Erweiterungsstudien durch Echokardiographie für 341 DS-Patienten und 263 LGS-Patienten über 3 Jahre lang bewertet [siehe WARNUNGS AND PRECAUTIONS ]. Screening for valvular heart disease assessed for mild or greater aortic regurgitation or moderate or greater mitral regurgitation Und assessed for additional characteristics of VHD (e.g. valve thickening or restrictive valve motion).
In diesen klinischen Studien zeigten zwei Patienten mit LGs eine leichte Aorteninsuffizienz (AR) (AR), aber keiner der Patient hatte Herzzeichen oder Symptome oder Hinweise auf strukturelle Veränderungen der Klappen.
Keiner der Patient hatte VHD. Die milden AR -Raten stimmen mit denen überein, die in der Screening -Periode vor der Behandlung beobachtet wurden (3 Patienten in LGs und 1 Patient in klinischen DS -Studien).
Nachmarkterfahrung
Die folgenden nachteiligen Reaktionen wurden während der Verwendung von FintePla nach der Annahme identifiziert. Da diese Reaktionen freiwillig aus einer Population unsicherer Größe berichtet werden, ist es nicht immer möglich, ihre Häufigkeit zuverlässig abzuschätzen oder ein kausales Verhältnis zur Arzneimittelexposition herzustellen.
Psychiatrische Störungen : Aggression
Wechselwirkungen mit Arzneimitteln for Fintepla
Auswirkung anderer Medikamente auf FintePla
Strippentol plus Clobazam
Gleichzeitige Verabreichung von FinstePla mit Strippentol plus Clobazam mit oder ohne Valproat erhöht die Fenfluramin -Plasmakonzentrationen [siehe Klinische Pharmakologie ]. If FINTEPLA is coadministered with Strippentol plus Clobazam the maximum daily dosage of FINTEPLA is 0,2 mg/kg zweimal täglich (maximum daily dosage of 17 mg) [see Dosierung und Verwaltung ].
Starke CYP1A2 CYP2B6- oder CYP3A -Induktoren
Gleichzeitige Verabreichung von FinstePla mit starken CYP1A2 -CYP2B6- oder CYP3A -Induktoren verringern die Fenfluramin -Plasmakonzentrationen Klinische Pharmakologie ].
Es wird empfohlen, die gleichzeitige Verabreichung von starken CYP1A2 -CYP2B6- oder CYP3A -Induktoren zu vermeiden. Wenn die gleichzeitige Verabreichung eines starken CYP1A2 -CYP2B6- oder CYP3A -Induktors mit FinzePla erforderlich ist, überwachen Sie den Patienten auf eine verringerte Wirksamkeit und erwägen Sie, die Dosierung der FintePla nach Bedarf zu erhöhen. Die maximale tägliche Dosierung von FintePla nicht überschreiten [siehe Dosierung und Verwaltung ].
Wenn ein starker CYP1A2 -CYP2B6- oder CYP3A -Induktor während der Erhaltungsbehandlung mit FintePla eingestellt wird WARNUNGS AND PRECAUTIONS ].
Starke CYP1A2- oder CYP2D6 -Inhibitoren
Die gleichzeitige Verabreichung von FinstePla mit starken CYP1A2- oder CYP2D6 -Inhibitoren erhöht die Fenfluramin -Plasmakonzentrationen [siehe Klinische Pharmakologie ]. If FINTEPLA is coadministered with strong CYP1A2 or CYP2D6 inhibitors the maximum daily dosage of FINTEPLA is 20 mg [see Dosierung und Verwaltung ].
Wenn ein starker CYP1A2- oder CYP2D6 -Inhibitor während der Erhaltungsbehandlung mit FinzePla abgebrochen wird, erwägen Sie eine allmähliche Erhöhung der FintePla -Dosierung der Dosis, die ohne CYP1A2- oder CYP2D6 -Inhibitoren empfohlen wird; Die maximale tägliche Dosierung von FintePla nicht überschreiten [siehe Dosierung und Verwaltung ].
Wenn FintePla mit Strippentol koadministeriert ist und ein starker CYP1A2- oder CYP2D6 -Inhibitor die maximale tägliche Dosierung von 17 mg nicht überschreitet [siehe Dosierung und Verwaltung ].
Auswirkungen von Serotoninrezeptorantagonisten
Cyproheptadin und potente 5-HT1A 5-HT1D 5-HT2A- und 5-HT2C-Serotonin-Rezeptor-Antagonisten können die Wirksamkeit von Finzepla verringern. Wenn Cyproheptadin oder potente 5-HT1A 5-HT1D 5-HT2A- oder 5-HT2C-Serotoninrezeptor-Antagonisten mit FINTEPLA-Patienten angemessen überwacht werden sollten.
Serotonerge Medikamente
Beglaubigte Verabreichung von FintePla und Arzneimitteln (z. B. SSRIS-Snris tcas mao-Inhibitoren Trazodon usw.) rezeptfreie Medikamente (z. B. Dextromethorphan) oder Kräuterzusagen (z. B. St. Johns-Wort), die Serotonin das Risiko des Serotonin-Syncroms erhöhen, [siehe [siehe St. Johns-Würze WARNUNGS AND PRECAUTIONS ]. Concomitant use of FINTEPLA is contraindicated within 14 days of taking MAOIs. Use FINTEPLA with caution in patients taking other medications that increase Serotonin.
Warnungen für FintePla
Eingeschlossen als Teil der 'VORSICHTSMASSNAHMEN' Abschnitt
Vorsichtsmaßnahmen für FintePla
Klappenherzerkrankung und pulmonale arterielle Hypertonie
FINTEPLA can cause valvular heart disease (VHD) Und pulmonary arterial hypertension (PAH). There is a known association between serotonergic drugs with 5-HT2B receptor agonist activity including fenfluramine (the active ingredient in FINTEPLA) Und valvular heart disease Und pulmonary arterial hypertension. Although no patients receiving FINTEPLA developed valvular heart disease or pulmonary arterial hypertension in clinical trials for DS Und LGS of up to 3 years in duration cases of valvular heart disease Und pulmonary arterial hypertension have been reported during use of FINTEPLA in the postmarketing setting [see Boxwarnung Und Nebenwirkungen ].
Aufgrund dieses Risikos ist eine Herzüberwachung vor der Behandlung während der Behandlung und nach der Behandlung mit FinnePla -Schluss erforderlich. Die Herzüberwachung über das Echokardiogramm kann Hinweise auf eine Herzkrankheit der Klappen und eine pulmonale arterielle Hypertonie ermitteln, bevor ein Patient beim frühen Nachweis dieser Erkrankungen symptomatisch hilft.
Überwachung
Vor Beginn der Behandlung müssen Patienten ein Echokardiogramm unterziehen, um die Herzkrankheit der Klappen und die pulmonale arterielle Hypertonie zu bewerten.
Echokardiogramme sollten alle 6 Monate und einmal 3-6 Monate nach der Behandlung mit FINTEPLA wiederholt werden.
Der Prescriber muss die Vorteile gegenüber den Risiken einer Initiierung oder fortgesetzter Behandlung mit FINTEPLA berücksichtigen, wenn eines der folgenden Anzeichen per Echo beobachtet wird:
- Klappenanomalie oder neue Anomalie über Echokardiogramm.
- VHD, wie durch milde oder größere Aorteninsuffizienz oder mittelschwere oder größere Mitralinsuffizienz mit zusätzlichen Merkmalen von VHD (z. B. Ventilverdickung oder restriktiver Ventilbewegung) angezeigt.
- PAH, wie durch erhöhtes Druck des rechten Herzens/Lungenarteriens angezeigt (PASP> 35 mm Hg).
FINTEPLA is available only through a restricted program under a REMS [see FINTEPLA REMS Program ].
FINTEPLA REMS Program
FINTEPLA is available only through a restricted distribution program called the FINTEPLA REMS program because of the risk of valvular heart disease Und pulmonary arterial hypertension [see Klappenherzerkrankung und pulmonale arterielle Hypertonie ].
Bemerkenswerte Anforderungen des FINTEPLA REMS -Programms umfassen:
- Verschreiber müssen durch Einschreibung in das FINTEPLA REMS -Programm zertifiziert werden.
- Verschreibungen müssen Patienten, die Finzepla über das Risiko einer Herzkrankheit der Klappen und der pulmonalen arteriellen Hypertonie erhalten, beraten, wie man Anzeichen und Symptome von Herzklappenerkrankungen und lungener arterieller Hypertonie erkennen kann.
- Die Patienten müssen sich für das REMS -Programm anmelden und die laufenden Überwachungsanforderungen erfüllen [siehe Klappenherzerkrankung und pulmonale arterielle Hypertonie ].
- Die Apotheke muss durch die Einschreibung in das REMS -Programm zertifiziert werden und muss nur an Patienten ausgegeben werden, die befugt sind, FINTEPLA zu erhalten.
- Großhändler und Distributoren dürfen sich nur an zertifizierte Apotheken verteilen.
Weitere Informationen finden Sie unter www.findeplarems.com oder telefonisch unter 1-877-964-3649.
Verringerte Appetit und verringerte Gewicht
FINTEPLA can cause decreases in appetite Und weight. In placebo-controlled studies for DS (Studie 1 Und Studie 2 combined) approximately 37% of patients treated with FINTEPLA reported as an adverse reaction Verringerter Appetit Und approximately 9% reported vermindertes Gewicht as compared to 8% Und 1% respectively of patients on placebo. In the placebocontrolled study for LGS (Studie 3) approximately 28% of patients treated with FINTEPLA reported as an adverse reaction Verringerter Appetit Und approximately 5% reported vermindertes Gewicht as compared to 15% Und 2% respectively of patients on placebo [see Nebenwirkungen ]. By the end of the controlled studies 19% (Studies 1 Und 2 combined) of DS patients Und 7% (Studie 3) of LGS patients treated with FINTEPLA had a measured decrease in weight of 7% or greater from their baseline weight compared to 2% (Studie 1 Und 2) Und 0% (Studie 3) of patients on placebo. This measured decrease in weight appeared to be dose-related. In the controlled studies for DS 26% of patients on FINTEPLA 0,7 mg/kg/Tag (Studie 1) 19% of patients on FINTEPLA 0,4 mg/kg/Tag in combination with stiripentol (Studie 2) Und 13% of patients taking FINTEPLA 0,2 mg/kg/Tag (Studie 1) experienced at least a 7% decrease in weight from baseline. In the controlled study for LGS 9% of patients on FINTEPLA 0,7 mg/kg/Tag (Studie 3) Und 6% of patients on FINTEPLA 0,2 mg/kg/Tag (Studie 3) experienced at least a 7% decrease in weight from baseline. Approximately half of the patients with LGS Und most patients with DS resumed the expected measured increases in weight during the open-label extension studies. Given the frequency of these adverse reactions the growth of pediatric patients treated with FINTEPLA should be carefully monitored. Weight should be monitored regularly during treatment with FINTEPLA Und dose modifications should be considered if a decrease in weight is observed.
Schläfrigkeits -Sedierung und Lethargie
FINTEPLA can cause somnolence Beruhigung Und Lethargie. In controlled studies for DS (Studie 1 Und Studie 2 combined) the incidence of somnolence Beruhigung Und Lethargie was 25% in patients treated with FINTEPLA compared with 11% of patients on placebo. In the controlled study for LGS (Studie 3) the incidence of somnolence Beruhigung Und Lethargie was 19% in patients treated with FINTEPLA compared with 16% of patients on placebo. In general these effects may diminish with continued treatment [see Nebenwirkungen ].
Andere Depressiva des Zentralnervensystems (ZNS), einschließlich Alkohol, kann diese Auswirkungen von FintePla potenzieren. Verschreibungen sollten Patienten auf Somnolence und Sedierung überwachen und den Patienten raten, Maschinen nicht zu fahren oder zu betreiben, bis sie ausreichend Erfahrung in der FintePla gesammelt haben, um zu beurteilen, ob dies ihre Fähigkeit zum Fahren oder Betrieb von Maschinen nachteilig beeinflusst.
Selbstmordverhalten und Vorstellung
Antiepileptikum (AEDs) einschließlich FintePla erhöhen das Risiko von Selbstmordgedanken oder Verhalten bei Patienten, die diese Medikamente für jegliche Indikation einnehmen. Patienten, die mit einem AED für Angaben behandelt wurden, sollten auf die Entstehung oder Verschlechterung von Selbstmordgedanken oder Verhalten für Depressionen oder ungewöhnliche Veränderungen in der Stimmung oder des Verhaltens überwacht werden.
Poolierte Analysen von 199 placebokontrollierten klinischen Studien (Mono- und Zusatztherapie) von 11 verschiedenen AEDs, die keine Finte-Pinten-Therapie umfassten, zeigten, dass Patienten, die randomisiert zu einem der AEDs randomisiert wurden, ungefähr das doppelt so doppelt so hoch wie das Risiko (angepasstes relatives Risiko 1,8 95% CI: 1,2 2,7) des Selbstizid-Denkmals oder Verhaltens des Patienten, das mit Patienten mit dem Orton randomisch angesehen wurde. In diesen Studien, die eine mediane Behandlungsdauer von 12 Wochen hatten, betrug die geschätzte Inzidenzrate des Selbstmordverhaltens oder der Vorstellung von 27863 AED-behandelten Patienten 0,43% im Vergleich zu 0,24% bei 16029 Placebo-behandelten Patienten, die einen Anstieg von ungefähr einem Fall von Suiziddenken oder Verhalten pro 530 behandelten Patienten repräsentieren. In den Studien gab es vier Selbstmorde bei medikamentenbehandelten Patienten, und keiner bei mit Placebo behandelten Patienten ist zu klein, um eine Schlussfolgerung über den Selbstmord der Arzneimitteleffekte auf den Arzneimittel zuzulassen.
Das erhöhte Risiko für Selbstmordgedanken oder Verhalten mit AEDs wurde bereits 1 Woche nach Beginn der medikamentösen Behandlung mit AEDs beobachtet und für die Dauer der Bewertung der Behandlungen bestehen. Da die meisten in die Analyse einbezogenen Studien nicht über 24 Wochen erstreckten, konnte das Risiko von Selbstmordgedanken oder Verhalten über 24 Wochen nicht bewertet werden.
Das Risiko von Selbstmordgedanken oder Verhaltensweisen war in den analysierten Daten im Allgemeinen konsistent. Die Feststellung eines erhöhten Risikos mit AEDs unterschiedlicher Wirkmechanismen und über eine Reihe von Indikationen legt nahe, dass das Risiko für alle AEDs gilt, die für jede Indikation verwendet werden. Das Risiko variierte in den analysierten klinischen Studien nicht wesentlich nach Alter (5-100 Jahre). Tabelle 3 zeigt ein absolutes und relatives Risiko durch Indikation für alle bewerteten AEDs.
Tabelle 3: Risiko von Selbstmordgedanken oder Verhaltensweisen durch Indikation für Antiepileptika in der gepoolten Analyse
| Anzeige | Placebo -Patienten mit Ereignissen pro 1000 Patienten | Drogenpatienten mit Ereignissen pro 1000 Patienten | Relatives Risiko: Inzidenz von Ereignissen bei Drogenpatienten/ Inzidenz bei Placebo -Patienten | Risikounterschied: Zusätzliche Drogenpatienten mit Ereignissen pro 1000 Patienten |
| Epilepsie | 1.0 | 3.4 | 3.5 | 2.4 |
| Psychiatrisch | 5.7 | 8.5 | 1.5 | 2.9 |
| Andere | 1.0 | 1.8 | 1.9 | 0.9 |
| Gesamt | 2.4 | 4.3 | 1.8 | 1.9 |
Das relative Risiko für Selbstmordgedanken oder Verhalten war in klinischen Studien bei Patienten mit Epilepsie höher als bei klinischen Studien bei Patienten mit psychiatrischen oder anderen Erkrankungen, aber die absoluten Risikounterschiede waren für die Epilepsie und die psychiatrischen Indikationen ähnlich.
Jeder, der über die Verschreibung von FintePla oder einem anderen AED in Betracht gezogen wird, muss das Risiko von Selbstmordgedanken oder Verhaltensweisen mit dem Risiko unbehandelter Krankheiten in Einklang bringen. Epilepsie und viele andere Krankheiten, für die AEDs verschrieben werden, sind selbst mit Morbidität und Mortalität und einem erhöhten Risiko für Selbstmordgedanken und Verhalten verbunden. Sollten während der Behandlung Selbstmordgedanken und Verhalten auftreten, ob das Auftreten dieser Symptome bei einem bestimmten Patienten mit der Behandlung der Krankheit zusammenhängt.
Entzug von Antiepileptika
Wie bei den meisten AEDs sollte FinstePla aufgrund des Risikos einer erhöhten Anfallsfrequenz und des Status epilepticus allmählich zurückgezogen werden. Wenn ein Entzug erforderlich ist, kann aufgrund einer schwerwiegenden nachteiligen Reaktion ein schnelles Absetzen in Betracht gezogen werden.
Serotons Syndrom
Serotonin-Syndrom Eine potenziell lebensbedrohliche Erkrankung kann bei FintePla auftreten, insbesondere bei gleichzeitiger Verabreichung von FintePla mit anderen serotonergen Arzneimitteln, einschließlich, aber nicht auf selektive Serotonin-Norephrin-Wiederfassungs-Röten-Inhibitoren (SSSRIS) -Trizien (SSRIS) -Tricyclic-Tricyclic-Tricyclic. Antidepressiva (TCAS) BUPROPRION TRYPTANS Nahrungsergänzungsmittel (z. B. St. Johns Worttryptophan) Medikamente, die den Stoffwechsel von Serotonin (einschließlich Monoaminoxidase -Inhibitoren [Maois] beeinträchtigen, die mit FintePla kontraindiziert sind [siehe Kontraindikationen ] Dextromethorphan Lithiumtramadol und Antipsychotika mit serotonerger agonistischer Aktivität. Die Patienten sollten auf die Entstehung von Anzeichen und Symptomen des Serotonin -Syndroms überwacht werden, zu denen autonomische Instabilität des psychischen Status (z. B. Agitation Halluzinationen) gehören (z. Wenn das Serotonin -Syndrom vermutet wird, sollte die Behandlung mit FintePla sofort gestoppt werden und die symptomatische Behandlung begonnen werden.
Blutdruckerhöhung
FINTEPLA can cause an increase in blood pressure [see Nebenwirkungen ]. Rare cases of significant elevation in blood pressure including hypertensive crisis has been reported in adult patients treated with fenfluramine including patients without a history of hypertension. In clinical trials of up to 3 years in duration no pediatric or adult patient receiving FINTEPLA developed a hypertensive crisis. Monitor blood pressure in patients treated with FINTEPLA.
Glaukom
Fenfluramin kann zu Mydriasis führen und den Winkelverschluss auslösen Glaukom . Erwägen Sie, die Behandlung mit FintePLA bei Patienten mit akuter Sehschärfe oder Augenschmerzen abzuschließen.
Patientenberatungsinformationen
Raten Sie dem Patienten, die von der FDA zugelassene Patientenkennzeichnung zu lesen ( Medikamentenhandbuch Und Instructions for Use ).
Verwaltungsinformationen
Beraten Sie Patienten, deren FintePla die von der Apotheke bereitgestellten oralen Dosierspritzen verschrieben haben [siehe Dosierung und Verwaltung Und Anweisungen zur Verwendung ]. Instruct patients to discard any unused FINTEPLA 3 months after first opening the bottle or if the discard after date on the dispensing bottle has passed whichever is sooner [see Wie geliefert ].
Klappenherzerkrankung und pulmonale arterielle Hypertonie
Beraten Sie den Patienten, dass die Herzüberwachung unter Verwendung der Echokardiographie durchgeführt werden muss, um schwerwiegende Herzklappenveränderungen oder Bluthochdruck in den Arterien der Lunge zu überwachen [siehe WARNUNGS AND PRECAUTIONS ].
FINTEPLA REMS Program
FINTEPLA is available only through a restricted program called the FINTEPLA REMS program [see WARNUNGS AND PRECAUTIONS ]. Inform the patient of the following notable requirements:
- Die Patienten müssen sich für das Programm anmelden und die anhaltenden Anforderungen an die Echokardiogrammüberwachung entsprechen [siehe WARNUNGS AND PRECAUTIONS ].
FINTEPLA is only prescribed by certified health care providers Und only dispensed from certified pharmacies participating in the program. Therefore provide patients with the telephone number Und website for information on how to obtain the product [see WARNUNGS AND PRECAUTIONS ].
Verringerte Appetit und verringerte Gewicht
Beraten Sie den Patienten, die der Appetit verringern WARNUNGS AND PRECAUTIONS ].
Schläfrigkeits -Sedierung und Lethargie
Informieren Sie die Patienten, dass FinstePla Säuglings -Sedierung und Lethargie verursachen kann. VORSICHT -Patienten vor dem Betrieb gefährlicher Maschinen, einschließlich Kraftfahrzeugen, bis sie einigermaßen sicher sind, dass FinstePla sie nicht nachteilig beeinflusst (z. B. Beeinträchtigung des Urteils Denken oder motorischen Fähigkeiten) [siehe WARNUNGS AND PRECAUTIONS ].
Selbstmorddenken und Verhalten
Anwältigen Patienten ihre Betreuer und ihre Familien, dass Antiepileptika das Risiko von Selbstmordgedanken und Verhalten erhöhen und ihnen empfehlen, auf die Entstehung oder Verschlechterung von Symptomen von Depressionen auf ungewöhnliche Veränderungen in der Stimmung oder des Verhaltens oder der Entstehung von Selbstmut zu Verhalten oder Gedanken des Selbstverletzung aufmerksam zu machen. Weisen Sie die Pflegepersonen und Familien an, Verhaltensweisen der Anbieter von Anbietern sofort zu melden [siehe WARNUNGS AND PRECAUTIONS ].
Entzug von Antiepileptika (AEDs)
Beraten Sie den Patienten, die Verwendung von FintePla nicht abzunehmen, ohne sich mit ihrem Gesundheitsdienstleister zu wenden. FinstePla sollte normalerweise allmählich zurückgezogen werden, um das Potenzial für eine erhöhte Anfallsfrequenz und den Status epilepticus zu verringern [siehe Dosierung und Verwaltung Und WARNUNGS AND PRECAUTIONS ].
Serotons Syndrom
Informieren Sie die Patienten über das Risiko eines Serotonin-Syndroms, das lebensbedrohlich sein kann. Beraten Sie den Patienten über die Anzeichen und Symptome des Serotonin-Syndroms und dass bestimmte rezeptfreie Medikamente und Kräuterpräparate dieses Risiko erhöhen können [siehe WARNUNGS AND PRECAUTIONS ].
Blutdruckerhöhung
Informieren die Patienten, dass FinstePla zu einem Anstieg des Blutdrucks führen kann [siehe WARNUNGS AND PRECAUTIONS ].
Glaukom
Informieren Sie die Patienten, dass FinstePla Mydriasis verursachen und das Glaukom des Winkelverschlusses ausführen kann.
Weisen Sie die Patienten an, ihren Gesundheitsdienstleister zu kontaktieren, wenn sie eine akute Abnahme der Sehschärfe oder Augenschmerzen aufweisen [siehe WARNUNGS AND PRECAUTIONS ].
Schwangerschaftsregister
Raten Sie den Patienten, ihren Gesundheitsdienstleister zu benachrichtigen, wenn sie schwanger werden oder beabsichtigen, während der Finte -Therapie schwanger zu werden. Ermutigen Sie Frauen, die FintePla einnehmen, sich in das NANAED -Schwangerschaftsregister des nordamerikanischen Antiepileptika (NAAED) einzuschreiben, wenn sie schwanger werden.
Dieses Register sammelt Informationen über die Sicherheit von Antiepileptika während der Schwangerschaft [siehe Verwendung in bestimmten Populationen ].
Nichtklinische Toxikologie
Karzinogenese -Mutagenese -Beeinträchtigung der Fruchtbarkeit
Karzinogenese
Orale Verabreichung von Fenfluramin zu TG.Rash2-Mäusen (0 4,3 13,0 34,6 oder 51,8 mg/kg/Tag) für 26 Wochen und männliche und weibliche Ratten (0 0,9 2,2 oder 6,9 mg/kg/Tag) für 89 und 97 Wochen in keiner Hinweise auf drogeninduzierte Tumoren in beiden Arten. Bei Ratten -Plasma -Expositionen (AUC) von Fenfluramin und Norfenfluramin (dem Hauptmetaboliten) bei der höchsten getesteten Dosis betrugen ungefähr 5 bzw. 11 -fache, die bei Menschen bei der maximal empfohlenen menschlichen Dosis (MRHD) von 26 mg/Tag.
Mutagenese
Fenfluramin war in einem negativ in vitro Bakterienmutation (AMES) -Assay und ein vergeblich Mikronukleus- und Kometenassay bei Ratten.
Beeinträchtigung der Fruchtbarkeit
Oral administration of fenfluramine (0 3.0 6.9 or 17.3 mg/kg/day) to male and female rats prior to and throughout mating and continuing in females to day 7 of gestation resulted in a decrease in fertility and increases in abnormal sperm and epithelial vacuolation of the epididymis at the highest dose tested and altered estrous cyclicity decreased corpora lutea and implantations and Erhöhte Embryolethalität in der mittleren und hohen Dosis. Diese Dosen waren mit der elterlichen Toxizität verbunden. Die No-Effect-Dosen für Nebenwirkungen auf die Fruchtbarkeit und die Fortpflanzungsleistung bei Ratten (NULL,9 bzw. 3,0 mg/kg/Tag bei Männern bzw. Frauen) waren mit Plasma Fenfluramin-Expositionen (AUC) ungefähr 3 bzw. 0,6-mal und Norfenfluramin-Expositionen ungefähr 5 bzw. 3-mal diejenigen, die sich bei den Menschen befassen.
Verwendung in bestimmten Populationen
Schwangerschaft
Schwangerschaft Exposure Registry
Es gibt ein Schwangerschafts -Expositionsregister, das die Schwangerschaftsergebnisse bei Frauen überwacht, die Antiepileptika (AEDs) wie FintePla während der Schwangerschaft ausgesetzt sind. Ermutigen Sie Frauen, die sich während der Schwangerschaft an der Bindepla einnehmen, sich in das North American Antiepileptic Drug (NAAED) -Verschwangerschaftsregister (NAAED) einzuschreiben, indem Sie die gebührenfreie Nummer 1-888-233-2334 bezeichnen oder https://www.aedpregnancyregistry.org besuchen.
Risikozusammenfassung
Es gibt keine Daten zum Gebrauch in der Fintepla bei schwangeren Frauen. Verfügbare Daten aus epidemiologischen Studien mit Fenfluramin oder Dexfenfluramin sind nicht ausreichend, um ein drogenassoziiertes Risiko von schwerwiegenden Geburtsfehlern Fehlgeburt oder anderen negativen nachteiligen oder fetalen Ergebnissen zu bewerten. FinstePla kann einen verringerten Appetit und ein verringertes Gewicht verursachen [siehe WARNUNGS AND PRECAUTIONS ]; Überwachen Sie eine angemessene Gewichtszunahme während der Schwangerschaft. In der Verabreichung von Fenfluramin während der Organogenese (Ratte und Kaninchen) oder während der gesamten Schwangerschaft und der Laktation (Ratte) führten Daten ).
Das geschätzte Hintergrundrisiko für schwere Geburtsfehler und Fehlgeburt für die angegebene Bevölkerung ist unbekannt. Alle Schwangerschaften haben ein Hintergrundrisiko von Geburtsfehler Verlust oder andere nachteilige Ergebnisse. In der US -allgemeinen Bevölkerung beträgt das geschätzte Hintergrundrisiko für größere Geburtsfehler und eine Fehlgeburt bei klinisch anerkannten Schwangerschaften 2 bis 4% bzw. 15 bis 20%.
Daten
Tierdaten
Die orale Verabreichung von Fenfluramin (0 4,5 8,6 oder 34,6 mg/kg/Tag) an schwangere Ratten während der Organogenese führte zu verminderten Körpergewichten des Fötus und zu einem deutlichen Anstieg der fetalen Missbildungen (externer viszeraler und skelettbemerkender) bei der höchsten getesteten Dosis, die mit der mütterlichen Toxizität assoziiert war. Bei der Dosis ohne Auswirkung (NULL,6 mg/kg/Tag) für Nebenwirkungen auf die Embryofetalentwicklung bei Ratten mütterlicherseitsem Plasmakonpositionen (AUC) von Fenfluramin und Norfenfluramin (der Hauptmetaboliten) waren ungefähr 2 und 5-mal diejenigen, die bei Menschen auf dem maximal empfohlenen Menschendosis (MRHD) von 26 mg/Tag (MRHD).
Die orale Verabreichung von Fenfluramin (0 4,3 8,6 13,0 mg/kg/Tag) an schwangere Kaninchen während der gesamten Organogenese führte zu einer erhöhten Embryofetalmortalität bei allen Dosen und zu einer Erhöhung der fetalen Fehlbildungen (externer und skelettaler) bei der höchsten getesteten Dosis, die mit einer Muttertoxizität assoziiert war. Eine Dosis ohne Adverse-Wirkung für nachteilige Auswirkungen auf die Embryofetalentwicklung bei Kaninchen wurde nicht identifiziert. Bei der niedrigsten Dosis, die in Kaninchen (NULL,3 mg/kg/Tag) getestet wurde, waren mütterliche Plasma -Expositionen von Fenfluramin und Norfenfluramin niedriger als bei Menschen am MRHD.
Die orale Verabreichung von Fenfluramin (0 4,3 86 oder 34,6 mg/kg/Tag) an weibliche Ratten während der Schwangerschaft und der Laktation führte zu deutlichen Erhöhungen von stilebürtigen Welpen und neonataler Nachkommen Todesfälle bei der höchsten Dosis getestet und verzögertes Wachstum und die Entwicklung der Vorabbeugung während der Vorwäschezeit bei aller Dosen. Die Gewichtszunahme der Mütter in allen Dosen während der Schwangerschaft und bei den beiden höchsten Dosen während der Laktation wurde verringert. Eine Dosis ohne Effekt für nachteilige Auswirkungen auf die Entwicklung vor und postnatal bei Ratten wurde nicht bestimmt. Bei der niedrigsten Dosis, die bei Ratten (NULL,3 mg/kg/Tag) getestet wurde, betrugen mütterliche Plasma -Expositionen von Fenfluramin und Norfenfluramin ungefähr 0,5 bzw. dreimal diejenigen beim Menschen am MRHD.
Stillzeit
Risikozusammenfassung
Es gibt keine Daten zum Vorhandensein von Fenfluramin oder seinen Metaboliten in der Muttermilch die Auswirkungen auf das gestillte Kind oder die Auswirkungen auf die Milchproduktion.
Die Entwicklungs- und gesundheitlichen Vorteile des Stillens sollten zusammen mit dem klinischen Bedürfnis nach müttern und dem mütterlichen Bedürfnis nach Finstern und potenziellen nachteiligen Auswirkungen auf das gestillte Kind aus der Fintepla oder aus dem zugrunde liegenden mütterlichen Zustand berücksichtigt werden.
Frauen und Männer des Fortpflanzungspotentials
Unfruchtbarkeit
In Tierstudien führte die orale Verabreichung von Fenfluramin bei Männern und Frauen in klinisch relevanten Dosen in Gegenwart einer elterlichen Toxizität zu unerwünschten Fortpflanzungseffekten [siehe Nichtklinische Toxikologie ].
Pädiatrische Verwendung
Die Sicherheit und Wirksamkeit von FintePla für die Behandlung von mit DS und LGs im Zusammenhang mit DS und LGs wurden bei Patienten 2 Jahre und älter eingerichtet.
Die Verwendung von FintePla zur Behandlung von mit DS verbundenen Anfällen bei Patienten 2 Jahre und älter wird durch zwei randomisierte doppelblinde, placebokontrollierte Studien bei 202 Patienten im Alter von 2 bis 18 Jahren unterstützt. Die Verwendung von FintePla zur Behandlung von mit LGs verbundenen Anfällen wird durch eine randomisierte doppelblinde placebokontrollierte Studie an 263 Patienten im Alter von 2 bis 35 Jahren, einschließlich 187 Patienten weniger als 18 Jahre, unterstützt [siehe Boxwarnung WARNUNGS AND PRECAUTIONS Nebenwirkungen Und Klinische Studien ].
FINTEPLA can cause decreases in appetite Und weight. The growth of pediatric patients treated with FINTEPLA should be carefully monitored.
Sicherheit und Wirksamkeit bei Patienten mit weniger als 2 Jahren wurden nicht festgestellt.
Jugendliche Tierdaten
Die orale Verabreichung von Fenfluramin (0 3,0 78 oder 17,3 mg/kg/Tag) an junge Ratten, die 10 Wochen lang am postnatalen Tag 7 waren, führte zu einem verringerten Körpergewicht und neurobehavioralen Veränderungen (verringerte lokomotorische Aktivität sowie Lern- und Gedächtnisdefiziten), die alle getesteten Dosen getestet wurden. Neurobehaviorale Wirkungen blieben nach dem Abbruch der Dosierung bestehen. Die Knochengröße wurde in der mittleren und hohen Dosen verringert; Die Gehirngröße wurde bei der höchsten Dosis verringert. Für diese Endpunkte wurde eine teilweise oder vollständige Genesung beobachtet. Eine Dosis ohne Effekt für die postnatale Entwicklungstoxizität wurde nicht identifiziert. Die niedrigste getestete Dosis (NULL,0 mg/kg/Tag) war mit Plasma -Fenfluramin -Expositionen (AUC) weniger als die beim Menschen mit der maximal empfohlenen menschlichen Dosis (MRHD) von 26 mg/Tag und Norfenfluramin (Metabolite) (MRHD) ungefähr zweimal 2 -mal das, was im Menschen im Menschen im Menschen im Menschen im Menschen im Menschen im Menschen ist.
Geriatrische Verwendung
In klinischen Studien mit FintePla zur Behandlung von DS oder LGS wurden Patienten nicht 65 Jahre und Over eingeschlossen, um festzustellen, ob sie anders als jüngere Patienten reagieren. Im Allgemeinen sollte die Dosisauswahl für einen älteren Patienten vorsichtig sein, normalerweise am unteren Ende des Dosierungsbereichs, der die größere Häufigkeit einer verringerten Nieren- oder Herzfunktion von Lebern und einer gleichzeitigen Erkrankung oder einer anderen medikamentösen Therapie widerspiegelt.
Hat Humira Steroide darin?
Nierenbehinderung
Bei Patienten mit geschätzter glomerulärer Filtrationsrate (EGFR) 15 bis 29 ml/min/1,73 m 2 Überschreiten Sie die maximale tägliche Dosierung von FINTEPLA von 20 mg nicht. Bei Patienten mit EGFR 15 bis 29 ml/min/1,73 m 2 Und concomitant stiripentol use do not exceed the maximum daily dosage of FINTEPLA of 17 mg [see Dosierung und Verwaltung Und Klinische Pharmakologie ].
FINTEPLA has not been studied in patients with eGFR <15 mL/min/1.73m 2 .
Hepatische Beeinträchtigung
Kombinierte molare Expositionen von Fenfluramin und Norfenfluramin waren bei Probanden mit unterschiedlichem Grade an Leberbeeinträchtigungen (Kinder-Pugh-Klasse A B und C) erhöht, was eine Dosierungsanpassung bei diesen Patienten erfordert [siehe Dosierung und Verwaltung Und Klinische Pharmakologie ].
Überdosierungsinformationen für FintePla
Überdosierung wurde im klinischen Studienprogramm in der FintePla nicht beobachtet. Überdosierung von Fenfluramin Der Wirkstoff in der FintePla wurde jedoch in höheren Dosen berichtet als in dem Programm für klinische Studien. Einige der Fälle waren tödlich. Zu den nach Überdosierungen gemeldeten Ereignisse gehören Mydriasis Tachykardie, die Zittern/Zuckenden/Muskelkrämpfe Agitation/Unruhe/Angst erhoben wurden, erhöhte Muskeltonus/Strenge/Opisthotonos -Atemnot oder Misserfolg und Anfalls. Anfallskoma und kardiorespiratorische Festnahme wurden in den meisten tödlichen Überdosierungen gemeldet.
Es gibt kein spezifisches Gegenmittel gegen die Überdosierungsreaktionen von FintePla. Im Falle einer Überdosierungsstandard -medizinische Praxis zur Behandlung von Überdosierung von Arzneimitteln sollte verwendet werden. Eine angemessene Sauerstoffversorgung und Belüftung von Atemwege sollte sichergestellt werden. Die Überwachung des Herzrhythmus und der Messung des Vitalzeichen wird empfohlen. Ein zertifiziertes Poison Control Center sollte kontaktiert werden, um aktualisierte Informationen zur Verwaltung der Überdosierung mit FintePla zu erhalten.
Kontraindikationen für FintePla
FINTEPLA is contraindicated in patients with:
- Überempfindlichkeit gegen Fenfluramin oder einen der Hilfsstoffe in der FintePla [siehe BESCHREIBUNG ]
- Gleichzeitige Verwendung oder innerhalb von 14 Tagen nach Verabreichung von Monoaminoxidase -Inhibitoren aufgrund eines erhöhten Risikos für das Serotonin -Syndrom [siehe WARNUNGS AND PRECAUTIONS ]
Klinische Pharmakologie for Fintepla
Wirkungsmechanismus
Der genaue Mechanismus, durch den Fenfluramin seine therapeutischen Wirkungen bei der Behandlung von Anfällen im Zusammenhang mit dem Dravet-Syndrom und dem Lennox-Gastaut-Syndrom ausübt, ist unbekannt. Fenfluramin und das Metabolit Norfenfluramin zeigen eine agonistische Aktivität an Serotonin-5-HT2-Rezeptoren. Es besteht eine Assoziation zwischen serotonergen Arzneimitteln mit einer agonistischen Aktivität von 5-HT2B-Rezeptor-Agonisten, einschließlich Fenfluramin und Norfenfluramin und Klappenherzerkrankung und pulmonaler arterieller Hypertonie.
Pharmakodynamik
Herzelektrophysiologie
Bei einer Dosis 4 -fache verlängerte die maximal empfohlene Dosis die FintePla das QT -Intervall nicht, wenn sie in einer erwachsenen Bevölkerung getestet wurden.
Pharmakokinetik
Die Pharmakokinetik von Fenfluramin und Norfenfluramin wurde bei gesunden Probanden bei pädiatrischen Patienten mit DS und bei pädiatrischen und erwachsenen Patienten mit LGs untersucht. Die systemische stationäre systemische Exposition (Cmax und AUC) von Fenfluramin war geringfügig größer als die Dosis über dem Dosisbereich von 13 bis 51,8 mg zweimal täglicher Fenfluramin (d. H. 1 bis 4-mal der maximal empfohlenen Dosis). Bei pädiatrischen Patienten mit DS, die bis zu einer Gesamtdosis von 26 mg Fenfluramin von 0,7 mg/kg/Tag bis zu einer Gesamtdosis von 26 mg fingen, betrug der geometrische mittlere stationäre Fenfluramin (Koeffizient der Variation) CMAX 68,0 (41%) ng/ml und AUC0-24H 1390 (44%) (44%) (44%).
Absorption
Fenfluramin hat eine Zeit bis zur maximalen Plasmakonzentration (TMAX) von 3 bis 5 Stunden im stationären Zustand. Die absolute Bioverfügbarkeit von Fenfluramin beträgt ungefähr 68-74%. Es gab keine Auswirkungen von Lebensmitteln auf die Pharmakokinetik von Fenfluramin oder Norfenfluramin.
Verteilung
Das geometrische Mittelwert (CV%) scheinbares Verteilungsvolumen (VZ/F) von Fenfluramin beträgt 11,9 (NULL,5%) l/kg nach oraler Verabreichung von FinzePla bei gesunden Probanden. Fenfluramin ist zu 50% an menschliche Plasmaproteine gebunden in vitro Und binding is independent of drug concentrations.
Beseitigung
Die Eliminierungshälfte von Fenfluramin betrug 20 Stunden und der geometrische Mittelwert (CV%) Clearance (CL/F) betrug 24,8 (29%) l/h nach oraler Verabreichung von FinzePla bei gesunden Probanden.
Stoffwechsel
Über 75% des Fenfluramins werden vor der Eliminierung hauptsächlich durch CYP1A2 CYP2B6 und CYP2D6 auf Norfenfluramin metabolisiert. Andere CYP -Enzyme, die in geringem Maße beteiligt sind, sind CYP2C9 CYP2C19 und CYP3A4/5. Sowohl Fenfluramin als auch Norfenfluramin sind pharmakologisch aktiv. Norfenfluramin wird weiter deaminiert und oxidiert, um inaktive Metaboliten zu bilden.
Ausscheidung
Der größte Teil einer oral verabreichten Dosis Fenfluramin (mehr als 90%) wird im Urin als Fenfluramin -Norfenfluramin oder andere Metaboliten mit Fenfluramin und Norfenfluramin ausgeschieden, die weniger als 25% der Gesamtzahl ausmachen; Weniger als 5% findet sich in Kot.
Spezifische Populationen
Die Auswirkung des Alters (Bereich: 2 bis 50 Jahre) Geschlecht und Rasse hatten keine klinisch bedeutsame Auswirkungen auf die Pharmakokinetik von Fenfluramin.
Patienten mit Nierenbehinderung
In einer dedizierten klinischen Studie, in der die Pharmakokinetik einer einzelnen Dosis von 0,35 mg/kg FINTEPLA bei Probanden mit schwerer Nierenbeeinträchtigung (EGFR <30 mL/min/1.73m 2 bestimmt von MDRD) und die gesunden Freiwilligen Cmax und AUC0-Inf von Fenfluramin stiegen um 20% bzw. 88%, und Cmax und AUC0-Inf von Norfenfluramin stiegen bei Probanden mit schweren Nierenbeeinträchtigungen um 13% bzw. 21% [siehe Verwendung in bestimmten Populationen ].
FINTEPLA has not been studied in patients with eGFR <15 mL/min/1.73m 2 (bestimmt durch MDRD). Es ist nicht bekannt, ob Fenfluramin oder Norfenfluramin dialyzierbar sind.
Patienten mit Leberbehinderung
In einer Studie, in der die Pharmakokinetik einer einzelnen Dosis von 0,35 mg/kg FINTEPLA bei Probanden mit leichter mittelschwerer oder schwerer Leberbeeinträchtigung (Kinder-Pugh-Klasse A B oder C) und Probanden mit normaler Leberfunktion AUC0-T von Fenfluraminen mit einer normalen Leberfunktion bei modifizierten und schweren Hepatikstörungen bei meicher und schwerwiegender Hepatik-Belastung verglichen wurde. Cmax von Fenfluramin stieg bei Probanden mit leichter mittelschwerer bzw. schwerer Leberbeeinträchtigung um 19% 16% bzw. 29%. AUC0-T von Norfenfluramin stieg bei einer mäßigen Leberbeeinträchtigung um 18% um 18% um 4% und nahm bei schwerer Leberbeeinträchtigungen um 11% ab. Cmax von Norfenfluramin nahm bei Probanden mit leichten mittelschweren bzw. schweren Leberbeeinträchtigungen um 21% 36% bzw. 45% ab. Die kombinierte Molar-AUC0-T von Fenfluramin und Norfenfluramin stieg bei Probanden mit leichten mittelschweren bzw. schweren Leberbeeinträchtigungen um 55% 56% bzw. 82%. Der kombinierte Molar -Cmax von Fenfluramin und Norfenfluramin stieg bei Probanden mit leichter mittelschwerer bzw. schwerer Leberbeeinträchtigung um 7,5% 1,3% bzw. 8%. Die maximale tägliche Dosierung der FintePla sollte bei Patienten mit einer leichten Leberbeeinträchtigung mit/ohne Strippentol plus Clobazam verringert werden. Die maximale tägliche Dosierung der FintePla sollte bei Patienten mit mittelschwerer oder schwerer Leberbeeinträchtigung ohne Strippentol plus Clobazam verringert werden [siehe Dosierung und Verwaltung Und Verwendung in bestimmten Populationen ].
Arzneimittelinteraktionsstudien
Klinische Studien
Wirkung einer einzelnen Dosis von Strippentol -Clobazam und Valproinsäure -Kombination
Die gleichzeitige Verabreichung einer einzelnen 0,7 mg/kg-Dosis FintePla mit einer einzelnen Dosis eines Strippentol-Clobazam- und Valproinsäure-Kombination in gesunden Freiwilligen erhöhte den AUC0-Inf von Fenfluramin-AUC0-Inf von 69% und verringerte sich mit 41% mit 41% und verringerte die AUC0-72-Stunden mit 41% mit 41% und dem Cmax mit 42 Stunden von Norfenfluramin mit 41% mit 41% und dem Cmax mit 42 Stunden von Norfenfluramin mit 41% und dem Cmax mit Flowfluramin mit 42% der Cmax und der Cmax mit Flowfluramin mit Flowfluramin und der CMAX mit 42 Stunden von Norfenfluramin. allein.
Auswirkung von stationärem Struktur und Clobazam mit oder ohne Valproat
Fenfluramin -pharmakokinetische Daten wurden von Patienten gesammelt, nachdem in Studie 1 mehrere Fenfluramin -Verwaltungen sowie die Modellierung und Simulation von Populationsmodellpopulationen in Studie 2 verwendet wurden, um die Wirkung von Strippentol plus Clobazam mit oder ohne Valproat auf Fenfluramin -Pharmakokinetika zu bewerten. Die Wirkung von Strippentol plus Clobazam mit oder ohne Valproat auf die Fenfluramin-Pharmakokinetik ist größer, wenn die FintePla im stationären Zustand ist als für die erste Dosis FintePla. At steady state in the patient population the coadministration of 0.1 mg/kg twice daily (0.2 mg/kg/day) maximum 17 mg/day of FINTEPLA with stiripentol plus clobazam with or without valproate is expected to result in a 166% increase in fenfluramine AUC0-24 and a 38% decrease in norfenfluramine AUC0-24 as compared to 0.2 Mg/kg/Tag maximal 26 mg/Tag FintePla -Dosis allein verabreicht [siehe Dosierung und Verwaltung Und Wechselwirkungen mit Arzneimitteln ].
Einfluss von Cannabidiol stationär
Die gleichzeitige Verabreichung einer einzelnen 0,35 mg/kg-Dosis FintePla mit wiederholten Dosen von Cannabidiol erhöhte den AUC0-Inf von Fenfluramin um 59% und den Cmax um 10% und verringerte die AUC0-INF von Norfenfluramin allein um 33% um 33%. Es wird nicht erwartet, dass diese Interaktion klinisch signifikant ist.
Wirkung starker CYP1A2- oder CYP2D6 -Inhibitoren
Die gleichzeitige Verabreichung einer einzelnen 0,35 mg/kg-Dosis FintePla mit Fluvoxamin (ein starker CYP1A2-Inhibitor) im stationären Zustand (50 mg einmal täglich) erhöhte die AUC0-Inf von Fenfluramin mit 22% und das CMAX mit 22% und minderte mit 22% das AUC0-Inf von Fenfluramin mit 22% und minderte mit 22% mit 22% das AUC0-Inf von Norfenfluramin mit 22%. Selbst verabreichte FintePla [siehe Wechselwirkungen mit Arzneimitteln ].
Die gleichzeitige Verabreichung einer einzelnen 0,35 mg/kg-Dosis FintePla mit Paroxetin (einem starken CYP2D6-Inhibitor) im stationären Zustand (30 mg einmal täglich) erhöhte den AUC0-Inf von Fenfluramin mit 81% und CMAX mit 13% und verringerte mit 13% mit 13% das AUC0-Inf von AUC0-Inf. Selbst verabreichte FintePla [siehe Wechselwirkungen mit Arzneimitteln ].
Wirkung von starken CYP1A2 CYP2B6- oder CYP3A -Induktoren
Coadministration of a single 0.35 mg/kg dose of FINTEPLA with rifampin (a CYP1A2 CYP2B6 and CYP3A inducer) at steady state (600 mg once daily) in healthy volunteers decreased the AUC0-inf of fenfluramine by 58% and the Cmax by 40% and decreased the AUC0-inf of norfenfluramine by 50% and increased the Cmax von Norfenfluramin um 13% im Vergleich zu allein verabreichtem Finstern [siehe Wechselwirkungen mit Arzneimitteln ].
Wirkung von FintePla auf andere Medikamente
Coadministration of a single 0.7 mg/kg dose of FINTEPLA with a single dose of a stiripentol clobazam and valproic acid combination did not affect the pharmacokinetics of stiripentol nor the pharmacokinetics of clobazam or its N.desmethyl-metabolite norclobazam nor the pharmacokinetics of valproic acid as compared to the stiripentol clobazam und Valproinsäure -Kombination allein. Die gleichzeitige Verabreichung einer einzelnen 0,35 mg/kg -Dosis FintePla mit wiederholten Cannabidioldosen hatte im Vergleich zu Cannabidiol allein keinen Einfluss auf die Pharmakokinetik von Cannabidiol.
In -vitro -Studien
Fenfluramin wird hauptsächlich durch CYP1A2 CYP2B6 und CYP2D6 metabolisiert in vitro . Andere CYP -Enzyme, die in geringem Maße beteiligt sind, sind CYP2C9 CYP2C19 und CYP3A4/5.
Wirkung von Fenfluramin und Norfenfluramin auf CYP -Substrate: Fenfluramin und Norfenfluramin sind keine Inhibitoren oder Induktoren von CYP1A2 CYP2B6 CYP2C8 CYP2C9 CYP2C19 CYP2D6 oder CYP3A4 bei klinisch relevanten Konzentrationen.
Wirkung von Transportern auf Fenfluramin und Norfenfluramin: Fenfluramin und Norfenfluramin sind keine Substrate der P-G BCRP OAT1 OAT3 OCT2 Mate1 oder Mate2-K-Transporter.
Wirkung von FintePla auf Transporter: Fenfluramin und Norfenfluramin sind keine Inhibitoren von p-gp bcrp oat1b1 OATP1B3 OAT1 OAT3 OCT2 Mate1 oder Mate2-K-Transporter.
Klinische Studien
Draved Syndrom
Die Wirksamkeit von FintePla für die Behandlung von mit DS verbundenen Anfällen bei DS bei Patienten 2 Jahre und älter wurde in zwei randomisierten doppelblinden placebokontrollierten Studien bei Patienten im Alter von 2 bis 18 Jahren festgelegt.
Studie 1 (N=117) compared a 0,7 mg/kg/Tag Und a 0,2 mg/kg/Tag dose of FINTEPLA with placebo in patients who were not receiving stiripentol (NCT02682927 Und NCT02826863).
Studie 2 (N=85) compared a 0,4 mg/kg/Tag dose of FINTEPLA with placebo in patients who were receiving stiripentol Und either clobazam valproate or both (NCT02926898). In both studies patients had a clinical diagnosis of DS Und were inadequately controlled on at least one AED or other antiseizure treatment including vagal nerve stimulation or a ketogenic diet. Both trials had a 6-week baseline period during which patients were required to have a minimum of 6 convulsive seizures while on stable AED therapy. Convulsive seizures included tonic clonic generalized tonic-clonic tonic-atonic secondarily generalized tonic-clonic hemiclonic Und focal with observable motor signs. The baseline period was followed by rUndomization into a 2- week (Studie 1) or 3-week (Studie 2) titration period Und a subsequent 12-week maintenance period where the dose of FINTEPLA remained stable.
In Studie 1 98% der Patienten nahmen zwischen 1 und 4 AEDs ein. Die am häufigsten verwendeten gleichzeitigen AEDs (bei mindestens 25%der Patienten) waren Valproat (61%) Clobazam (59%) und Topiramat (25%). In Studie nahmen 2 100% der Patienten zwischen 2 und 4 zu gleichzeitigen AEDs. Die am häufigsten verwendeten gleichzeitigen AEDs (bei mindestens 25%der Patienten) waren Strippentol (100%) Clobazam (94%) und Valproat (89%).
Der primäre Wirksamkeitsendpunkt in beiden Studien war die Änderung gegenüber dem Ausgangswert bei der Häufigkeit von konvulsiven Anfällen pro 28 Tage während der kombinierten 14-wöchigen (Studie 1) oder 15-wöchiger (Studie 2) Titration und Erhaltsperioden (d. H. Behandlungszeit). Das mittlere längste Intervall zwischen krampfhaften Anfällen wurde ebenfalls bewertet.
In Studie 1 und Studie 2 war die Verringerung der konvulsiven Anfallsfrequenz pro 28 Tage für alle Dosisgruppen von FINTEPLA im Vergleich zu Placebo statistisch signifikant höher (Tabelle 6). Eine Verringerung der krampfhaften Anfälle wurde innerhalb von 3 bis 4 Wochen nach Beginn der FintePla beobachtet, und der Effekt blieb im Allgemeinen über den Behandlungszeitraum von 14 oder 15 Wochen konsistent.
Tabelle 6: Veränderung der Häufigkeit der Krampfanfall
| Krampfneigungsfrequenz (pro 28 Tage) | Placebo | FINTEPLA 0,2 mg/kg/Tag | FINTEPLA 0,7 mg/kg/Tag | FINTEPLA 0,4 mg/kg/Tag |
| Studie 1 | N = 39 | N = 38 | N = 40 | N / A |
| Ausgangszeitraum Median | 29.4 | 18.1 | 18.7 | N / A |
| % Unterschied im Vergleich zu Placebo* | -31,7% | -70,0% | N / A | |
| p-Wert im Vergleich zu Placebo | 0.043 | <0.001 | ||
| Studie 2 | N = 42 | N / A | N / A | N = 43 |
| Ausgangszeitraum Median | 11.5 | N / A | N / A | 15.0 |
| % Unterschied im Vergleich zu Placebo* | N / A | -59,5% | ||
| p-Wert im Vergleich zu Placebo | <0.001 | |||
| *Abgeleitet aus dem primären Analysemodell ± Alle Patienten mit 0,4 mg/kg/Tag nahmen ebenfalls gleichzeitig ein Sturz auf Strippentol ein, was die Exposition von FintePla erhöht. |
Abbildung 1 und Abbildung 2 zeigen den Prozentsatz der Patienten nach Kategorie der Anfallsreaktion aus dem Ausgangswert bei der Häufigkeit von Krampfanfällen (pro 28 Tage) während des Behandlungszeitraums in Studie 1 und Studie 2.
Abbildung 1: Anteil der Patienten nach Kategorie der Anfallsreaktion für FintePla und Placebo bei Patienten mit Dravet -Syndrom (Studie 1)
| |
Abbildung 2: Anteil der Patienten nach Kategorie der Anfallsreaktion für FintePla und Placebo bei Patienten mit Dravet -Syndrom (Studie 2)
| |
In Studie 1 3 von 40 (8%) Patienten in der FINTEPLA-Gruppe von 0,7 mg/kg/Tag und 3 von 38 (8%) Patienten in der FINTEPLA-Gruppe von 0,2 mg/kg/Tag berichteten während der 14-wöchigen Behandlungszeit im Vergleich zu 0 Patienten in der Placebo-Gruppe keine konvulsiven Anfälle. In Studie 2 1 von 43 (2%) Patienten in der FINTEPLA-Gruppe von 0,4 mg/kg/Tag berichteten während des 15-wöchigen Behandlungszeitraums im Vergleich zu 0 Patienten in der Placebo-Gruppe keine konvulsiven Anfälle.
In Studie 1 und Studie 2 war FinstePla mit einem statistisch signifikanten längeren Intervall zwischen konvulsiven Anfällen im Vergleich zu Placebo assoziiert (Abbildung 3).
Abbildung 3: Das mediane längste Intervall zwischen krampfhaften Anfällen bei Patienten mit Dravet -Syndrom (Studie 1 und Studie 2)
| |
Lennox-Gastaut-Syndrom
Die Wirksamkeit von FintePla für die Behandlung von mit LGs im Zusammenhang mit LGs im Alter von 2 Jahren und älteren Anfällen in einer randomisierten doppelblinden, placebokontrollierten Studie an 263 Patienten 2 bis 35 Jahre wurde festgelegt (Studie 3; NCT03355209).
Studie 3 compared a 0,7 mg/kg/Tag Und a 0,2 mg/kg/Tag dose of FINTEPLA with placebo.
Die Patienten hatten eine Diagnose von LGs und wurden mindestens eine AED mit oder ohne Vagusnervstimulation und/oder ketogene Ernährung unzureichend kontrolliert. Die Studie hatte eine 4-wöchige Grundlinienzeit, in der die Patienten bei einer stabilen AED-Therapie mindestens 8 Drop-Anfälle aufweisen mussten. Tropfenanfälle waren verallgemeinerte tonic-klonische sekundär verallgemeinerte tonisch-klonische Tonic Atonic oder Tonic-Atonic-Anfälle, die bestätigt wurden, dass sie zu Tropfen führen. Auf die Basisdauer folgte eine Randomisierung in einen 2-wöchigen Titrationszeitraum und eine nachfolgende 12-wöchige Wartungszeit, in der die Dosis von FintePla stabil blieb.
In Studie nahmen 3 99% der Patienten zwischen 1 und 4 zu gleichzeitigen AEDs. Die am häufigsten verwendeten gleichzeitigen AEDs (bei mindestens 25%der Patienten) waren Clobazam (45%) Lamotrigin (34%) und Valproat (56%).
Der primäre Wirksamkeitsendpunkt in Studie 3 war der mittlere Prozentwechsel von Ausgangswert bei der Häufigkeit von Abfallanfällen pro 28 Tage während der kombinierten 14-wöchigen Titrations- und Wartungszeiträume (d. H. Die Behandlungszeit). Der Anteil der Patienten, die eine Verbesserung (minimal und sehr stark verbessert) im klinischen globalen Eindruck von Veränderungen (CGI-I) erzielen, war ein sekundärer Endpunkt.
In Studie 3 war die mediane prozentuale Veränderung gegenüber dem Ausgangswert (Reduktion) der Häufigkeit der Abfallanfälle pro 28 Tage für die Dosisgruppe von 0,7 mg/kg/Tag im Vergleich zu Placebo signifikant höher (Tabelle 7). Eine Verringerung der Abfallanfälle wurde innerhalb von 2 Wochen nach der Initiierung der Behandlung mit FinstePla beobachtet, und der Effekt blieb im Allgemeinen über den 14-wöchigen Behandlungszeitraum im Allgemeinen konsistent.
Die durchschnittliche prozentuale Reduktion von Ausgangswert bei der Abfallannahmefrequenz pro 28 Tage für die niedrigere Finanzdosis an FintePla (NULL,2 mg/kg/Tag) erreichte im Vergleich zu Placebo keine statistische Signifikanz (Tabelle 7).
Tabelle 7: Änderung der Abfallanschlagsfrequenz während des Behandlungszeitraums bei Patienten mit dem Lennox-Gastaut-Syndrom (Studie 3)
| Frequenz der Anfallsnfall (pro 28 Tage) | Placebo | FINTEPLA 0,2 mg/kg/Tag | FINTEPLA 0,7 mg/kg/Tag |
| Studie 3 | N = 85* | N = 86* | N = 83* |
| Ausgangszeitraum Median Beschlagnahme Frequency | 55.0 | 77.8 | 80.0 |
| Mediane prozentuale Änderung gegenüber dem Ausgangswert während der Behandlung | -8,7% | -13,2% | -23,7% |
| p-Wert im Vergleich zu Placebo | 0,1917 | 0.0037 | |
| *Die Gesamtzahl der Patienten, auf denen die Wirksamkeitsanalyse basiert, ist geringer als die Gesamtzahl, die in der doppelblinden placebokontrollierten Studie randomisiert wurde, da Patienten mit fehlenden Daten von der Wirksamkeitsanalyse ausgeschlossen wurden. |
Abbildung 4 zeigt den Prozentsatz der Patienten nach Reduktionskategorie von Ausgangswert bei der Abfallanfallungshäufigkeit pro 28 Tage während des Behandlungszeitraums in Studie 3.
Abbildung 4: Anteil der Patienten nach Kategorie der Anfallsreaktion für FintePla und Placebo bei Patienten mit Lennox.Gastaut -Syndrom (Studie 3)
| |
Numerisch größere Verbesserungen des CGI-I durch Forscher wurden bei Patienten beobachtet, die im Vergleich zu Placebo behandelt wurden.
Patienteninformationen für FintePla
FINTEPLAR ®
(Fin-Tep-La)
(Fenfluramin) Mundlösung
Lesen Sie diesen Medikamentenhandbuch, bevor Sie anfangen, FinstePla zu nehmen, und jedes Mal, wenn Sie eine Nachfüllung erhalten. Es kann neue Informationen geben. Diese Informationen treten nicht an den Platz, mit Ihrem Gesundheitsdienstleister über Ihre Krankheit oder Behandlung zu sprechen.
Was sind die wichtigsten Informationen, die ich über FinstePla wissen sollte?
FINTEPLA can cause serious side effects including :
1. Probleme mit den Klappen im Herzen (Klappenherzerkrankung) und Bluthochdruck in den Arterien der Lunge (pulmonale arterielle Hypertonie) wurden mit FintePla in Verbindung gebracht. Ihr Gesundheitsdienstleister wird einen Test namens Echokardiogramm durchführen, um Ihr Herz zu überprüfen, und für hohen Blutdruck in den Arterien der Lungen, bevor Sie während der Behandlung und einmal 3 bis 6 Monate nach der Einnahme Ihrer letzten Dosis an der Luft in der Luft in der Nähe anfangen.
Rufen Sie Ihren Gesundheitsdienstleister sofort an, wenn Sie diese Anzeichen und Symptome von Herz- oder Lungenproblemen während der Behandlung mit FINTEPLA entwickeln:
- Kurzatmigkeit
- Brustschmerzen
- Müdigkeit oder Schwäche
- Empfindungen eines schnellen flatternden Herzschlags
- insbesondere bei erhöhter Aktivität (Herzklopfen)
- Benommenheit or Ohnmacht
- unregelmäßiger Puls
- geschwollene Knöchel oder Füße
- bläuliche Farbe zu Ihren Lippen und Haut (Cyanose)
Aufgrund des Risikos von Herzklappenproblemen (Klappenherzerkrankung) und Bluthochdruck in Arterien von Lungen (pulmonaler arterieller Hypertonie) ist FINTEPLA nur über ein eingeschränktes Programm als REM -Programm (FINTEPLA -Risikobewertung und -minderungsstrategie) erhältlich. Bevor Sie oder Ihr Kind FINTEPLA erhalten, stellt Ihr Gesundheitsdienstleister oder Apotheker sicher, dass Sie verstehen, wie Sie FintePla sicher einnehmen. Wenn Sie Fragen zu FINTEPLA haben, fragen Sie Ihrem Gesundheitsdienstleister unter www.finsteplarems.com oder telefonisch unter 1-877-964-3649.
2. Verringerte Appetit und verringerte Gewicht. Verringerter Appetit Und vermindertes Gewicht are both serious Und common side effects of FINTEPLA in people with Dravet syndrome (DS) or Lennox-Gastaut syndrome (LGS).
- Ihr Gewicht sollte regelmäßig während Ihrer Behandlung mit FintePla überprüft werden.
- Ihr Gesundheitsdienstleister muss möglicherweise Änderungen an Ihrer FintePla -Dosis vornehmen, wenn Ihr Gewicht abnimmt. In einigen Fällen muss FINTEPLA möglicherweise gestoppt werden.
3. Schläfrigkeit Sedierung und Energiemangel (Lethargie). Dies sind sowohl schwerwiegende als auch häufige Nebenwirkungen von FinstePla bei Menschen mit Dravet-Syndrom (DS) oder Lennox-Gastaut-Syndrom (LGS). Die Einnahme von FinnePla mit Depressiva des Zentralnervensystems (ZNS), einschließlich Alkohol, kann die Schläfrigkeit erhöhen. Fahren Sie nicht mit schweren Maschinen oder führen Sie andere gefährliche Aktivitäten aus, bis Sie wissen, wie sich die FintePla auf Sie auswirkt.
4. Wie alle anderen Antiepileptika kann finnepla bei einer sehr kleinen Anzahl von Menschen Selbstmordgedanken oder Handlungen verursachen (ca. 1 zu 500).
Rufen Sie Ihren Gesundheitsdienstleister sofort an, wenn Sie eines dieser Symptome haben, insbesondere wenn sie neuer sind, oder Sie besorgen Sie:
- Gedanken über Selbstmord oder Sterben
- Neue oder schlechtere Angst
- Probleme beim Schlafen (Schlaflosigkeit)
- auf gefährliche Impulse wirken
- Versuche, Selbstmord zu begehen
- aufgeregt oder unruhig fühlen
- Neue oder schlechtere Reizbarkeit
- Eine extreme Zunahme von Aktivität und Reden (Manie)
- Neue oder schlechtere Depression
- Panikattacken
- aggressiv handeln, wütend oder gewalttätig zu sein
- Andere ungewöhnliche Verhaltensänderungen in Verhalten oder Stimmung
Wie kann ich nach frühen Symptomen von Selbstmordgedanken und Handlungen achten?
- Achten Sie auf Änderungen, insbesondere plötzliche Veränderungen im Stimmungsverhalten Gedanken oder Gefühle.
- Führen Sie alle Follow-up-Besuche bei Ihrem Gesundheitsdienstleister wie geplant.
Selbstmordgedanken oder Handlungen können durch andere Dinge als Medikamente verursacht werden. Wenn Sie Selbstmordgedanken oder Handlungen haben, kann Ihr Gesundheitsdienstleister nach anderen Ursachen überprüfen.
5. Hören Sie nicht auf, FinstePla zu nehmen, ohne zuerst mit Ihrem Gesundheitsdienstleister zu sprechen. Wenn Sie ein Anfallsmedizin wie FintePla stoppen, können Sie plötzlich öfter Anfälle oder Anfälle haben, die nicht aufhören (Status epilepticus).
Rufen Sie Ihren Gesundheitsdienstleister zwischen den Besuchen nach Bedarf an, insbesondere wenn Sie sich Sorgen um Symptome machen.
Was ist FINTEPLA?
- FINTEPLA is a prescription medicine used to treat the seizures associated with Dravet syndrome (DS) Und Lennox- Gastaut syndrome (LGS) in patients 2 years of age Und older.
- Es ist nicht bekannt, ob FinstePla bei Kindern im Alter von weniger als 2 Jahren sicher und wirksam ist.
Nehmen Sie keine Fintepla, wenn Sie:
- sind allergisch gegen Fenfluramin oder einen der Zutaten in der Fintepla. Das Ende dieses Medikamentenleitfadens finden Sie in einer vollständigen Liste von Zutaten in der FintePla.
- Nehmen oder haben in den letzten 14 Tagen die Einnahme von Medikamenten einnehmen, die als Monoaminoxidase -Inhibitoren (MAOI) bezeichnet werden. Dies kann ein schwerwiegendes oder lebensbedrohliches Problem verursachen, das als Serotonin-Syndrom bezeichnet wird. Wenn Sie nicht sicher sind, ob Sie einen dieser Arzneimittel einnehmen oder nicht, wenden Sie sich an Ihren Gesundheitsdienstleister.
Bevor Sie FINTEPLA nehmen, teilen Sie Ihrem Gesundheitsdienstleister alle Ihre medizinischen Erkrankungen mit, einschließlich, wenn Sie:
- Herzprobleme haben
- Gewichtsverlust haben oder
- Depression Stimmungsprobleme oder Selbstmordgedanken oder Verhalten hatten oder hatte
- Nierenprobleme haben
- Leberprobleme haben
- sind schwanger oder planen, schwanger zu werden. Teilen Sie Ihrem Gesundheitsdienstleister sofort mit, wenn Sie während der Einnahme von BINTEPLA schwanger werden. Sie und Ihr Gesundheitsdienstleister entscheiden, ob Sie während der Schwangerschaft FintePla einnehmen sollten.
- Wenn Sie schwanger werden, während Sie BINTEPLA mit Ihrem Gesundheitsdienstleister über die Registrierung mit dem Nordamerika -Schwangerschaftsregister des Antiepileptika -Arzneimittels sprechen. Sie können sich in dieser Registrierung unter 1-888-233-2334 anmelden oder unter www gehen.
- AedpregnancyRegistry.org. Der Zweck dieses Registers ist es, Informationen über die Sicherheit von Antiepileptika während der Schwangerschaft zu sammeln.
- stillen oder planen zu stillen. Es ist nicht bekannt, ob FintePla in Ihre Muttermilch übergeht. Sprechen Sie mit Ihrem Gesundheitsdienstleister darüber, wie Sie Ihr Baby am besten füttern können, während Sie die Fintepla einnehmen.
Teilen Sie Ihrem Gesundheitsdienstleister über alle Medikamente, die Sie einnehmen einschließlich verschreibungspflichtiger und rezeptfreier Medikamente Vitamine und Kräuterpräparate.
Kennen Sie die Medikamente, die Sie einnehmen. Halten Sie eine Liste von ihnen, um Ihren Gesundheitsdienstleister oder Apotheker zu zeigen, wenn Sie ein neues Medikament erhalten.
Wie soll ich FINTEPLA einnehmen?
- Lesen Sie die Anweisungen zur Verwendung Am Ende dieses Medikamentenhandbuchs finden Sie Informationen zum richtigen Weg zur Verwendung von FintePla.
- Nehmen Sie FINTEPLA genau so, wie Ihr Gesundheitsdienstleister Ihnen sagt, dass Sie es nehmen sollen.
- Ihr Gesundheitsdienstleister wird Ihnen sagen, wie viel FINTEPLA Sie nehmen und wann Sie es nehmen sollen.
- FINTEPLA may be taken with or without food.
- Messen Sie Ihre Dosis FintePla mit der von der Apotheke bereitgestellten Dosierspritze. Verwenden Sie keinen Haushaltslöffel oder Esslöffel.
- FINTEPLA can be given through gastric Und nasogastric feeding tubes
Was soll ich vermeiden, während ich FintePla einnehme?
- Nicht Fahrt betreiben schwere Maschinen oder führen Sie andere gefährliche Aktivitäten aus, bis Sie wissen, wie sich FintePla auf Sie auswirkt. FINTEPLA kann dazu führen, dass Sie sich schläfrig fühlen.
Was sind die möglichen Nebenwirkungen von FintePla?
FINTEPLA may cause serious side effects including:
Rufen Sie Ihren Gesundheitsdienstleister sofort an, wenn Sie eines der folgenden Symptome des Serotonin -Syndroms haben.
- Siehe Was sind die wichtigsten Informationen, die ich über FintePla wissen sollte?
- Serotonin syndrome. Das Serotonin-Syndrom ist ein lebensbedrohliches Problem, das bei Menschen auftreten kann, insbesondere wenn FINTEPLA mit bestimmten anderen Medikamenten eingenommen wird, um Folgendes zu umfassen:
- Antidepressiva-Medikamente, die SSRIS SNRIS TCAs und Maois genannt werden
- St. Johns Würze
- Tryptophan
- Dextromethorphan
- Lithium
- Tramadol
- Antipsychotika
- Veränderungen im psychischen Status, z. B. Dinge, die nicht dort sind (Halluzinationen), oder des Komas
- Schneller Herzschlag
- Übelkeit erbrechen Durchfall
- Blutdruckänderungen
- hohe Körpertemperatur
- enge Muskeln
- Probleme beim Gehen
- Bluthochdruck (Bluthochdruck). Bluthochdruck ist sowohl eine schwerwiegende als auch eine gemeinsame Nebenwirkung. FinstePla kann dazu führen, dass Ihr Blutdruck zunimmt, auch wenn Sie noch nie einen hohen Blutdruck hatten. Ihr Gesundheitsdienstleister überprüft Ihren Blutdruck, während Sie FintePla einnehmen.
- Erhöhter Druck in Ihrem Auge (Glaukom). Zu den Symptomen des Glaukoms können gehören:
- rote Augen
- Verringertes Sehen
- Halos oder leuchtende Farben um Licht sehen
- Augenschmerzen oder Beschwerden
- Übelkeit oder Erbrechen
- verschwommenes Sehen
Wenn Sie eines dieser Symptome haben, rufen Sie Ihren Gesundheitsdienstleister sofort an.
Die häufigsten Nebenwirkungen von FinstePla bei der Behandlung zur Behandlung von Dravet -Syndrom (DS) sind:
- Verringerter Appetit
- Durchfall
- Niedrige Energie
- Schläfrigkeit
- Probleme mit der Bewegungs Balance und Gehen
- Erhöhtes Sabbern
- Atemwegsinfektion
- Erhöhter Blutdruck
- vermindertes Gewicht
- Erbrechen
- Fieber
- Falls
- Verstopfung
- Anfälle, die nicht aufhören
- Abnormale Echokardiogramm
- Schwäche
Zu den häufigsten Nebenwirkungen von FinstePla, wenn sie zur Behandlung von Lennox-Gastaut-Syndrom (LGS) verwendet werden, gehören:
- Durchfall
- Müdigkeit
- Erbrechen
- Schläfrigkeit
- Verringerter Appetit
Dies sind nicht alle möglichen Nebenwirkungen von FintePla. Weitere Informationen finden Sie in Ihrem Gesundheitsdienstleister oder Apotheker.
Sagen Sie Ihrem Gesundheitsdienstleister, wenn Sie einen Nebeneffekt haben, der Sie stört oder der nicht verschwindet.
Rufen Sie Ihren Arzt an, um medizinische Beratung zu Nebenwirkungen zu erhalten. Sie können die FDA bei 1-800-FDA-1088 Nebenwirkungen melden.
Wie soll ich FINTEPLA aufbewahren?
- Lagern Sie FinstePla bei Raumtemperatur zwischen 68 ° F und 77 ° F (25 ° C).
- Nicht kühlen oder einfrieren.
- Lagern Sie die FINTEPLA -Flasche und spritzen Sie zusammen in einem sauberen Bereich.
- Werfen Sie alle nicht verwendeten FintePla weg (verwerfen) 3 Monate nach dem ersten Öffnen der Flasche oder wenn das Verwerfen nach dem Datum auf dem Paket oder der Flasche vergangen ist. Was auch immer man an erster Stelle kommt.
Halten Sie FintePla und alle Medikamente außerhalb der Reichweite der Kinder.
Allgemeine Informationen über den sicheren und effektiven Einsatz von FintePla.
Medikamente werden manchmal für andere Zwecke als die in einem Medikamentenhandbuch aufgeführten Zwecke verschrieben. Verwenden Sie keine FintePla für einen Zustand, für den sie nicht verschrieben wurde. Geben Sie anderen Menschen keine Fintepla, auch wenn sie die gleichen Symptome haben, die Sie haben. Es kann ihnen schaden.
Sie können Ihren Apotheker oder Gesundheitsdienstleister um Informationen über FinstePla bitten, die für Angehörige der Gesundheitsberufe geschrieben wurden.
Was sind die Zutaten in der FintePla?
Wirkstoff: Fenfluraminhydrochlorid
Inaktive Zutaten: Kirschgeschmack Zitronensäure Ethylparabenhydroxyethylcellulose Methylparaben Kaliumcitrat -Sucralose und Wasser.
FINTEPLA contains no ingredient made from gluten-containing grain (wheat barley or rye) Und contains not more than 0.1% of Kohlenhydrate das ist aus dem Kirschgeschmack.
Dieser Medikamentenführer wurde von der US -amerikanischen Food and Drug Administration zugelassen.
Anweisungen zur Verwendung
FINTEPLA ®
(Fin-Tep-La)
(Fenfluramin) Mundlösung 2.2 mg/mL
Stellen Sie sicher, dass Sie verstehen und befolgen Sie diese Anweisungen, bevor Sie anfangen, die mündliche FINTEPLA -Lösung zu verwenden, und jedes Mal, wenn Sie eine Nachfüllung erhalten. Es kann neue Informationen geben.
Diese Verwendungsanweisungen enthält Informationen zur Einnahme von FINTEPLA. Diese Informationen treten nicht an den Platz, mit Ihrem Gesundheitsdienstleister über Ihre Krankheit oder Behandlung zu sprechen.
Was ist in FINTEPLA enthalten?
Die folgenden Elemente sind enthalten, um eine mündliche Dosis FintePla vorzubereiten und zu geben:
- 1 Flasche FintePla Orallösung (NULL,2 mg/ml)
- 2 wiederverwendbare orale Spritzen
| |
Rufen Sie den Apotheker unter 1-844-288-5007 an, wenn Sie die oben aufgeführten Elemente nicht erhalten haben oder wenn Sie Hilfe verwenden.
Wichtige Informationen über FintePla
- FINTEPLA is an oral medicine (taken by mouth) Und is given 2 mal jeden Tag . Befolgen Sie Ihre Anweisungen für die Gesundheitsdienstleister, um Dosen in der Fintepla zu nehmen oder zu geben.
- Wenn Sie Fragen zur Vorbereitung oder Erstellung von FintePla haben, wenden Sie sich an Ihren Gesundheitsdienstleister oder rufen Sie Ihren Apotheker an.
- Verwenden Sie immer die oralen Spritzen, die mit FintePla versehen sind, um sicherzustellen, dass die richtige Dosis angegeben ist. Wenn Sie eine neue Spritze benötigen, wenden Sie sich an Ihren Apotheker. Nicht Verwenden Sie einen Haushaltslöffel oder einen Esslöffel.
Orale Spritzen mit der Apotheke mit FintePla versehen.
Mit FINTEPLA erhalten Sie 2 wiederverwendbare orale Spritzen.
2 Mundspritzen, die bis zu 3 ml messen können
ODER
2 orale Spritzen, die bis zu 6 ml messen können
| |
Rufen Sie den Apotheker unter 1-844-288-5007 an, wenn Sie Fragen zu den Spritzen mit FinzePla haben.
Teile der oralen Spritze
| |
Vorbereitung einer Dosis
Schritt 1 . Stellen Sie sicher, dass Sie:
- Die Flasche Finnepla Mundlösung und
- Eine saubere, trockene wiederverwendbare orale Spritze, die mit FintePla versorgt wurde.
Schritt 2. Überprüfen Sie den Abwurf nach Datum (MM/DD/JJJJ).
| |
- Nicht Verwenden Sie das Arzneimittel, wenn das Datum des Wurfverlusts (Verrückte) vergangen ist.
- Wenn sich das Datum in der Nähe von Ihrer Apotheke oder Ihrem Gesundheitsdienstleister befindet, um eine Nachfüllung oder ein neues Rezept zu erhalten.
- Wenn das Datum verabschiedet wurde, entsorgen Sie nicht genutzte Fintepla.
Schritt 3. Drücken Sie nach unten und drehen Sie die kindersichere Kappe nach links (gegen den Uhrzeigersinn) und entfernen Sie sie aus der Flasche.
- Stellen Sie die Kappe beiseite (werfen Sie nicht weg).
| |
Schritt 4. Stellen Sie sicher, dass sich der Adapter auf der Flasche befindet.
- Wenn die Flasche keinen Adapter hat, wenden Sie sich an den Apotheker.
- Lassen Sie den Adapter immer an Ort und Stelle in der Flasche Medizin.
| |
Schritt 5. Entfernen Sie bei Bedarf eine orale Spritze aus der Verpackung.
Verwenden Sie nur die oralen Spritzen, die mit FintePla versehen sind.
Wenn eine orale Spritze beschädigt ist oder Sie die Dosismarkierungen nicht lesen können:
- Verwenden Sie die andere mündliche Spritze oder
- Wenden Sie sich an den Apotheker, um eine neue zu erhalten.
| |
Schritt 6. Stellen Sie sicher, dass der Kolben bis in die Mundspritze gedrängt wird.
| |
Schritt 7. Halten Sie die Flasche Medizin fest auf einer harten flachen Oberfläche.
Schritt 8. Schieben Sie die Spitze der oralen Spritze in die Öffnung des Adapters, bis sie nicht weiter gedrückt werden kann.
| |
Schritt 9. Halten Sie die mündliche Spritze und füllen Sie zusammen und drehen Sie sich auf den Kopf.
| |
Schritt 10. Ziehen Sie langsam den Kolben der oralen Spritze, um die vorgeschriebene Dosis zurückzuziehen.
| |
| |
| |
Vorbereitung einer Dosis (Fortsetzung)
Schritt 11. Richten Sie das Ende des Kolbens mit der Marke für die vorgeschriebene Dosis auf der oralen Spritze aus.
Tipps zur richtigen Dosis
- Wenn Sie zu viel Medizin herausziehen:
- Lassen Sie die orale Spritze im Adapter.
- Drücken Sie den Kolben langsam zurück in die Spritze, bis Sie die vorgeschriebene Dosis erreichen.
- Wenn Sie Luftblasen in der Medizin sehen:
- Lassen Sie die orale Spritze im Adapter.
- Ziehen Sie den Kolben weiter nach unten.
- Lassen Sie die Blasen zur Spitze der Spritze aufsteigen.
- Schieben Sie den Kolben auf den Weg.
- Ziehen Sie den Kolben langsam zur vorgeschriebenen Dosis.
Notiz: Sehr kleine Blasen in der Flüssigkeit sind normal.
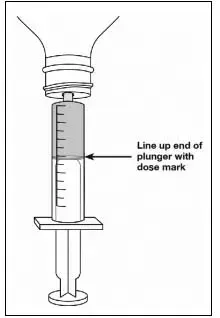
Schritt 12. Halten Sie die orale Spritze und flaschen Sie zusammen und drehen Sie dann die Flasche rechts nach oben.
| |
Schritt 13. Halten Sie die Flasche fest vorsichtig, um die orale Spritze aus dem Flaschenadapter zu ziehen.
| |
Schritt 14. Stellen Sie sicher, dass die Dosis in der oralen Spritze immer noch mit der vorgeschriebenen Dosis übereinstimmt.
Wenn die Dosis nicht übereinstimmt:
- Setzen Sie die Spritze wieder in den Adapter.
- Siehe die Schritte 9 bis 11, um die Dosis nach Bedarf anzupassen.
FINTEPLA geben
Schritt 15. Legen Sie die Spitze der oralen Spritze gegen die Innenseite der Wange.
Schritt 16. Schieben Sie den Kolben vorsichtig hinein, bis die gesamte Medizin in der oralen Spritze angegeben ist.
| |
- Nicht Spritzen Sie die Medizin in den Rücken des Hals. Dies kann zum Ersticken führen.
Schritt 17. Legen Sie die Kappe wieder auf die Flasche, indem Sie die Kappe (im Uhrzeigersinn) nach rechts drehen, bis sie anhält.
- Lassen Sie den Adapter immer an Ort und Stelle in the bottle
- Die Kappe passt darüber.
| |
Reinigen Sie die Spritze
- Spülen Sie die orale Spritze mit sauberem Leitungswasser aus und lassen Sie sie nach jedem Gebrauch lufttrocknen.
- Stellen Sie sicher, dass Sie die Innenseite der Spritze und den Kolben ausspülen.
Reinigungstipps:
- Ziehen Sie das saubere Leitungswasser mit dem Kolben in die Spritze und schieben Sie es mehrmals heraus, um die Spritze zu reinigen.
- Entfernen Sie den Kolben aus dem Lauf der oralen Spritze
- Spülen Sie beide Teile unter Leitungswasser aus
- Stellen Sie sicher, dass die Spritze und der Kolben vor dem nächsten Gebrauch vollständig trocken sind.
- Die Spritze ist auch sicher im Geschirrspüler zu reinigen.
| |
Wie soll ich FINTEPLA aufbewahren?
- Lagern Sie FintePla bei Raumtemperatur zwischen 68 ° F und 77 ° F (25 bis 25 ° C).
- Nicht kühlen oder einfrieren.
- Halten Sie die Kappe dicht geschlossen und die Flasche aufrecht.
- Lagern Sie die FINTEPLA -Flasche und spritzen Sie zusammen in einem sauberen Bereich.
- Werfen Sie alle nicht verwendeten FintePla weg (verwerfen) 3 Monate nach dem ersten Öffnen der Flasche oder wenn das Verwerfen nach dem Datum auf dem Paket oder der Flasche vergangen ist. Was auch immer man an erster Stelle kommt.
- Halten Sie FintePla und alle Medikamente außerhalb der Reichweite der Kinder.
Diese Verwendung wurden von der US -amerikanischen Food and Drug Administration genehmigt.
